ಭೌತಿಕವಾಗಿ ವಿಸರ್ಜನೆ ರಾಸಾಯನಿಕ ಪ್ರಕ್ರಿಯೆ
ದ್ರಾವಕ ಮತ್ತು ದ್ರಾವಕದ ಪರಸ್ಪರ ಕ್ರಿಯೆಯಿಂದ ಪರಿಹಾರಗಳು ರೂಪುಗೊಳ್ಳುತ್ತವೆ. ದ್ರಾವಕ ಮತ್ತು ದ್ರಾವಕದ ನಡುವಿನ ಪರಸ್ಪರ ಕ್ರಿಯೆಯ ಪ್ರಕ್ರಿಯೆಯನ್ನು ಸಾಲ್ವೇಶನ್ ಎಂದು ಕರೆಯಲಾಗುತ್ತದೆ (ದ್ರಾವಕವು ನೀರು ಆಗಿದ್ದರೆ - ಜಲಸಂಚಯನ).

ಚಿತ್ರ 1 ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳನ್ನು ಕರಗಿಸುವ ಪ್ರಕ್ರಿಯೆ.
ವಿಸರ್ಜನೆಯು ವಿಭಿನ್ನ ಆಕಾರಗಳು ಮತ್ತು ಸಾಮರ್ಥ್ಯಗಳ ಉತ್ಪನ್ನಗಳ ರಚನೆಯೊಂದಿಗೆ ಮುಂದುವರಿಯುತ್ತದೆ - ಹೈಡ್ರೇಟ್ಗಳು. ಇದು ದೈಹಿಕ ಮತ್ತು ಎರಡನ್ನೂ ಒಳಗೊಂಡಿರುತ್ತದೆ ರಾಸಾಯನಿಕ ಪ್ರಕೃತಿ. ಘಟಕಗಳ ಈ ರೀತಿಯ ಪರಸ್ಪರ ಕ್ರಿಯೆಯ ಕಾರಣದಿಂದಾಗಿ ವಿಸರ್ಜನೆಯ ಪ್ರಕ್ರಿಯೆಯು ವಿವಿಧ ಉಷ್ಣ ವಿದ್ಯಮಾನಗಳೊಂದಿಗೆ ಇರುತ್ತದೆ.
ಶಕ್ತಿ ಗುಣಲಕ್ಷಣಗಳುವಿಸರ್ಜನೆಯು ದ್ರಾವಣದ ರಚನೆಯ ಶಾಖವಾಗಿದೆ, ಇದನ್ನು ಪರಿಗಣಿಸಲಾಗುತ್ತದೆ ಬೀಜಗಣಿತದ ಮೊತ್ತಪ್ರಕ್ರಿಯೆಯ ಎಲ್ಲಾ ಎಂಡೋ- ಮತ್ತು ಎಕ್ಸೋಥರ್ಮಿಕ್ ಹಂತಗಳ ಉಷ್ಣ ಪರಿಣಾಮಗಳು. ಅವುಗಳಲ್ಲಿ ಅತ್ಯಂತ ಗಮನಾರ್ಹವಾದವುಗಳು:
- ಶಾಖ-ಹೀರಿಕೊಳ್ಳುವ ಪ್ರಕ್ರಿಯೆಗಳು - ಸ್ಫಟಿಕ ಜಾಲರಿಯ ನಾಶ, ಅಣುಗಳಲ್ಲಿನ ರಾಸಾಯನಿಕ ಬಂಧಗಳನ್ನು ಮುರಿಯುವುದು;
ಶಾಖ-ಉತ್ಪಾದಿಸುವ ಪ್ರಕ್ರಿಯೆಗಳು - ದ್ರಾವಕ (ಹೈಡ್ರೇಟ್ಗಳು) ಜೊತೆಗೆ ಕರಗಿದ ವಸ್ತುವಿನ ಪರಸ್ಪರ ಕ್ರಿಯೆಯ ಉತ್ಪನ್ನಗಳ ರಚನೆ.
ವಿನಾಶದ ಶಕ್ತಿಯಾಗಿದ್ದರೆ ಸ್ಫಟಿಕ ಜಾಲರಿಕರಗಿದ ವಸ್ತುವಿನ ಕಡಿಮೆ ಜಲಸಂಚಯನ ಶಕ್ತಿ, ನಂತರ ಶಾಖದ ಬಿಡುಗಡೆಯೊಂದಿಗೆ ವಿಸರ್ಜನೆ ಸಂಭವಿಸುತ್ತದೆ (ಬೆಚ್ಚಗಾಗುವಿಕೆಯನ್ನು ಗಮನಿಸಲಾಗಿದೆ). ಹೀಗಾಗಿ, NaOH ವಿಸರ್ಜನೆಯು ಎಕ್ಸೋಥರ್ಮಿಕ್ ಪ್ರಕ್ರಿಯೆಯಾಗಿದೆ: 884 kJ/mol ಸ್ಫಟಿಕ ಜಾಲರಿಯ ನಾಶಕ್ಕೆ ಖರ್ಚುಮಾಡಲಾಗುತ್ತದೆ ಮತ್ತು ಹೈಡ್ರೀಕರಿಸಿದ Na+ ಮತ್ತು OH- ಅಯಾನುಗಳ ರಚನೆಯ ಸಮಯದಲ್ಲಿ, ಕ್ರಮವಾಗಿ 422 ಮತ್ತು 510 kJ/mol ಬಿಡುಗಡೆಯಾಗುತ್ತವೆ.
ಸ್ಫಟಿಕ ಜಾಲರಿಯ ಶಕ್ತಿಯು ಜಲಸಂಚಯನ ಶಕ್ತಿಗಿಂತ ಹೆಚ್ಚಿದ್ದರೆ, ಶಾಖದ ಹೀರಿಕೊಳ್ಳುವಿಕೆಯೊಂದಿಗೆ ವಿಸರ್ಜನೆಯು ಸಂಭವಿಸುತ್ತದೆ (NH 4 NO 3 ನ ಜಲೀಯ ದ್ರಾವಣವನ್ನು ತಯಾರಿಸುವಾಗ, ತಾಪಮಾನದಲ್ಲಿ ಇಳಿಕೆ ಕಂಡುಬರುತ್ತದೆ).
ದ್ರವಗಳಲ್ಲಿ ದ್ರವಗಳು ಅಥವಾ ಘನವಸ್ತುಗಳ ಪರಸ್ಪರ ಕರಗುವಿಕೆಯು ಈ ವಸ್ತುಗಳ ಹಲವಾರು ಗುಣಲಕ್ಷಣಗಳನ್ನು ಅವಲಂಬಿಸಿರುತ್ತದೆ: ರಾಸಾಯನಿಕ ಸ್ವರೂಪ, ಗಾತ್ರ ಮತ್ತು ಕಣಗಳ ರಚನೆ, ವಿದ್ಯುದಾವೇಶ(ಅಯಾನುಗಳ ಸಂದರ್ಭದಲ್ಲಿ), ದ್ವಿಧ್ರುವಿ ಕ್ಷಣಗಳು, ಇತ್ಯಾದಿ.
ಅನಿಯಮಿತ ಕರಗುವಿಕೆ ಎಂದು ಕರೆಯಲ್ಪಡುತ್ತದೆ, ಎರಡು ದ್ರವಗಳು ಎಲ್ಲಾ ಪ್ರಮಾಣದಲ್ಲಿ ಪರಸ್ಪರ ಕರಗಿದಾಗ ಮತ್ತು ಸೀಮಿತವಾದಾಗ, ಇನ್ನೊಂದು ದ್ರವದ ಕರಗುವಿಕೆಯು ಒಂದು ನಿರ್ದಿಷ್ಟ ಸಾಂದ್ರತೆಗೆ ಸೀಮಿತವಾಗಿರುತ್ತದೆ.
ಎ ಮತ್ತು ಬಿ ಎರಡು ದ್ರವಗಳ ಸೀಮಿತ ಪರಸ್ಪರ ಕರಗುವಿಕೆಯೊಂದಿಗೆ, ಪ್ರತಿಯೊಂದೂ ಕರಗುತ್ತದೆ, ಮತ್ತು ನೆಲೆಸಿದ ನಂತರ, ಎರಡು ಪದರಗಳು ರೂಪುಗೊಳ್ಳುತ್ತವೆ, ಅವು ಸಾಂದ್ರತೆಯನ್ನು ಕಡಿಮೆ ಮಾಡುವ ಕ್ರಮದಲ್ಲಿ ಒಂದರ ಮೇಲೊಂದು ನೆಲೆಗೊಂಡಿವೆ ಮತ್ತು A ಯಲ್ಲಿ B ಯ ಪರಿಹಾರವನ್ನು ಒಳಗೊಂಡಿರುತ್ತವೆ ಮತ್ತು B ಯಲ್ಲಿ A ಯ ಪರಿಹಾರದ ಇನ್ನೊಂದು.
ಪರಿಹಾರಗಳು ರಾಸಾಯನಿಕ ಸಂಯುಕ್ತಗಳು ಮತ್ತು ಯಾಂತ್ರಿಕ ಮಿಶ್ರಣಗಳ ನಡುವೆ ಮಧ್ಯಂತರ ಸ್ಥಾನವನ್ನು ಆಕ್ರಮಿಸುತ್ತವೆ. ಪರಿಹಾರಗಳು ರಾಸಾಯನಿಕ ಸಂಯುಕ್ತಗಳಿಂದ ಅವುಗಳ ಸಂಯೋಜನೆಯ ವ್ಯತ್ಯಾಸದಿಂದ ಮತ್ತು ಎರಡನೆಯದರಿಂದ ಅವುಗಳ ಏಕರೂಪತೆಯಿಂದ ಭಿನ್ನವಾಗಿರುತ್ತವೆ. ಅದಕ್ಕಾಗಿಯೇ ಪರಿಹಾರಗಳನ್ನು ವೇರಿಯಬಲ್ ಸಂಯೋಜನೆಯ ಏಕ-ಹಂತದ ವ್ಯವಸ್ಥೆಗಳು ಎಂದು ಕರೆಯಲಾಗುತ್ತದೆ, ಇದು ಕನಿಷ್ಠ ಎರಡು ಸ್ವತಂತ್ರ ಘಟಕಗಳಿಂದ ರೂಪುಗೊಂಡಿದೆ.
DI. ವಿಸರ್ಜನೆಯನ್ನು ಮಾತ್ರವಲ್ಲದೆ ಪರಿಗಣಿಸಿದವರಲ್ಲಿ ಮೆಂಡಲೀವ್ ಮೊದಲಿಗರು ಭೌತಿಕ ಪ್ರಕ್ರಿಯೆ, ಆದರೆ ಒಂದು ಪ್ರಕ್ರಿಯೆಯಾಗಿ ರಾಸಾಯನಿಕ ಪರಸ್ಪರ ಕ್ರಿಯೆದ್ರಾವಕದೊಂದಿಗೆ ದ್ರಾವಕ. ನಿರ್ದಿಷ್ಟವಾಗಿ ಹೇಳುವುದಾದರೆ, ವಿಸರ್ಜನೆಯ ಸಮಯದಲ್ಲಿ, ಶಕ್ತಿ (ದ್ರಾವಣದ ಶಾಖ) ಯಾವಾಗಲೂ ಹೀರಲ್ಪಡುತ್ತದೆ ಅಥವಾ ಬಿಡುಗಡೆಯಾಗುತ್ತದೆ ಮತ್ತು ದ್ರವದ ಪರಿಮಾಣವು ಬದಲಾಗುತ್ತದೆ.
ಬಳಸುವ ಪರಿಹಾರಗಳ ಅಧ್ಯಯನ ವಿವಿಧ ವಿಧಾನಗಳುಅವುಗಳಲ್ಲಿ ಹಲವು ಸಾಲ್ವೇಟ್ಗಳು ಅಥವಾ ಹೈಡ್ರೇಟ್ಗಳು ಎಂದು ಕರೆಯಲ್ಪಡುವ ಉಪಸ್ಥಿತಿಯನ್ನು ಸ್ಥಾಪಿಸಲು ಸಾಧ್ಯವಾಗಿಸಿತು, ಇದು ಪರಿಹಾರ ಮತ್ತು ಜಲಸಂಚಯನದ ಅನುಗುಣವಾದ ಪ್ರಕ್ರಿಯೆಗಳ ಪರಿಣಾಮವಾಗಿ ರೂಪುಗೊಳ್ಳುತ್ತದೆ.
ಜಲೀಯ ದ್ರಾವಣಗಳಲ್ಲಿನ ವಸ್ತುಗಳ ಜಲಸಂಚಯನವು ಯಾವುದೇ ದ್ರಾವಕದಿಂದ ಪರಿಹಾರದ ಪ್ರತ್ಯೇಕ ಪ್ರಕರಣವಾಗಿದೆ. ದ್ರಾವಕವು ನೀರಾಗಿದ್ದರೆ, ಈ ಸಂಯುಕ್ತಗಳನ್ನು ಹೈಡ್ರೇಟ್ ಎಂದು ಕರೆಯಲಾಗುತ್ತದೆ. ಜಲಸಂಚಯನ ಪ್ರಕ್ರಿಯೆಯನ್ನು ಒಂದು ವಸ್ತುವಿಗೆ ನೀರನ್ನು ಸೇರಿಸುವ ರಾಸಾಯನಿಕ ಕ್ರಿಯೆ ಎಂದು ಪರಿಗಣಿಸಬೇಕು. ನೀರಿನ ಅಣುಗಳು ಮತ್ತು ಹೈಡ್ರೀಕರಿಸಿದ ವಸ್ತುವಿನ ನಡುವಿನ ಆಣ್ವಿಕ ಪರಸ್ಪರ ಕ್ರಿಯೆಯ ಶಕ್ತಿಗಳ ಪ್ರಭಾವದ ಅಡಿಯಲ್ಲಿ ಜಲಸಂಚಯನ ಸಂಭವಿಸುತ್ತದೆ. ಗಮನಾರ್ಹವಾದ ಅಯಾನುಗಳಿಂದ ಲವಣಗಳು ಹೈಡ್ರೀಕರಿಸಲ್ಪಡುತ್ತವೆ ವಿದ್ಯುತ್ ಕ್ಷೇತ್ರಗಳು, ಇದು ವಿದ್ಯುತ್ ಧ್ರುವೀಯ ನೀರಿನ ಅಣುಗಳನ್ನು ಆಕರ್ಷಿಸುತ್ತದೆ. ಹೇಗೆ ಬಲವಾದ ಕ್ಷೇತ್ರಅಯಾನ್, ಅಂದರೆ, ಅದರ ಚಾರ್ಜ್ ಮತ್ತು ಚಿಕ್ಕದಾದ ತ್ರಿಜ್ಯವು ಹೆಚ್ಚು ಬಲವಾಗಿ ಹೈಡ್ರೀಕರಿಸಲ್ಪಟ್ಟಿದೆ ಮತ್ತು ಬಲವಾದ ಹೈಡ್ರೇಟ್ಗಳು ರೂಪುಗೊಳ್ಳುತ್ತವೆ. ಅನೇಕ ಸಂದರ್ಭಗಳಲ್ಲಿ ಸಾಲ್ವೇಟ್ಗಳ ರಚನೆಯು ದ್ರಾವಕದ ಗುಣಲಕ್ಷಣಗಳನ್ನು ಬದಲಾಯಿಸುತ್ತದೆ, ಇದನ್ನು ನೇರ ವೀಕ್ಷಣೆಯಿಂದ ಸುಲಭವಾಗಿ ನಿರ್ಧರಿಸಲಾಗುತ್ತದೆ.
ಉದಾಹರಣೆಗೆ, ಪ್ರತ್ಯೇಕ ಅಣುಗಳನ್ನು ಒಳಗೊಂಡಿರುವ ಅಯೋಡಿನ್, ಅನಿಲ ಸ್ಥಿತಿಯಲ್ಲಿ ನೇರಳೆ ಬಣ್ಣವನ್ನು ಹೊಂದಿರುತ್ತದೆ. ಅಯೋಡಿನ್ ಅನ್ನು ಗ್ಯಾಸೋಲಿನ್ನಲ್ಲಿ ಕರಗಿಸಿದಾಗ ಅದೇ ಬಣ್ಣವನ್ನು ಸಂರಕ್ಷಿಸಲಾಗಿದೆ. ಅಯೋಡಿನ್ ಅನ್ನು ಆಲ್ಕೋಹಾಲ್ನಲ್ಲಿ ಕರಗಿಸಿದರೆ, ದ್ರಾವಣವು ಗಾಢ ಕಂದು ಬಣ್ಣದ್ದಾಗಿರುತ್ತದೆ. ಈ ಬಣ್ಣ ಬದಲಾವಣೆಯು ಅಯೋಡಿನ್ ಮತ್ತು ಆಲ್ಕೋಹಾಲ್ ಅಣುಗಳ ನಡುವಿನ ಪರಸ್ಪರ ಕ್ರಿಯೆಯ ಉಪಸ್ಥಿತಿಯನ್ನು ಸೂಚಿಸುತ್ತದೆ.
ಹೈಡ್ರೇಟ್ಗಳು ಅಸ್ಥಿರ ಸಂಯುಕ್ತಗಳಾಗಿವೆ; ಅನೇಕ ಸಂದರ್ಭಗಳಲ್ಲಿ ದ್ರಾವಣಗಳು ಆವಿಯಾದಾಗ ಅವು ಕೊಳೆಯುತ್ತವೆ. ಆದರೆ ಕೆಲವೊಮ್ಮೆ ಜಲಸಂಚಯನ ನೀರು ಕರಗಿದ ವಸ್ತುವಿನ ಅಣುಗಳಿಗೆ ತುಂಬಾ ಬಿಗಿಯಾಗಿ ಬಂಧಿಸಲ್ಪಡುತ್ತದೆ, ಎರಡನೆಯದನ್ನು ದ್ರಾವಣದಿಂದ ಬೇರ್ಪಡಿಸಿದಾಗ, ಅದು ಅದರ ಸ್ಫಟಿಕಗಳ ಭಾಗವಾಗುತ್ತದೆ. ಅಂತಹ ಔಷಧೀಯ ಪದಾರ್ಥಗಳಲ್ಲಿ ಗ್ಲೂಕೋಸ್, ಟೆರ್ಪೀನ್ ಹೈಡ್ರೇಟ್, ಮೆಗ್ನೀಸಿಯಮ್ ಸಲ್ಫೇಟ್, ತಾಮ್ರದ ಸಲ್ಫೇಟ್, ಅಲ್ಯೂಮ್, ಕೊಡೈನ್ ಇತ್ಯಾದಿಗಳು ಸೇರಿವೆ, ಇವುಗಳು ಸ್ಫಟಿಕದಂತಹ ಹೈಡ್ರೇಟ್ಗಳಾಗಿವೆ. ವಿಭಿನ್ನ ವಿಷಯಸ್ಫಟಿಕೀಕರಣದ ನೀರು. ಸ್ಫಟಿಕದಂತಹ ಹೈಡ್ರೇಟ್ಗಳಿಂದ ನೀರನ್ನು ತೆಗೆದುಹಾಕಿದಾಗ, ಅವು ಬದಲಾಗುತ್ತವೆ ಕಾಣಿಸಿಕೊಂಡಮತ್ತು ವೈಯಕ್ತಿಕ ಗುಣಲಕ್ಷಣಗಳು(ತಾಮ್ರದ ಸಲ್ಫೇಟ್, ಜಿಪ್ಸಮ್, ಸ್ಫಟಿಕದ ಸೋಡಾ, ಇತ್ಯಾದಿ).
ನೀರಿನಲ್ಲಿ ಕರಗಿದ ಉಪ್ಪಿನ ಪ್ರತ್ಯೇಕ ಅಯಾನುಗಳು ಸಹ ಹೈಡ್ರೀಕರಿಸಿದ ಸ್ಥಿತಿಯಲ್ಲಿ ಉಳಿಯುತ್ತವೆ, ಇದು ಉಪ್ಪು ದ್ರಾವಣಗಳ ಅನೇಕ ಗುಣಲಕ್ಷಣಗಳಿಗೆ ನಿರ್ಣಾಯಕ ಪ್ರಾಮುಖ್ಯತೆಯನ್ನು ಹೊಂದಿದೆ. ದ್ರಾವಣಗಳಲ್ಲಿ ಅಯಾನುಗಳ ಜಲಸಂಚಯನದ ಕಲ್ಪನೆಯನ್ನು ಮೊದಲು ವ್ಯಕ್ತಪಡಿಸಿದವರು I.A. ಕಬ್ಲುಕೋವ್ ಮತ್ತು ವಿ.ಎ. ಕಿಸ್ಟ್ಯಾಕೋವ್ಸ್ಕಿ.
ನೀರಿನಲ್ಲಿ (ಅಥವಾ ಇತರ ದ್ರಾವಕಗಳು) ಅನೇಕ ಪದಾರ್ಥಗಳ ಸೀಮಿತಗೊಳಿಸುವ ಕರಗುವಿಕೆ ಸ್ಥಿರ ಮೌಲ್ಯ, ನಿರ್ದಿಷ್ಟ ತಾಪಮಾನದಲ್ಲಿ ಸ್ಯಾಚುರೇಟೆಡ್ ದ್ರಾವಣದ ಸಾಂದ್ರತೆಗೆ ಅನುಗುಣವಾಗಿರುತ್ತದೆ. ಇದು ಕರಗುವಿಕೆಯ ಗುಣಾತ್ಮಕ ಲಕ್ಷಣವಾಗಿದೆ ಮತ್ತು 100 ಗ್ರಾಂ ದ್ರಾವಕಕ್ಕೆ (ಕೆಲವು ಪರಿಸ್ಥಿತಿಗಳಲ್ಲಿ) ಗ್ರಾಂನಲ್ಲಿ ಉಲ್ಲೇಖ ಪುಸ್ತಕಗಳಲ್ಲಿ ನೀಡಲಾಗಿದೆ.
ಹರಡುವ ಬೆಳಕಿನಲ್ಲಿ ಗಮನಿಸಿದಾಗ ದ್ರಾವಣದಲ್ಲಿ ವಸ್ತುವಿನ ಯಾವುದೇ ಕಣಗಳು ಪತ್ತೆಯಾಗದಿದ್ದರೆ ಔಷಧವನ್ನು ಕರಗಿಸಲಾಗುತ್ತದೆ ಎಂದು ಪರಿಗಣಿಸಲಾಗುತ್ತದೆ. ಕರಗುವಿಕೆಗೆ ಸಂಬಂಧಿಸಿದಂತೆ, ಅವರು ಸ್ವಲ್ಪ ಮಟ್ಟಿಗೆ ಹಳೆಯ ತತ್ವದಿಂದ ಮಾರ್ಗದರ್ಶಿಸಲ್ಪಡುತ್ತಾರೆ "ಹಾಗೆ ಕರಗುತ್ತದೆ" ( ಸಿಮಿಲಿಯಾ ಸಿಮಿಲಿಬಸ್ ಸಾಲ್ವೆಂಟೂರ್), ಅಂದರೆ, ಬೆಳಕಿನಲ್ಲಿ ಆಧುನಿಕ ವೀಕ್ಷಣೆಗಳುಅಣುವಿನ ರಚನೆಯ ಆಧಾರದ ಮೇಲೆ, ಇದು ಈ ರೀತಿ ತೋರುತ್ತದೆ: ಧ್ರುವೀಯವಲ್ಲದ ದ್ರಾವಕಗಳಲ್ಲಿ (ಗ್ಯಾಸೋಲಿನ್, ಈಥರ್, ಇತ್ಯಾದಿ) ಧ್ರುವೀಯವಲ್ಲದ ಅಥವಾ ಕಡಿಮೆ-ಧ್ರುವೀಯ ಅಣುಗಳೊಂದಿಗೆ ವಿವಿಧ ಸಂಯುಕ್ತಗಳು ಚೆನ್ನಾಗಿ ಕರಗುತ್ತವೆ ಮತ್ತು ಇತರ ವಿಧದ ವಸ್ತುಗಳು ಕರಗುವುದಿಲ್ಲ. ಇದಕ್ಕೆ ವಿರುದ್ಧವಾಗಿ, ಅಣುಗಳ (ನೀರು) ಬಲವಾಗಿ ಧ್ರುವೀಯ ಪಾತ್ರವನ್ನು ಹೊಂದಿರುವ ದ್ರಾವಕವು ನಿಯಮದಂತೆ, ಧ್ರುವೀಯ ಮತ್ತು ಭಾಗಶಃ ಅಣುಗಳೊಂದಿಗೆ ವಸ್ತುಗಳನ್ನು ಕರಗಿಸುತ್ತದೆ. ಅಯಾನಿಕ್ ವಿಧಗಳುಮತ್ತು ಧ್ರುವೀಯವಲ್ಲದ ಅಣುಗಳೊಂದಿಗೆ ಪದಾರ್ಥಗಳನ್ನು ಕರಗಿಸುವುದಿಲ್ಲ. ಧ್ರುವೀಯ ದ್ರಾವಕಗಳು ದೊಡ್ಡ ಡೈಎಲೆಕ್ಟ್ರಿಕ್ ಸ್ಥಿರ, ದೊಡ್ಡ ದ್ವಿಧ್ರುವಿ ಕ್ಷಣ, ಉಪಸ್ಥಿತಿಯೊಂದಿಗೆ ಸಂಯೋಜಿಸುವ ದ್ರವಗಳನ್ನು ಒಳಗೊಂಡಿರುತ್ತವೆ. ಕ್ರಿಯಾತ್ಮಕ ಗುಂಪುಗಳು, ಸಮನ್ವಯದ ರಚನೆಯನ್ನು ಖಚಿತಪಡಿಸುವುದು ( ಬಹುತೇಕ ಭಾಗಹೈಡ್ರೋಜನ್) ಬಂಧಗಳು: ನೀರು, ಆಮ್ಲಗಳು, ಕಡಿಮೆ ಆಲ್ಕೋಹಾಲ್ಗಳು ಮತ್ತು ಗ್ಲೈಕೋಲ್ಗಳು, ಅಮೈನ್ಗಳು, ಇತ್ಯಾದಿ. ವಸ್ತುವಿನ ಅಣುವಿನಲ್ಲಿ ಧ್ರುವೀಯ ಗುಂಪುಗಳ ಉಪಸ್ಥಿತಿಯು ಅದರ ಕರಗುವಿಕೆಯ ಮೇಲೆ ಹೆಚ್ಚು ಪರಿಣಾಮ ಬೀರುತ್ತದೆ.
ನಿಯಮದಂತೆ, ಪ್ರತಿ ಧ್ರುವೀಯ ಗುಂಪಿಗೆ ಮೂರು ಹೈಡ್ರೋಕಾರ್ಬನ್ ರಾಡಿಕಲ್ ಪರಮಾಣುಗಳಿಗಿಂತ ಹೆಚ್ಚು ಇಲ್ಲದಿದ್ದರೆ ವಸ್ತುಗಳು ನೀರಿನಲ್ಲಿ ಮತ್ತು ಪರಸ್ಪರ ಹೆಚ್ಚು ಕರಗುತ್ತವೆ. ಹೈಡ್ರೋಕಾರ್ಬನ್ ರಾಡಿಕಲ್ಗಳ ಹೆಚ್ಚಿನ ಉಪಸ್ಥಿತಿಯೊಂದಿಗೆ, ಅಂತಹ ದೊಡ್ಡ ಪ್ರಸರಣ ಶಕ್ತಿಗಳು ಅಣುಗಳ ನಡುವೆ ಉದ್ಭವಿಸುತ್ತವೆ, ಅವು ಧ್ರುವೀಯ ದ್ರಾವಕಗಳಲ್ಲಿ ಅಂತಹ ಪದಾರ್ಥಗಳ ವಿಸರ್ಜನೆಯನ್ನು ತಡೆಯುತ್ತವೆ.
ಧ್ರುವೀಯ ಪದಾರ್ಥಗಳು ಅಯಾನಿಕ್ (ಅಯಾನಿಕ್ ಸ್ಫಟಿಕಗಳು) ಮತ್ತು ಧ್ರುವೀಯ ಬಂಧ(ಧ್ರುವೀಯ ಅಣುಗಳು), ಉದಾಹರಣೆಗೆ, ಸೋಡಿಯಂ ಕ್ಲೋರೈಡ್.
ಧ್ರುವೀಯವಲ್ಲದ ದ್ರಾವಕಗಳು ಸಕ್ರಿಯ ಕ್ರಿಯಾತ್ಮಕ ಗುಂಪುಗಳನ್ನು ಹೊಂದಿರದ ಸಣ್ಣ ದ್ವಿಧ್ರುವಿ ಕ್ಷಣದೊಂದಿಗೆ ದ್ರವಗಳನ್ನು ಒಳಗೊಂಡಿರುತ್ತವೆ, ಉದಾಹರಣೆಗೆ, ಹೈಡ್ರೋಕಾರ್ಬನ್ಗಳು, ಆಲ್ಕೈಲ್ ಹಾಲೈಡ್ಗಳು, ಇತ್ಯಾದಿ. ಧ್ರುವೀಯವಲ್ಲದ ವಸ್ತುಗಳು- ಇವುಗಳು ವಿದ್ಯುತ್ ಕಂಬಗಳಿಲ್ಲದೆ ಕಟ್ಟುನಿಟ್ಟಾಗಿ ಸಮ್ಮಿತೀಯ ರಚನೆಯ ವಸ್ತುಗಳು (ಉದಾಹರಣೆಗೆ, ಪ್ಯಾರಾಫಿನ್, ಟರ್ಪಂಟೈನ್, ಕರ್ಪೂರ, ಥೈಮೋಲ್, ಇತ್ಯಾದಿ).
ಆದಾಗ್ಯೂ, ಮೇಲಿನ ನಿಯಮವು ಯಾವಾಗಲೂ ಮಾನ್ಯವಾಗಿರುವುದಿಲ್ಲ, ವಿಶೇಷವಾಗಿ ಸಂಕೀರ್ಣಕ್ಕೆ ಅನ್ವಯಿಸಿದಾಗ ಸಾವಯವ ಸಂಯುಕ್ತಗಳು, ಧ್ರುವೀಯ (-OH, -SO 3 H, -NH 2, -COOH, -COONa) ಮತ್ತು ಧ್ರುವೀಯವಲ್ಲದ (ಆಲ್ಕೈಲ್ ಅಥವಾ ಆರಿಲ್ ರಾಡಿಕಲ್ಸ್) ಗುಂಪುಗಳನ್ನು ಒಳಗೊಂಡಿರುತ್ತದೆ. ಈ ಸಂಯುಕ್ತಗಳಲ್ಲಿ ಕಾರ್ಬೋಹೈಡ್ರೇಟ್ಗಳು, ಆಲ್ಕೋಹಾಲ್ಗಳು, ಕೀಟೋನ್ಗಳು, ಸಾವಯವ ಆಮ್ಲಗಳು, ಅಮೈನ್ಗಳು, ಇತ್ಯಾದಿ. ಈ ಪದಾರ್ಥಗಳ ಕರಗುವಿಕೆಯು ಧ್ರುವೀಯ ಅಥವಾ ಧ್ರುವೀಯ ಗುಂಪುಗಳ ಪ್ರಾಬಲ್ಯವನ್ನು ಅವಲಂಬಿಸಿರುತ್ತದೆ. ಉದಾಹರಣೆಗೆ, ಈಥೈಲ್ ಆಲ್ಕೋಹಾಲ್ C 2 H 5 OH ಯಾವುದೇ ಅನುಪಾತದಲ್ಲಿ ನೀರಿನೊಂದಿಗೆ ಬೆರೆಯುತ್ತದೆ, ಅಮೈಲ್ ಆಲ್ಕೋಹಾಲ್ C 5 H 11 OH - 10% ಕ್ಕಿಂತ ಹೆಚ್ಚಿಲ್ಲ, ಮತ್ತು cetyl ಆಲ್ಕೊಹಾಲ್ C 16 H 33 OH ಪ್ರಾಯೋಗಿಕವಾಗಿ ನೀರಿನಲ್ಲಿ ಕರಗುವುದಿಲ್ಲ.
ಕರಗುವಿಕೆ ದ್ರಾವಕ ಮತ್ತು ದ್ರಾವಕ, ತಾಪಮಾನ ಮತ್ತು ಒತ್ತಡದ ಸ್ವರೂಪವನ್ನು ಅವಲಂಬಿಸಿರುತ್ತದೆ.
1) ಕರಗುವ ವಸ್ತುವಿನ ಸ್ವರೂಪ.

Fig.2 ದ್ರಾವಣದ ಸ್ವರೂಪ.
ಸ್ಫಟಿಕದಂತಹ ಪದಾರ್ಥಗಳನ್ನು ವಿಂಗಡಿಸಲಾಗಿದೆ:
ಪಿ - ಹೆಚ್ಚು ಕರಗುವ (100 ಗ್ರಾಂ ನೀರಿಗೆ 1.0 ಗ್ರಾಂ ಗಿಂತ ಹೆಚ್ಚು);
ಎಂ - ಸ್ವಲ್ಪ ಕರಗುವ (0.1 ಗ್ರಾಂ - 100 ಗ್ರಾಂ ನೀರಿಗೆ 1.0 ಗ್ರಾಂ);
ಎಚ್ - ಕರಗದ (100 ಗ್ರಾಂ ನೀರಿಗೆ 0.1 ಗ್ರಾಂ ಗಿಂತ ಕಡಿಮೆ).
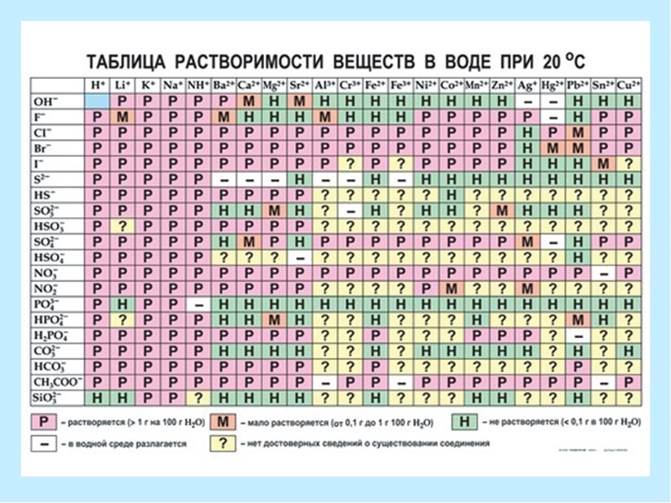
Fig.3. ಕರಗುವ ಟೇಬಲ್.
2) ದ್ರಾವಕದ ಸ್ವರೂಪ. ಪರಿಹಾರವು ರೂಪುಗೊಂಡಾಗ, ಪ್ರತಿ ಘಟಕದ ಕಣಗಳ ನಡುವಿನ ಬಂಧಗಳನ್ನು ಕಣಗಳ ನಡುವಿನ ಬಂಧಗಳಿಂದ ಬದಲಾಯಿಸಲಾಗುತ್ತದೆ. ವಿವಿಧ ಘಟಕಗಳು. ಹೊಸ ಬಂಧಗಳನ್ನು ರೂಪಿಸಲು, ಪರಿಹಾರದ ಘಟಕಗಳು ಒಂದೇ ರೀತಿಯ ಬಂಧಗಳನ್ನು ಹೊಂದಿರಬೇಕು, ಅಂದರೆ. ಅದೇ ಸ್ವಭಾವದವರಾಗಿರುತ್ತಾರೆ. ಅದಕ್ಕೇ ಅಯಾನಿಕ್ ಪದಾರ್ಥಗಳುಧ್ರುವೀಯ ದ್ರಾವಕಗಳಲ್ಲಿ ಮತ್ತು ಧ್ರುವೀಯವಲ್ಲದವುಗಳಲ್ಲಿ ಕಳಪೆಯಾಗಿ ಕರಗುತ್ತವೆ, ಮತ್ತು
ಆಣ್ವಿಕ ಪದಾರ್ಥಗಳು- ಪ್ರತಿಕ್ರಮದಲ್ಲಿ.
ನೀರು ಒಂದು ಅನನ್ಯ, ಅತ್ಯಂತ ಸಾಮಾನ್ಯ ಮತ್ತು ಪ್ರವೇಶಿಸಬಹುದಾದ ದ್ರಾವಕವಾಗಿದೆ. ಅಜೈವಿಕ (ಲವಣಗಳು, ಆಮ್ಲಗಳು, ಬೇಸ್ಗಳು) ಮತ್ತು ಸಾವಯವ (ಅಮೈನೋ ಆಮ್ಲಗಳು, ಸಾರಜನಕ ನೆಲೆಗಳು, ಜಲೀಯ ದ್ರಾವಣಗಳು, ನ್ಯೂಕ್ಲಿಯಿಕ್ ಆಮ್ಲಗಳು) ಪದಾರ್ಥಗಳು, ಕಡಿಮೆ - ಮತ್ತು ಹೆಚ್ಚಿನ ಆಣ್ವಿಕ ತೂಕದ ಸಂಯುಕ್ತಗಳು, ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳು ಮತ್ತು ಅಲ್ಲದ ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳು, ಅತ್ಯಂತ ಪ್ರಮುಖವಾದ ಆಧಾರವನ್ನು ರೂಪಿಸುತ್ತವೆ ಜೈವಿಕ ದ್ರವಗಳು, ಇದರಲ್ಲಿ ದೇಹದ ಜೀವನವನ್ನು ಖಾತ್ರಿಪಡಿಸುವ ಎಲ್ಲಾ ಭೌತಿಕ ಮತ್ತು ರಾಸಾಯನಿಕ ಪ್ರಕ್ರಿಯೆಗಳು ನಡೆಯುತ್ತವೆ. ಉದಾಹರಣೆಗೆ, ಔಷಧದಲ್ಲಿ ಅವರು ಜೈವಿಕ ದ್ರವಗಳ ಕೃತಕ ಸಾದೃಶ್ಯಗಳನ್ನು ಬಳಸುತ್ತಾರೆ - ಕೊಲೊಯ್ಡಲ್ ಮತ್ತು ಲವಣಯುಕ್ತ ರಕ್ತದ ಬದಲಿ ಪರಿಹಾರಗಳು.

ಅಕ್ಕಿ. 4. ಕರಗುವಿಕೆಯ ಸ್ವರೂಪದ ಮೇಲೆ ವಸ್ತುಗಳ ಕರಗುವಿಕೆಯ ಅವಲಂಬನೆ.
3) ತಾಪಮಾನದ ಪ್ರಭಾವ. ವಸ್ತುವಿನ ವಿಸರ್ಜನೆಯು ಎಕ್ಸೋಥರ್ಮಿಕ್ ಪ್ರಕ್ರಿಯೆಯಾಗಿದ್ದರೆ, ಹೆಚ್ಚುತ್ತಿರುವ ತಾಪಮಾನದೊಂದಿಗೆ ಅದರ ಕರಗುವಿಕೆ ಕಡಿಮೆಯಾಗುತ್ತದೆ (ಉದಾಹರಣೆಗೆ, ನೀರಿನಲ್ಲಿ Ca(OH)2) ಮತ್ತು ಪ್ರತಿಯಾಗಿ. ಹೆಚ್ಚಿನ ಲವಣಗಳು ಬಿಸಿಯಾದಾಗ ಕರಗುವಿಕೆಯ ಹೆಚ್ಚಳದಿಂದ ನಿರೂಪಿಸಲ್ಪಡುತ್ತವೆ. ಬಹುತೇಕ ಎಲ್ಲಾ ಅನಿಲಗಳು ಶಾಖದ ಬಿಡುಗಡೆಯೊಂದಿಗೆ ಕರಗುತ್ತವೆ. ದ್ರವಗಳಲ್ಲಿನ ಅನಿಲಗಳ ಕರಗುವಿಕೆಯು ಹೆಚ್ಚುತ್ತಿರುವ ತಾಪಮಾನದೊಂದಿಗೆ ಕಡಿಮೆಯಾಗುತ್ತದೆ ಮತ್ತು ಕಡಿಮೆ ತಾಪಮಾನದೊಂದಿಗೆ ಹೆಚ್ಚಾಗುತ್ತದೆ.
4) ಒತ್ತಡದ ಪರಿಣಾಮ. ಹೆಚ್ಚುತ್ತಿರುವ ಒತ್ತಡದೊಂದಿಗೆ, ದ್ರವಗಳಲ್ಲಿನ ಅನಿಲಗಳ ಕರಗುವಿಕೆಯು ಹೆಚ್ಚಾಗುತ್ತದೆ ಮತ್ತು ಕಡಿಮೆ ಒತ್ತಡದೊಂದಿಗೆ ಅದು ಕಡಿಮೆಯಾಗುತ್ತದೆ.
ಜೊತೆಗೆ ಪದಾರ್ಥಗಳ ಪರಿಹಾರಗಳು ಮೋಲಾರ್ ದ್ರವ್ಯರಾಶಿ 5000 g/mol ಗಿಂತ ಕಡಿಮೆಯಿರುವ ಪ್ರಮಾಣವನ್ನು ಕಡಿಮೆ ಆಣ್ವಿಕ ತೂಕದ ಸಂಯುಕ್ತಗಳ (LMC) ಪರಿಹಾರಗಳು ಎಂದು ಕರೆಯಲಾಗುತ್ತದೆ, ಮತ್ತು 5000 g/mol ಗಿಂತ ಹೆಚ್ಚಿನ ಮೋಲಾರ್ ದ್ರವ್ಯರಾಶಿಯನ್ನು ಹೊಂದಿರುವ ಪದಾರ್ಥಗಳ ಪರಿಹಾರಗಳನ್ನು ಹೆಚ್ಚಿನ ಆಣ್ವಿಕ ತೂಕದ ಸಂಯುಕ್ತಗಳ (HMC) ಪರಿಹಾರಗಳು ಎಂದು ಕರೆಯಲಾಗುತ್ತದೆ.
ಉಪಸ್ಥಿತಿ ಅಥವಾ ಅನುಪಸ್ಥಿತಿಯಿಂದ ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯ ವಿಘಟನೆ NMS ಪರಿಹಾರಗಳನ್ನು ಎರಡು ವರ್ಗಗಳಾಗಿ ವಿಂಗಡಿಸಲಾಗಿದೆ - ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳು ಮತ್ತು ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳಲ್ಲದ ಪರಿಹಾರಗಳು.
ಕೋಷ್ಟಕ 1.
ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳು ಮತ್ತು ಎಲೆಕ್ಟ್ರೋಲೈಟ್ ಅಲ್ಲದ ಕೋಷ್ಟಕ.
ಎಲೆಕ್ಟ್ರೋಲೈಟ್ ದ್ರಾವಣಗಳು ಲವಣಗಳು, ಆಮ್ಲಗಳು, ಬೇಸ್ಗಳು ಮತ್ತು ಆಂಫೋಲೈಟ್ಗಳ ಪರಿಹಾರಗಳಾಗಿವೆ, ಅದು ಅಯಾನುಗಳಾಗಿ ವಿಭಜನೆಯಾಗುತ್ತದೆ. ಉದಾಹರಣೆಗೆ, KNO3, HCl, KOH, Al(OH)3, ಗ್ಲೈಸಿನ್ನ ಪರಿಹಾರಗಳು. ಎಲೆಕ್ಟ್ರೋಲೈಟ್ ದ್ರಾವಣಗಳ ವಿದ್ಯುತ್ ವಾಹಕತೆಯು ದ್ರಾವಕಕ್ಕಿಂತ ಹೆಚ್ಚಾಗಿರುತ್ತದೆ.
ನಾನ್ ಎಲೆಕ್ಟ್ರೋಲೈಟ್ ದ್ರಾವಣಗಳು ನೀರಿನಲ್ಲಿ ಪ್ರಾಯೋಗಿಕವಾಗಿ ವಿಭಜನೆಯಾಗದ ವಸ್ತುಗಳ ಪರಿಹಾರಗಳಾಗಿವೆ. ಉದಾಹರಣೆಗೆ, ಸುಕ್ರೋಸ್, ಗ್ಲೂಕೋಸ್, ಯೂರಿಯಾದ ಪರಿಹಾರಗಳು. ಎಲೆಕ್ಟ್ರೋಲೈಟ್ ಅಲ್ಲದ ದ್ರಾವಣಗಳ ವಿದ್ಯುತ್ ವಾಹಕತೆಯು ದ್ರಾವಕದಿಂದ ಸ್ವಲ್ಪ ಭಿನ್ನವಾಗಿರುತ್ತದೆ.
NMS (ಎಲೆಕ್ಟ್ರೋಲೈಟ್ಗಳು ಮತ್ತು ಎಲೆಕ್ಟ್ರೋಲೈಟ್ಗಳಲ್ಲದ) ಪರಿಹಾರಗಳನ್ನು ಇದಕ್ಕೆ ವಿರುದ್ಧವಾಗಿ ನಿಜ ಎಂದು ಕರೆಯಲಾಗುತ್ತದೆ ಕೊಲೊಯ್ಡಲ್ ಪರಿಹಾರಗಳು. ನಿಜವಾದ ಪರಿಹಾರಗಳುಸಂಯೋಜನೆಯ ಏಕರೂಪತೆ ಮತ್ತು ದ್ರಾವಕ ಮತ್ತು ದ್ರಾವಕದ ನಡುವಿನ ಅಂತರಸಂಪರ್ಕದ ಅನುಪಸ್ಥಿತಿಯಿಂದ ನಿರೂಪಿಸಲಾಗಿದೆ. ಕರಗಿದ ಕಣಗಳ ಗಾತ್ರ (ಅಯಾನುಗಳು ಮತ್ತು ಅಣುಗಳು) 10 -9 ಮೀ ಗಿಂತ ಕಡಿಮೆ.
ಹೆಚ್ಚಿನ IUD ಗಳು ಪಾಲಿಮರ್ಗಳಾಗಿವೆ, ಇವುಗಳ ಅಣುಗಳು (ಮ್ಯಾಕ್ರೋಮಾಲಿಕ್ಯೂಲ್ಗಳು) ಒಳಗೊಂಡಿರುತ್ತವೆ ದೊಡ್ಡ ಸಂಖ್ಯೆಪುನರಾವರ್ತಿತ ಗುಂಪುಗಳು ಅಥವಾ ಮಾನೋಮರ್ ಘಟಕಗಳು ಪರಸ್ಪರ ಸಂಪರ್ಕ ಹೊಂದಿವೆ ರಾಸಾಯನಿಕ ಬಂಧಗಳು. IUD ಪರಿಹಾರಗಳನ್ನು ಪಾಲಿಎಲೆಕ್ಟ್ರೋಲೈಟ್ ಪರಿಹಾರಗಳು ಎಂದು ಕರೆಯಲಾಗುತ್ತದೆ.
ಪಾಲಿಎಲೆಕ್ಟ್ರೋಲೈಟ್ಗಳಲ್ಲಿ ಪಾಲಿಯಾಸಿಡ್ಗಳು (ಹೆಪಾರಿನ್, ಪಾಲಿಡೆನಿಲಿಕ್ ಆಮ್ಲ, ಪಾಲಿಯಾಸ್ಪಾರ್ಟಿಕ್ ಆಮ್ಲ, ಇತ್ಯಾದಿ), ಪಾಲಿಬೇಸ್ಗಳು (ಪಾಲಿಲೈಸಿನ್), ಪಾಲಿಯಂಫೋಲೈಟ್ಗಳು (ಪ್ರೋಟೀನ್ಗಳು, ನ್ಯೂಕ್ಲಿಯಿಕ್ ಆಮ್ಲಗಳು) ಸೇರಿವೆ.
IUD ಪರಿಹಾರಗಳ ಗುಣಲಕ್ಷಣಗಳು NMS ಪರಿಹಾರಗಳ ಗುಣಲಕ್ಷಣಗಳಿಂದ ಗಮನಾರ್ಹವಾಗಿ ಭಿನ್ನವಾಗಿವೆ.
ದೇಹಗಳು ಮತ್ತು ವಸ್ತುಗಳೊಂದಿಗೆ ವಿವಿಧ ಬದಲಾವಣೆಗಳು ಸಂಭವಿಸುತ್ತವೆ ಎಂದು ನಿಮಗೆ ಈಗಾಗಲೇ ತಿಳಿದಿದೆ, ಇದನ್ನು ವಿದ್ಯಮಾನಗಳು ಎಂದು ಕರೆಯಲಾಗುತ್ತದೆ ಮತ್ತು ಅವುಗಳನ್ನು ಭೌತಿಕ ಮತ್ತು ರಾಸಾಯನಿಕಗಳಾಗಿ ವಿಂಗಡಿಸಲಾಗಿದೆ ಎಂದು ನೆನಪಿಡಿ. ಭೌತಿಕ ವಿದ್ಯಮಾನಗಳಲ್ಲಿ, ಶುದ್ಧ ಸಂಯೋಜನೆ ಪ್ರತ್ಯೇಕ ವಸ್ತುಗಳುಬದಲಾಗದೆ ಉಳಿದಿದೆ, ಆದರೆ ಅವನದು ಮಾತ್ರ ಒಟ್ಟುಗೂಡಿಸುವಿಕೆಯ ಸ್ಥಿತಿಅಥವಾ ದೇಹಗಳ ಆಕಾರ ಮತ್ತು ಗಾತ್ರ.
ಭೌತಿಕ ವಿದ್ಯಮಾನಗಳು, ವಸ್ತುವಿನ ಒಟ್ಟು ಸ್ಥಿತಿ ಅಥವಾ ದೇಹಗಳ ಆಕಾರ ಮತ್ತು ಗಾತ್ರದಲ್ಲಿನ ಬದಲಾವಣೆಗಳಲ್ಲಿ ವ್ಯಕ್ತಪಡಿಸಲಾಗುತ್ತದೆ, ಅವುಗಳ ಅನ್ವಯದ ಪ್ರಮುಖ ಕ್ಷೇತ್ರಗಳನ್ನು ನಿರ್ಧರಿಸುತ್ತದೆ ರಾಷ್ಟ್ರೀಯ ಆರ್ಥಿಕತೆ. ಹೀಗಾಗಿ, ಅಲ್ಯೂಮಿನಿಯಂನ ಪ್ಲಾಸ್ಟಿಟಿಯು ಅದನ್ನು ತಂತಿಯೊಳಗೆ ಎಳೆಯಲು ಅಥವಾ ತೆಳುವಾದ ಫಾಯಿಲ್ಗೆ ಸುತ್ತುವಂತೆ ಮಾಡುತ್ತದೆ; ಅಲ್ಯೂಮಿನಿಯಂನ ವಿದ್ಯುತ್ ವಾಹಕತೆ ಮತ್ತು ತುಲನಾತ್ಮಕ ಲಘುತೆಯು ಅದನ್ನು ವಿದ್ಯುತ್ ಪ್ರಸರಣ ತಂತಿಗಳಾಗಿ ಬಳಸಲು ಸಾಧ್ಯವಾಗಿಸುತ್ತದೆ, ಮತ್ತು ಮಿಶ್ರಲೋಹಗಳು - ವಿಮಾನ ನಿರ್ಮಾಣದಲ್ಲಿ; ಉಷ್ಣ ವಾಹಕತೆ, ಪ್ಲಾಸ್ಟಿಟಿ ಮತ್ತು ವಿಷಕಾರಿಯಲ್ಲದ - ಭಕ್ಷ್ಯಗಳ ತಯಾರಿಕೆಯಲ್ಲಿ, ಇತ್ಯಾದಿ.
ಸ್ವಚ್ಛಗೊಳಿಸಲು ಹಲವು ಮಾರ್ಗಗಳು ರಾಸಾಯನಿಕ ವಸ್ತುಗಳುಮೂಲಭೂತವಾಗಿ ಭೌತಿಕ ವಿದ್ಯಮಾನಗಳಾಗಿವೆ. ಇವುಗಳಲ್ಲಿ ಬಟ್ಟಿ ಇಳಿಸುವಿಕೆ, ಸ್ಫಟಿಕೀಕರಣ, ಶೋಧನೆ, ಉತ್ಪತನ ಇತ್ಯಾದಿಗಳು ಸೇರಿವೆ. ಉದಾಹರಣೆಗೆ, ಬಟ್ಟಿ ಇಳಿಸುವಿಕೆಯ ವಿಧಾನ (ಚಿತ್ರ 84), ಅಥವಾ ಬಟ್ಟಿ ಇಳಿಸುವಿಕೆ, ಪದಾರ್ಥಗಳ ಕುದಿಯುವ ಬಿಂದುಗಳಲ್ಲಿನ ವ್ಯತ್ಯಾಸವನ್ನು ಆಧರಿಸಿದೆ.
ಅಕ್ಕಿ. 84.
ಬಟ್ಟಿ ಇಳಿಸುವಿಕೆ
ಈ ವಿಧಾನವು ಅದರಲ್ಲಿ ಕರಗಿದ ವಸ್ತುಗಳಿಂದ ಶುದ್ಧೀಕರಿಸಿದ ನೀರನ್ನು ಉತ್ಪಾದಿಸುತ್ತದೆ. ಈ ನೀರನ್ನು ಡಿಸ್ಟಿಲ್ಡ್ ಎಂದು ಕರೆಯಲಾಗುತ್ತದೆ. ಔಷಧೀಯ ಪರಿಹಾರಗಳನ್ನು ತಯಾರಿಸಲು ಮತ್ತು ಕಾರುಗಳ ತಂಪಾಗಿಸುವ ವ್ಯವಸ್ಥೆಗೆ ಸುರಿಯುವುದಕ್ಕಾಗಿ ಇದನ್ನು ಬಳಸಲಾಗುತ್ತದೆ.
ದ್ರವ ಮಿಶ್ರಣಗಳನ್ನು ಬೇರ್ಪಡಿಸುವ ವಿಧಾನವಾಗಿ ಬಟ್ಟಿ ಇಳಿಸುವಿಕೆಯನ್ನು ಪಡೆಯಲು ಬಳಸಲಾಗುತ್ತದೆ ನೈಸರ್ಗಿಕ ತೈಲವೈಯಕ್ತಿಕ ಪೆಟ್ರೋಲಿಯಂ ಉತ್ಪನ್ನಗಳು. ಕೈಗಾರಿಕಾ ಸ್ಥಾಪನೆತೈಲದ ನಿರಂತರ ಬಟ್ಟಿ ಇಳಿಸುವಿಕೆಗಾಗಿ, ಇದು ತೈಲವನ್ನು ಬಿಸಿಮಾಡಲು ಕೊಳವೆಯಾಕಾರದ ಕುಲುಮೆಯನ್ನು (ಚಿತ್ರ 85, 1) ಒಳಗೊಂಡಿರುತ್ತದೆ ಮತ್ತು ಬೇರ್ಪಡಿಸುವಿಕೆ, ಅಥವಾ ಸರಿಪಡಿಸುವಿಕೆ, ಕಾಲಮ್ (ಚಿತ್ರ 85, 2), ಅಲ್ಲಿ ತೈಲವನ್ನು ಭಿನ್ನರಾಶಿಗಳಾಗಿ ವಿಂಗಡಿಸಲಾಗಿದೆ (ಬಟ್ಟಿ ಇಳಿಸುತ್ತದೆ) - ವೈಯಕ್ತಿಕ ತೈಲ ಉತ್ಪನ್ನಗಳು.
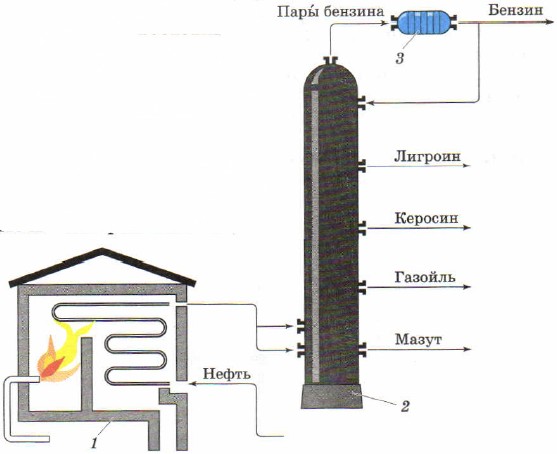
ಅಕ್ಕಿ. 85.
ನಿರಂತರ ತೈಲ ಬಟ್ಟಿ ಇಳಿಸುವಿಕೆಗಾಗಿ ಕೊಳವೆಯಾಕಾರದ ಅನುಸ್ಥಾಪನೆಯ ರೇಖಾಚಿತ್ರ:
1 - ಕೊಳವೆಯಾಕಾರದ ಕುಲುಮೆ; 2 - ಬಟ್ಟಿ ಇಳಿಸುವಿಕೆಯ ಕಾಲಮ್; 3 - ರೆಫ್ರಿಜರೇಟರ್
ಸುರುಳಿಯಾಕಾರದ ಕೊಳವೆ ಕುಲುಮೆಯಲ್ಲಿ ಉದ್ದವಾದ ಪೈಪ್ಲೈನ್ ಇದೆ. ಇಂಧನ ತೈಲ ಅಥವಾ ಅನಿಲವನ್ನು ಸುಡುವ ಮೂಲಕ ಒಲೆ ಬಿಸಿಮಾಡಲಾಗುತ್ತದೆ. ತೈಲವನ್ನು ಪೈಪ್ಲೈನ್ ಮೂಲಕ ನಿರಂತರವಾಗಿ ಸರಬರಾಜು ಮಾಡಲಾಗುತ್ತದೆ, ಅಲ್ಲಿ ಅದನ್ನು 320-350 ° C ಗೆ ಬಿಸಿಮಾಡಲಾಗುತ್ತದೆ ಮತ್ತು ದ್ರವ ಮತ್ತು ಆವಿಯ ಮಿಶ್ರಣದ ರೂಪದಲ್ಲಿ ಬಟ್ಟಿ ಇಳಿಸುವಿಕೆಯ ಕಾಲಮ್ಗೆ ಪ್ರವೇಶಿಸುತ್ತದೆ.
ಬಟ್ಟಿ ಇಳಿಸುವಿಕೆಯ ಕಾಲಮ್ ಸುಮಾರು 40 ಮೀ ಎತ್ತರದ ಉಕ್ಕಿನ ಸಿಲಿಂಡರಾಕಾರದ ಉಪಕರಣವಾಗಿದೆ.ಇದು ರಂಧ್ರಗಳಿರುವ ಹಲವಾರು ಡಜನ್ ಸಮತಲ ವಿಭಾಗಗಳನ್ನು ಹೊಂದಿದೆ, ಇದನ್ನು ಪ್ಲೇಟ್ಗಳು ಎಂದು ಕರೆಯಲಾಗುತ್ತದೆ. ಕಾಲಮ್ಗೆ ಪ್ರವೇಶಿಸುವ ತೈಲ ಆವಿಯು ಮೇಲಕ್ಕೆ ಏರುತ್ತದೆ ಮತ್ತು ಫಲಕಗಳಲ್ಲಿನ ರಂಧ್ರಗಳ ಮೂಲಕ ಹಾದುಹೋಗುತ್ತದೆ. ಅವು ಮೇಲಕ್ಕೆ ಚಲಿಸುವಾಗ ಕ್ರಮೇಣ ತಣ್ಣಗಾಗುತ್ತವೆ, ಅವುಗಳು ತಮ್ಮ ಕುದಿಯುವ ಬಿಂದು ಮತ್ತು ಸಾಂದ್ರತೆಯನ್ನು ಅವಲಂಬಿಸಿ ಕೆಲವು ಫಲಕಗಳ ಮೇಲೆ ದ್ರವವಾಗುತ್ತವೆ. ಹೈಡ್ರೋಕಾರ್ಬನ್ಗಳು ಕಡಿಮೆ ಬಾಷ್ಪಶೀಲವಾಗಿರುತ್ತವೆ ಮತ್ತು ಮೊದಲ ಪ್ಲೇಟ್ಗಳಲ್ಲಿ ಈಗಾಗಲೇ ದ್ರವೀಕರಿಸಲ್ಪಟ್ಟಿವೆ, ಅನಿಲ ತೈಲ ಭಾಗವನ್ನು ರೂಪಿಸುತ್ತವೆ, ಹೆಚ್ಚು ಬಾಷ್ಪಶೀಲ ಹೈಡ್ರೋಕಾರ್ಬನ್ಗಳು ಹೆಚ್ಚಿನ ಪ್ರಮಾಣದಲ್ಲಿ ಸಂಗ್ರಹಿಸಲ್ಪಡುತ್ತವೆ ಮತ್ತು ಸೀಮೆಎಣ್ಣೆ ಭಾಗವನ್ನು ರೂಪಿಸುತ್ತವೆ, ನಾಫ್ತಾ ಭಾಗವನ್ನು ಇನ್ನೂ ಹೆಚ್ಚಿನ ಪ್ರಮಾಣದಲ್ಲಿ ಸಂಗ್ರಹಿಸಲಾಗುತ್ತದೆ, ಹೆಚ್ಚು ಬಾಷ್ಪಶೀಲ ಹೈಡ್ರೋಕಾರ್ಬನ್ಗಳು ಕಾಲಮ್ ಅನ್ನು ಈ ರೂಪದಲ್ಲಿ ಬಿಡುತ್ತವೆ ಆವಿಗಳು ಮತ್ತು ರೂಪ ಗ್ಯಾಸೋಲಿನ್. ದಪ್ಪ ಕಪ್ಪು ದ್ರವವು ಕೆಳಗೆ ಸಂಗ್ರಹಿಸುತ್ತದೆ - ಇಂಧನ ತೈಲ. ಇದನ್ನು ಇಂಧನವಾಗಿ ಬಳಸಲಾಗುತ್ತದೆ, ಜೊತೆಗೆ ಹೆಚ್ಚುವರಿ ಬಟ್ಟಿ ಇಳಿಸುವಿಕೆಯ ಮೂಲಕ ನಯಗೊಳಿಸುವ ತೈಲಗಳನ್ನು ಪಡೆಯಲು ಬಳಸಲಾಗುತ್ತದೆ.
ಬಟ್ಟಿ ಇಳಿಸುವ ವಿಧಾನ ದ್ರವ ಗಾಳಿಅದರಿಂದ ವೈಯಕ್ತಿಕವಾಗಿ ಪಡೆಯುವ ಆಧಾರದ ಮೇಲೆ ಇರುತ್ತದೆ ಘಟಕಗಳು- ಸಾರಜನಕ (ಇದು ಮೊದಲು ಕುದಿಯುತ್ತದೆ), ಆಮ್ಲಜನಕ, ಇತ್ಯಾದಿ.

ಅಕ್ಕಿ. 86.
ಶೋಧನೆ
ಲವಣಗಳನ್ನು ಶುದ್ಧೀಕರಿಸಲು, ಸ್ಫಟಿಕೀಕರಣ ವಿಧಾನವನ್ನು ಬಳಸಲಾಗುತ್ತದೆ. ಈ ಸಂದರ್ಭದಲ್ಲಿ, ಉದಾಹರಣೆಗೆ, ನೈಸರ್ಗಿಕ ಉಪ್ಪನ್ನು ನೀರಿನಲ್ಲಿ ಕರಗಿಸಲಾಗುತ್ತದೆ ಮತ್ತು ನಂತರ ಫಿಲ್ಟರ್ ಮಾಡಲಾಗುತ್ತದೆ (ಚಿತ್ರ 86). ಪರಿಣಾಮವಾಗಿ ಮರಳು, ಜೇಡಿಮಣ್ಣು ಮತ್ತು ನೀರಿನಲ್ಲಿ ಕರಗದ ಇತರ ಕಲ್ಮಶಗಳಿಂದ ಶುದ್ಧೀಕರಿಸಿದ ಟೇಬಲ್ ಉಪ್ಪಿನ ಪರಿಹಾರವಾಗಿದೆ. ನಂತರ ಉಪ್ಪನ್ನು ಆವಿಯಾಗುವಿಕೆಯಿಂದ ದ್ರಾವಣದಿಂದ ಬೇರ್ಪಡಿಸಲಾಗುತ್ತದೆ (ಚಿತ್ರ 87), ನೀರು ಆವಿಯಾಗುತ್ತದೆ ಮತ್ತು ಉಪ್ಪು ಹರಳುಗಳು ಪಿಂಗಾಣಿ ಕಪ್ನಲ್ಲಿ ಉಳಿಯುತ್ತವೆ.
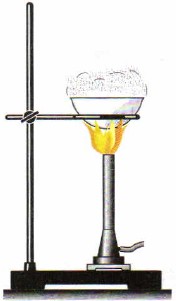
ಅಕ್ಕಿ. 87.
ಆವಿಯಾಗುವಿಕೆ
ಫಿಲ್ಟರಿಂಗ್ ವಿಧಾನವು ವಿಭಿನ್ನತೆಯನ್ನು ಆಧರಿಸಿದೆ ಬ್ಯಾಂಡ್ವಿಡ್ತ್ಸರಂಧ್ರ ವಸ್ತು - ಮಿಶ್ರಣವನ್ನು ರೂಪಿಸುವ ಕಣಗಳಿಗೆ ಸಂಬಂಧಿಸಿದಂತೆ ಫಿಲ್ಟರ್. ಸ್ವಚ್ಛಗೊಳಿಸಲು ಫಿಲ್ಟರ್ ಕುಡಿಯುವ ನೀರುನೀರಿನ ಸಂಸ್ಕರಣಾ ಘಟಕಗಳಲ್ಲಿ ಮರಳಿನ ಪದರವಿದೆ. ಅದರಲ್ಲಿ ಅಮಾನತುಗೊಳಿಸಿದ ಧೂಳಿನಿಂದ ಗಾಳಿಯನ್ನು ಸ್ವಚ್ಛಗೊಳಿಸುವ ನಿರ್ವಾಯು ಮಾರ್ಜಕದಲ್ಲಿ, ಕಾಗದ ಅಥವಾ ಫ್ಯಾಬ್ರಿಕ್ ಫಿಲ್ಟರ್ಗಳನ್ನು ಬಳಸಲಾಗುತ್ತದೆ; ಔಷಧದಲ್ಲಿ, ರೋಗಿಗಳಿಗೆ ಆರೈಕೆ ಮಾಡುವಾಗ ಅಥವಾ ಶಸ್ತ್ರಚಿಕಿತ್ಸೆಯ ಸಮಯದಲ್ಲಿ, ಬಹುಪದರದ ಗಾಜ್ ಡ್ರೆಸ್ಸಿಂಗ್ ಅನ್ನು ಫಿಲ್ಟರ್ ಆಗಿ ಬಳಸಲಾಗುತ್ತದೆ.
ಶುದ್ಧ ಅಯೋಡಿನ್ ಮತ್ತು ಗಂಧಕವನ್ನು ಪಡೆಯಲು, ಉತ್ಪತನದಂತಹ ಭೌತಿಕ ವಿದ್ಯಮಾನವನ್ನು ಬಳಸಲಾಗುತ್ತದೆ, ಅಂದರೆ, ವಸ್ತುವಿನ ಪರಿವರ್ತನೆ ಘನ ಸ್ಥಿತಿಅನಿಲ ರೂಪಕ್ಕೆ, ದ್ರವ ಹಂತವನ್ನು ಬೈಪಾಸ್ ಮಾಡುವುದು (ಚಿತ್ರ 88). ಉತ್ಪತನದ ಸಮಯದಲ್ಲಿ, ಸ್ಫಟಿಕದಂತಹ ವಸ್ತುವು ಸಾಧನದ ಬಿಸಿಯಾದ ಭಾಗದಲ್ಲಿ ಆವಿಯಾಗುತ್ತದೆ ಮತ್ತು ತಂಪಾಗುವ ಭಾಗದಲ್ಲಿ ಅದು ಸ್ಫಟಿಕಗಳನ್ನು ರೂಪಿಸಲು ಮತ್ತೆ ಘನೀಕರಿಸುತ್ತದೆ. ಮಂಜುಗಡ್ಡೆಯು ಉತ್ಪತನಕ್ಕೆ ಸಮರ್ಥವಾಗಿದೆ; ಒದ್ದೆಯಾದ ಲಾಂಡ್ರಿ ಶೀತದಲ್ಲಿಯೂ ಒಣಗುವುದು ಯಾವುದಕ್ಕೂ ಅಲ್ಲ.
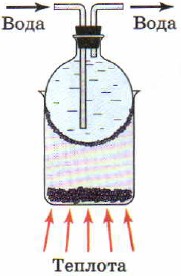
ಅಕ್ಕಿ. 88.
ಅಯೋಡಿನ್ ಉತ್ಪತನ
ಉತ್ಪತನವು ಘನದ ಬಳಕೆಯನ್ನು ನಿರ್ಧರಿಸುತ್ತದೆ ಇಂಗಾಲದ ಡೈಆಕ್ಸೈಡ್ CO 2 (ನಿಮಗೆ ತಿಳಿದಿರುವಂತೆ, ಇದನ್ನು ಡ್ರೈ ಐಸ್ ಎಂದು ಕರೆಯಲಾಗುತ್ತದೆ) ಆಹಾರವನ್ನು ಸಂಗ್ರಹಿಸಲು, ವಿಶೇಷವಾಗಿ ಐಸ್ ಕ್ರೀಮ್.

ಅಕ್ಕಿ. 89.
ತೈಲ ಬೇರ್ಪಡಿಕೆ ಕಾಲಮ್
ಪದಾರ್ಥಗಳ ವಿಭಿನ್ನ ಸಾಂದ್ರತೆಗಳು ನೆಲೆಗೊಳ್ಳುವಂತಹ ಮಿಶ್ರಣಗಳನ್ನು ಬೇರ್ಪಡಿಸುವ ಈ ವಿಧಾನದ ಆಧಾರವಾಗಿದೆ. ಉದಾಹರಣೆಗೆ, ತೈಲ ಮತ್ತು ನೀರಿನ ಮಿಶ್ರಣಗಳು, ಸಸ್ಯಜನ್ಯ ಎಣ್ಣೆಮತ್ತು ನೀರು ತ್ವರಿತವಾಗಿ ಬೇರ್ಪಡುತ್ತದೆ ಮತ್ತು ಆದ್ದರಿಂದ ಬೇರ್ಪಡಿಸುವ ಕೊಳವೆಯನ್ನು ಬಳಸಿಕೊಂಡು ಪರಸ್ಪರ ಬೇರ್ಪಡಿಸಲು ಸುಲಭವಾಗಿದೆ (ಚಿತ್ರ 89, 90).

ಅಕ್ಕಿ. 90.
ಬೇರ್ಪಡಿಸುವ ಕೊಳವೆ
ನೆಲೆಗೊಳ್ಳುವ ಬದಲು ಮಿಶ್ರಣಗಳನ್ನು ಬೇರ್ಪಡಿಸುವ ಪ್ರಕ್ರಿಯೆಯನ್ನು ವೇಗಗೊಳಿಸಲು ಪ್ರಯೋಗಾಲಯ ಅಭ್ಯಾಸಕೇಂದ್ರಾಪಗಾಮಿಯನ್ನು ಹೆಚ್ಚಾಗಿ ಬಳಸಲಾಗುತ್ತದೆ, ಇದು ವಿಶೇಷ ಸಾಧನದ ಕಾರಣದಿಂದಾಗಿ ಈ ಹೆಸರನ್ನು ಪಡೆದುಕೊಂಡಿದೆ - ಕೇಂದ್ರಾಪಗಾಮಿ. ಪದಾರ್ಥಗಳ ಮಿಶ್ರಣವನ್ನು ಹೊಂದಿರುವ ಪರೀಕ್ಷಾ ಕೊಳವೆಗಳನ್ನು ಕೇಂದ್ರಾಪಗಾಮಿಯಲ್ಲಿ ಇರಿಸಲಾಗುತ್ತದೆ. ಅವರು ಸಾಧನವನ್ನು ಆನ್ ಮಾಡುತ್ತಾರೆ, ಅದು ಏರಿಳಿಕೆಯಂತೆ ಪ್ರಾರಂಭವಾಗುತ್ತದೆ, ಅದರಲ್ಲಿ ಸ್ಥಿರವಾಗಿರುವ ಪರೀಕ್ಷಾ ಟ್ಯೂಬ್ಗಳನ್ನು ತೀವ್ರವಾಗಿ ತಿರುಗಿಸಲು. ಕಣದ ಕೇಂದ್ರಾಪಗಾಮಿ ಬಲದ ಪ್ರಭಾವದ ಅಡಿಯಲ್ಲಿ ವಿವಿಧ ಪದಾರ್ಥಗಳುವಿಭಿನ್ನ ವೇಗವರ್ಧನೆಗಳನ್ನು ಪಡೆಯುತ್ತವೆ, ಏಕೆಂದರೆ ಅವುಗಳು ಹೊಂದಿವೆ ವಿಭಿನ್ನ ಸಾಂದ್ರತೆಗಳು, ಮತ್ತು ಮಿಶ್ರಣವನ್ನು ಪ್ರತ್ಯೇಕಿಸಲಾಗಿದೆ (ಚಿತ್ರ 91).
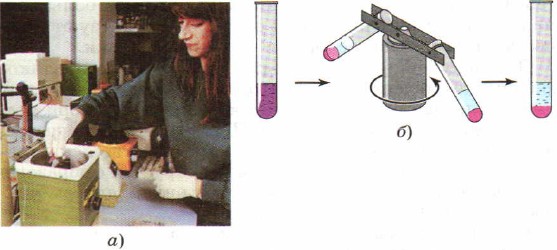
ಅಕ್ಕಿ. 91.
ಕೇಂದ್ರಾಪಗಾಮಿ:
a - ಕೇಂದ್ರಾಪಗಾಮಿ ಛಾಯಾಚಿತ್ರ; ಬಿ - ಕೇಂದ್ರಾಪಗಾಮಿ ಕಾರ್ಯಾಚರಣೆ ರೇಖಾಚಿತ್ರ
ಪ್ರಮುಖ ಪದಗಳು ಮತ್ತು ನುಡಿಗಟ್ಟುಗಳು
- ಬಟ್ಟಿ ಇಳಿಸುವಿಕೆ ಅಥವಾ ಬಟ್ಟಿ ಇಳಿಸುವಿಕೆ.
- ಭಟ್ಟಿ ಇಳಿಸಿದ ನೀರು.
- ಸ್ಫಟಿಕೀಕರಣ ಮತ್ತು ಆವಿಯಾಗುವಿಕೆ.
- ಶೋಧನೆ.
- ಉತ್ಪತನ.
- ವಕಾಲತ್ತು.
- ಬೇರ್ಪಡಿಸುವ ಕೊಳವೆ.
- ಕೇಂದ್ರಾಪಗಾಮಿ.
ಕಂಪ್ಯೂಟರ್ನೊಂದಿಗೆ ಕೆಲಸ ಮಾಡಿ
- ಎಲೆಕ್ಟ್ರಾನಿಕ್ ಅಪ್ಲಿಕೇಶನ್ ಅನ್ನು ನೋಡಿ. ಪಾಠದ ವಿಷಯವನ್ನು ಅಧ್ಯಯನ ಮಾಡಿ ಮತ್ತು ನಿಯೋಜಿಸಲಾದ ಕಾರ್ಯಗಳನ್ನು ಪೂರ್ಣಗೊಳಿಸಿ.
- ಅಂತರ್ಜಾಲದಲ್ಲಿ ಹುಡುಕಿ ಮಿಂಚಂಚೆ ವಿಳಾಸಗಳು, ಇದು ಸೇವೆ ಮಾಡಬಹುದು ಹೆಚ್ಚುವರಿ ಮೂಲಗಳು, ಪ್ಯಾರಾಗ್ರಾಫ್ನಲ್ಲಿ ಕೀವರ್ಡ್ಗಳು ಮತ್ತು ಪದಗುಚ್ಛಗಳ ವಿಷಯವನ್ನು ಬಹಿರಂಗಪಡಿಸುವುದು. ಹೊಸ ಪಾಠವನ್ನು ಸಿದ್ಧಪಡಿಸುವಲ್ಲಿ ಶಿಕ್ಷಕರಿಗೆ ನಿಮ್ಮ ಸಹಾಯವನ್ನು ನೀಡಿ - ಮೂಲಕ ಸಂದೇಶವನ್ನು ಕಳುಹಿಸಿ ಕೀವರ್ಡ್ಗಳುಮತ್ತು ಮುಂದಿನ ಪ್ಯಾರಾಗ್ರಾಫ್ನಲ್ಲಿ ನುಡಿಗಟ್ಟುಗಳು.
ಪ್ರಶ್ನೆಗಳು ಮತ್ತು ಕಾರ್ಯಗಳು
- ಎ. ಬೆಲ್ಯಾವ್ ಅವರ ವೈಜ್ಞಾನಿಕ ಕಾದಂಬರಿ "ದಿ ಏರ್ ಸೆಲ್ಲರ್" ನಲ್ಲಿ ಮಿಶ್ರಣಗಳನ್ನು ಬೇರ್ಪಡಿಸುವ ಯಾವ ವಿಧಾನವನ್ನು ವಿವರಿಸಲಾಗಿದೆ?
- ಚೆಲ್ಲಿದ ಉಪ್ಪು ಜಗಳಕ್ಕೆ ಕಾರಣವಾಗುತ್ತದೆ ಎಂಬ ನಂಬಿಕೆ ಎಲ್ಲಿಂದ ಬರುತ್ತದೆ? ಚೆಲ್ಲಿದ ಉಪ್ಪಿನ ಬಗ್ಗೆ ಜಗಳವಾಡಿದ ಜನರನ್ನು ಹೇಗೆ ಸಮನ್ವಯಗೊಳಿಸುವುದು?
- ಕೆಳಗಿನ ಮಿಶ್ರಣಗಳನ್ನು ಬೇರ್ಪಡಿಸುವ ವಿಧಾನಗಳನ್ನು ಸೂಚಿಸಿ: a) ಹಲ್ಲಿನ ಪುಡಿ ಮತ್ತು ಉಪ್ಪು; ಬಿ) ಮದ್ಯ ಮತ್ತು ನೀರು; ಸಿ) ಗ್ಯಾಸೋಲಿನ್ ಮತ್ತು ನೀರು.
- ಪ್ರಯಾಣ ಮಾಡುವಾಗ ಸ್ವಚ್ಛಗೊಳಿಸಲು ಮತ್ತು ಸೋಂಕುರಹಿತಗೊಳಿಸುವುದು ಹೇಗೆ ನದಿ ನೀರುಮತ್ತು ಅದನ್ನು ಕುಡಿಯಲು ಮತ್ತು ಅಡುಗೆಗೆ ಸೂಕ್ತವಾಗಿಸುವುದೇ?
- ಎಲಿವೇಟರ್ (ಗ್ರಾನರಿ) ಕೆಲಸಗಾರರು ಧಾನ್ಯವನ್ನು ಬೇರ್ಪಡಿಸುವಾಗ ಮತ್ತು ವಿಂಗಡಿಸುವಾಗ ವಿಶೇಷ ಮುಖವಾಡವನ್ನು ಏಕೆ ಧರಿಸುತ್ತಾರೆ?
- ಟೀಪಾಟ್ನಿಂದ ಸ್ಟ್ರೈನರ್ ಮೂಲಕ ಸುರಿಯುವಾಗ ಚಹಾ ಎಲೆಗಳಿಂದ ಚಹಾ ಎಲೆಗಳನ್ನು ತೆರವುಗೊಳಿಸಲು ನೀವು ಯಾವ ವಿಧಾನವನ್ನು ಬಳಸುತ್ತೀರಿ?
ಮುಖ್ಯಸ್ಥ: ಬೋಗರ್ ನಟಾಲಿಯಾ ವ್ಲಾಡಿಮಿರೋವ್ನಾ, ರಸಾಯನಶಾಸ್ತ್ರ ಶಿಕ್ಷಕ
ವಿಷಯ: "ವಿಸರ್ಜನೆ - ಭೌತಿಕ ಅಥವಾ ರಾಸಾಯನಿಕ ಪ್ರಕ್ರಿಯೆ?"
ಶೈಕ್ಷಣಿಕ ಸಂಸ್ಥೆ: MBOU ಕಾರ್ಗಾಸೊಕ್ಸ್ಕಾಯಾ ಮಾಧ್ಯಮಿಕ ಶಾಲೆ ಸಂಖ್ಯೆ 2, ಕಾರ್ಗಾಸೊಕ್ ಗ್ರಾಮ, ಟಾಮ್ಸ್ಕ್ ಪ್ರದೇಶ
ಬಳಸಿದ ಮಾಧ್ಯಮ ಸಂಪನ್ಮೂಲಗಳು: ವರ್ಡ್ ಪಠ್ಯ ಸಂಪಾದಕ, ಇಂಟರ್ನೆಟ್ ಸಂಪನ್ಮೂಲಗಳು
1) ಅಧ್ಯಯನದ ಪ್ರಸ್ತುತತೆ (ಏಕೆ ಈ ವಿಷಯಲೇಖಕರು ಸಂಶೋಧನೆಗಾಗಿ ತೆಗೆದುಕೊಂಡಿದ್ದಾರೆ)
ನಾವು ಈಗ ಎರಡು ವರ್ಷಗಳಿಂದ ಭೌತಶಾಸ್ತ್ರವನ್ನು ಅಧ್ಯಯನ ಮಾಡುತ್ತಿದ್ದೇವೆ, ನಾವು ಈ ವಿಜ್ಞಾನದ ಬಗ್ಗೆ ಉತ್ಸಾಹ ಹೊಂದಿದ್ದೇವೆ, ನಾವು ಮೂಲಭೂತ ಕಾನೂನುಗಳು ಮತ್ತು ಭೌತಿಕ ವಿದ್ಯಮಾನಗಳನ್ನು ಅಧ್ಯಯನ ಮಾಡುತ್ತಿದ್ದೇವೆ. ಮತ್ತು ಸಕ್ಕರೆ, ಉಪ್ಪು ಮತ್ತು ಇತರವನ್ನು ಕರಗಿಸುವ ಪ್ರಕ್ರಿಯೆಯು ನಮಗೆ ಯಾವಾಗಲೂ ಸ್ಪಷ್ಟವಾಗಿದೆ ಕರಗುವ ವಸ್ತುಗಳುನೀರಿನಲ್ಲಿ - ಒಂದು ಭೌತಿಕ ವಿದ್ಯಮಾನ. ಈ ವರ್ಷ ನಾವು ಅಧ್ಯಯನ ಮಾಡಲು ಪ್ರಾರಂಭಿಸಿದ್ದೇವೆ ಹೊಸ ವಿಜ್ಞಾನ- ರಸಾಯನಶಾಸ್ತ್ರ. ಮತ್ತು ವಿಸರ್ಜನೆಯ ಪ್ರಕ್ರಿಯೆಯು ರಾಸಾಯನಿಕ ವಿದ್ಯಮಾನವಾಗಿದೆ ಎಂಬುದು ನಮಗೆ ಆಶ್ಚರ್ಯಕರವಾಗಿತ್ತು. ರಸಾಯನಶಾಸ್ತ್ರವು ವಸ್ತುಗಳು, ಗುಣಲಕ್ಷಣಗಳು ಮತ್ತು ಅವುಗಳ ರೂಪಾಂತರಗಳ ವಿಜ್ಞಾನವಾಗಿದೆ. ಆದರೆ ನೀರಿನಲ್ಲಿ ಸಕ್ಕರೆಯನ್ನು ಕರಗಿಸುವ ಪ್ರಕ್ರಿಯೆಯಲ್ಲಿ, ನಾವು ಆಮ್ಲ, ಕ್ಷಾರ ಅಥವಾ ಇನ್ನಾವುದೇ ವಸ್ತುವನ್ನು ಪಡೆಯಲಿಲ್ಲ. ಸಕ್ಕರೆ ಸಕ್ಕರೆಯಾಗಿಯೇ ಉಳಿದಿದೆ.
2) ಸಂಶೋಧನೆಯ ವಿಷಯದ ವ್ಯಾಖ್ಯಾನ (ಯಾವುದನ್ನು ಅಧ್ಯಯನ ಮಾಡಬೇಕು?)
ಅವರು ಹೇಗೆ ಭಿನ್ನರಾಗಿದ್ದಾರೆ ಎಂಬ ಪ್ರಶ್ನೆಯಲ್ಲಿ ನಾವು ಆಸಕ್ತಿ ಹೊಂದಿದ್ದೇವೆ ದೈಹಿಕ ಬದಲಾವಣೆಗಳುರಾಸಾಯನಿಕಗಳಿಂದ? ಇದು ತುಂಬಾ ಸರಳವಾದ ಪ್ರಶ್ನೆಯಲ್ಲ.
3) ಸಮಸ್ಯೆಯ ಸೂತ್ರೀಕರಣ. ಸಮಸ್ಯೆ ಏನು? ಯಾವ ಪ್ರಶ್ನೆ(ಗಳಿಗೆ) ಉತ್ತರಿಸಬೇಕು?
ನೀರಿನಲ್ಲಿ ವಸ್ತುಗಳನ್ನು ಕರಗಿಸುವ ಪ್ರಕ್ರಿಯೆಯು ಭೌತಿಕ ಅಥವಾ ರಾಸಾಯನಿಕವಾಗಿದೆಯೇ ಎಂದು ಕಂಡುಹಿಡಿಯಿರಿ.
4) ಒಂದು ಊಹೆಯನ್ನು ಪ್ರತಿಪಾದಿಸುವುದು. ಸಂಭವನೀಯ ಉತ್ತರ ಏನಿರಬಹುದು?
ನಾವು ಒಂದು ಊಹೆಯನ್ನು ಮುಂದಿಡುತ್ತೇವೆ : ಭೌತಿಕ ಮತ್ತು ರಾಸಾಯನಿಕ ರೂಪಾಂತರಗಳ ನಡುವಿನ ರೇಖೆಯು ಅನಿಯಂತ್ರಿತ ಮತ್ತು ನಿರಂಕುಶವಾಗಿರುವುದು ಸಾಧ್ಯ.
5) ಕಲ್ಪನೆಯ ಪರೀಕ್ಷೆ.
ಆನ್ ಈ ಹಂತದಲ್ಲಿಕೆಲಸವು ಮೂರು ದಿಕ್ಕುಗಳಲ್ಲಿ ನಡೆಯುತ್ತದೆ:
- ವೈಜ್ಞಾನಿಕ ಸಾಹಿತ್ಯದ ಸೈದ್ಧಾಂತಿಕ ವಿಶ್ಲೇಷಣೆ;
- ಭೌತಿಕ ಮತ್ತು ರಾಸಾಯನಿಕ ಪ್ರಯೋಗ;
- ಪ್ರಾಯೋಗಿಕ ಡೇಟಾದ ವಿಶ್ಲೇಷಣೆ.
ಮೊದಲ ದಿಕ್ಕಿನಲ್ಲಿ ಕೆಲಸವು ಪರಿಗಣಿಸಲು ಸಾಧ್ಯವಾಯಿತು ಸೈದ್ಧಾಂತಿಕ ಸಮಸ್ಯೆಗಳುನೀರಿನಲ್ಲಿ ವಸ್ತುಗಳನ್ನು ಕರಗಿಸುವ ಪ್ರಕ್ರಿಯೆ. ವಿಸರ್ಜನೆಯ ಸಮಸ್ಯೆಯು ದೀರ್ಘಕಾಲದವರೆಗೆ ಮನುಷ್ಯನಿಗೆ ಆಸಕ್ತಿಯನ್ನುಂಟುಮಾಡಿದೆ. ರಸವಾದಿಗಳು ಮತ್ತು ನಂತರದ ಶತಮಾನಗಳ ರಸಾಯನಶಾಸ್ತ್ರಜ್ಞರು ವಿಸರ್ಜನೆಯ ಪ್ರಕ್ರಿಯೆಯ ಸಾರವನ್ನು ಬಿಚ್ಚಿಡಲು ಪ್ರಯತ್ನಿಸಿದರು. ಹೀಗಾಗಿ, ಇಂಗ್ಲಿಷ್ ರಸಾಯನಶಾಸ್ತ್ರಜ್ಞ ಆರ್. ಬೋಯ್ಲ್ (1627-1691) ದ್ರಾವಕ ಕಣಗಳು ಸ್ಪೈಕ್ಗಳು, ಕೊಕ್ಕೆಗಳು ಮತ್ತು ಇತರ ಸಾಧನಗಳನ್ನು ಹೊಂದಿರುತ್ತವೆ, ಅದರ ಸಹಾಯದಿಂದ ಅವು ಕರಗಿದ ವಸ್ತುವಿನ ಕಣಗಳಿಗೆ ಅಂಟಿಕೊಳ್ಳುತ್ತವೆ, ಅದಕ್ಕಾಗಿಯೇ ವಿಸರ್ಜನೆ ಸಂಭವಿಸುತ್ತದೆ.
ಅವರು M.V ಯ ವಿಸರ್ಜನೆಯ ಬಗ್ಗೆ ಹೆಚ್ಚು ವೈಜ್ಞಾನಿಕ ಅಭಿಪ್ರಾಯವನ್ನು ವ್ಯಕ್ತಪಡಿಸಿದರು. ಲೋಮೊನೊಸೊವ್ (1711-1765): "ಲವಣ ಕಣಗಳು ನೀರಿನ ಕಣಗಳ ಕ್ರಿಯೆಯಿಂದ ಪರಸ್ಪರ ಬೇರ್ಪಡಿಸಲ್ಪಟ್ಟಿವೆ ..." ಮತ್ತು, ನೀರಿನ ಕಣಗಳಿಗೆ ಅಂಟಿಕೊಂಡಿರುತ್ತವೆ, ಒಟ್ಟಿಗೆ ಅವು ಮುಂದೆ ಚಲಿಸಲು ಪ್ರಾರಂಭಿಸುತ್ತವೆ ಮತ್ತು ದ್ರಾವಕದ ಉದ್ದಕ್ಕೂ ಹರಡುತ್ತವೆ."
19 ನೇ ಶತಮಾನದಲ್ಲಿ, ಪರಿಹಾರಗಳ ಸಂಶೋಧನೆಯನ್ನು ಡಿ.ಐ. ಮೆಂಡಲೀವ್ (1834-1907). ದೊಡ್ಡ ಪ್ರಾಮುಖ್ಯತೆವಿಸರ್ಜನೆಯ ಸಮಯದಲ್ಲಿ ಉಷ್ಣ ಪರಿಣಾಮಗಳ ಅಧ್ಯಯನಕ್ಕೆ ಅವರು ಪ್ರಾಮುಖ್ಯತೆಯನ್ನು ನೀಡಿದರು. ಕೆಲವು ವಸ್ತುಗಳು ಕರಗಿದಾಗ, ಶಾಖ ಬಿಡುಗಡೆಯಾಗುತ್ತದೆ, ಆದರೆ ಇತರರು ಹೀರಿಕೊಳ್ಳುತ್ತಾರೆ ಎಂದು ತಿಳಿದಿದೆ.
ಸ್ವೀಡಿಷ್ ವಿಜ್ಞಾನಿ ಸ್ವಾಂಟೆ ಅರ್ಹೆನಿಯಸ್ (1859-1927) ಅವರ ಕೃತಿಗಳಲ್ಲಿ ಕರಗುವಿಕೆಯ ಸಿದ್ಧಾಂತವನ್ನು ಅಭಿವೃದ್ಧಿಪಡಿಸಲಾಯಿತು. ದ್ರಾವಣದಲ್ಲಿರುವ ವಸ್ತುವು ಅಯಾನುಗಳಾಗಿ ಒಡೆಯುತ್ತದೆ ಎಂದು ಅವರು ಸೂಚಿಸಿದರು. ತರುವಾಯ, ರಷ್ಯಾದ ವಿಜ್ಞಾನಿ I.A. ಕಬ್ಲುಕೋವ್ (1857-1942) S. ಅರ್ಹೆನಿಯಸ್ನ ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯ ವಿಘಟನೆಯ ಸಿದ್ಧಾಂತವನ್ನು D.I ನ ಹೈಡ್ರೇಟ್ ಸಿದ್ಧಾಂತದೊಂದಿಗೆ ಸಂಯೋಜಿಸಿದರು. ಮೆಂಡಲೀವ್. ದ್ರಾವಣದಲ್ಲಿ ರೂಪುಗೊಂಡ ಅಯಾನುಗಳ ಜಲಸಂಚಯನ (ನೀರಿನೊಂದಿಗೆ ಸಂವಹನ) ಊಹೆಯನ್ನು ಅವರು ಮುಂದಿಟ್ಟರು, ಇದು ಪ್ರಾಯೋಗಿಕವಾಗಿ ಸಾಬೀತಾಗಿದೆ.
ವ್ಯಾಂಟ್ ಹಾಫ್, ಅರ್ಹೆನಿಯಸ್ ಮತ್ತು ಓಸ್ವಾಲ್ಡ್ ಅಭಿವೃದ್ಧಿಪಡಿಸಿದ ಪರಿಹಾರಗಳ ಭೌತಿಕ ಸಿದ್ಧಾಂತದ ಪ್ರತಿಪಾದಕರು, ವಿಸರ್ಜನೆಯ ಪ್ರಕ್ರಿಯೆಯು ಪ್ರಸರಣದ ಪರಿಣಾಮವಾಗಿದೆ ಎಂದು ನಂಬಿದ್ದರು, ಅಂದರೆ. ನೀರಿನ ಅಣುಗಳ ನಡುವಿನ ಜಾಗಕ್ಕೆ ದ್ರಾವಕದ ನುಗ್ಗುವಿಕೆ, ಅಂದರೆ. ಭೌತಿಕ ವಿದ್ಯಮಾನ.
ಪರಿಹಾರಗಳ ರಾಸಾಯನಿಕ ಸಿದ್ಧಾಂತದ ಬೆಂಬಲಿಗರು, ಇದನ್ನು ಡಿ.ಐ. ಮೆಂಡಲೀವ್, I.A. ಕಬ್ಲುಕೋವ್, ವಿ.ಎ. ಕಿಸ್ಟ್ಯಾಕೋವ್ಸ್ಕಿ, ವಿಸರ್ಜನೆಯ ಪ್ರಕ್ರಿಯೆಯು ಕರಗಿದ ವಸ್ತು ಮತ್ತು ನೀರಿನ ನಡುವಿನ ರಾಸಾಯನಿಕ ಪರಸ್ಪರ ಕ್ರಿಯೆಯಾಗಿದೆ ಎಂದು ನಂಬಿದ್ದರು.
ಸೈದ್ಧಾಂತಿಕ ಸಮಸ್ಯೆಗಳನ್ನು ಪರಿಗಣಿಸಿದ ನಂತರ, ನಾವು ನಮ್ಮ ಕೆಲಸದ ಪ್ರಾಯೋಗಿಕ ಭಾಗವನ್ನು ಪ್ರಾರಂಭಿಸಿದ್ದೇವೆ.
ಪ್ರಯೋಗ ನಡೆಸೋಣ, ಗುರಿ ಯಾವಾಗ ಎಂಬುದನ್ನು ಪ್ರದರ್ಶಿಸಲುವಿಸರ್ಜನೆಯ ಪ್ರಕ್ರಿಯೆಯು ಸಂಭವಿಸುತ್ತದೆ ಏಕರೂಪದ ವಿತರಣೆಒಂದು ವಸ್ತುವು ಇನ್ನೊಂದರಲ್ಲಿ, ಇದರಲ್ಲಿ ದ್ರಾವಕವು ದ್ರಾವಕದ ಒಟ್ಟು ಸ್ಥಿತಿಗೆ ಹಾದುಹೋಗುತ್ತದೆ, ಅಂದರೆ. ಒಂದು ಭೌತಿಕ ವಿದ್ಯಮಾನವು ಸಂಭವಿಸುತ್ತದೆ.
ಅನುಭವ ಸಂಖ್ಯೆ 1. ಪೊಟ್ಯಾಸಿಯಮ್ ಪರ್ಮಾಂಗನೇಟ್ನ ಉದಾಹರಣೆಯನ್ನು ಬಳಸಿಕೊಂಡು ಪ್ರಸರಣದ ವಿದ್ಯಮಾನ
ನೀರನ್ನು ಹೊಂದಿರುವ ಬೀಕರ್ನಲ್ಲಿ ನಾವು ಪೊಟ್ಯಾಸಿಯಮ್ ಪರ್ಮಾಂಗನೇಟ್ನ ಹಲವಾರು ಗ್ರ್ಯಾನ್ಯೂಲ್ಗಳನ್ನು ಹಾಕಿದರೆ, ಅದರ ಪ್ರಮಾಣ ಹೇಗೆ ಎಂಬುದನ್ನು ನಾವು ಗಮನಿಸಬಹುದು. ಘನಕ್ರಮೇಣ ಕಡಿಮೆಯಾಗುತ್ತದೆ. ಅದೇ ಸಮಯದಲ್ಲಿ, ಸ್ಫಟಿಕಗಳನ್ನು ಸೇರಿಸಿದ ನೀರು ಹೊಸ ಗುಣಗಳನ್ನು ಪಡೆಯುತ್ತದೆ. ಕಡುಗೆಂಪು ಬಣ್ಣ ಕಾಣಿಸಿಕೊಳ್ಳುತ್ತದೆ.
ತೀರ್ಮಾನ : ನಾವು ಪ್ರಸರಣದ ಪ್ರಕ್ರಿಯೆಯನ್ನು ಗಮನಿಸುತ್ತಿದ್ದೇವೆ – ಇದು ಒಂದು ವಸ್ತುವಿನ ಅಣುಗಳು ಇನ್ನೊಂದರ ಅಣುಗಳ ನಡುವಿನ ಅಂತರಕ್ಕೆ ಸ್ವಾಭಾವಿಕವಾಗಿ ಪರಸ್ಪರ ನುಗ್ಗುವಿಕೆಯಾಗಿದೆ. ಒಂದು ಮತ್ತು ಇನ್ನೊಂದು ವಸ್ತುವಿನ ಅಣುಗಳು ಪರಸ್ಪರ ಪರಸ್ಪರ ಭೇದಿಸುವುದರಿಂದ ಇದು ಸಂಭವಿಸುತ್ತದೆ.
ಅನುಭವ ಸಂಖ್ಯೆ 2. ಪ್ರಸರಣ ಪ್ರಕ್ರಿಯೆಯ ಮೇಲೆ ತಾಪಮಾನದ ಪರಿಣಾಮ
ಕೆಲವು ವಸ್ತುಗಳ ಪ್ರಸರಣದ ದರವು ತಾಪಮಾನದಲ್ಲಿನ ಬದಲಾವಣೆಗಳಿಂದ ಪ್ರಭಾವಿತವಾಗಿರುತ್ತದೆ ಎಂದು ಅದು ತಿರುಗುತ್ತದೆ. ಇದನ್ನು ಖಚಿತಪಡಿಸಿಕೊಳ್ಳಲು, ನಾವು ಎರಡು ಗ್ಲಾಸ್ಗಳನ್ನು ತೆಗೆದುಕೊಂಡಿದ್ದೇವೆ, ಒಂದು ಬಿಸಿ ಮತ್ತು ಇನ್ನೊಂದು ಜೊತೆ ತಣ್ಣೀರು. ಸಮಾನ ಪ್ರಮಾಣದ ಪೊಟ್ಯಾಸಿಯಮ್ ಪರ್ಮಾಂಗನೇಟ್ ಅನ್ನು ಸುರಿಯಲಾಗುತ್ತದೆ. ಒಂದು ಕನ್ನಡಕದಲ್ಲಿ, ಪ್ರಸರಣವು ಹೆಚ್ಚು ವೇಗವಾಗಿ ಹೋಗುತ್ತದೆ. ನಮಗೆ ಹೇಳುವಂತೆ ಜೀವನದ ಅನುಭವ, ಪ್ರಸರಣವು ವೇಗವಾಗಿ ಹರಡುವ ವಸ್ತುಗಳ ಹೆಚ್ಚಿನ ತಾಪಮಾನ ಸಂಭವಿಸುತ್ತದೆ.
ತೀರ್ಮಾನ: ವಸ್ತುಗಳ ಹೆಚ್ಚಿನ ತಾಪಮಾನ, ವೇಗವಾಗಿ ಪ್ರಸರಣ ಸಂಭವಿಸುತ್ತದೆ.
ದ್ರಾವಕದೊಂದಿಗೆ ವಸ್ತುವಿನ ರಾಸಾಯನಿಕ ಪರಸ್ಪರ ಕ್ರಿಯೆಯನ್ನು ಕೆಲವು ಚಿಹ್ನೆಗಳಿಂದ ನಿರ್ಣಯಿಸಲಾಗುತ್ತದೆ. ಚಿಹ್ನೆಗಳನ್ನು ಪಟ್ಟಿ ಮಾಡೋಣ ರಾಸಾಯನಿಕ ಪ್ರತಿಕ್ರಿಯೆಗಳು:
- ಬಣ್ಣ ಬದಲಾವಣೆ;
- ವಾಸನೆಯ ನೋಟ;
- ಕೆಸರು ರಚನೆ ಮತ್ತು ವಿಸರ್ಜನೆ;
- ಅನಿಲ ಬಿಡುಗಡೆ;
- ಶಾಖದ ಬಿಡುಗಡೆ ಅಥವಾ ಹೀರಿಕೊಳ್ಳುವಿಕೆ.
ಪ್ರಯೋಗ ನಡೆಸೋಣ, ಗುರಿ ಪರಿಹಾರಗಳು ರೂಪುಗೊಂಡಾಗ, ಶಾಖವನ್ನು ಬಿಡುಗಡೆ ಮಾಡಬಹುದು ಎಂದು ಇದು ತೋರಿಸುತ್ತದೆ.
ಅನುಭವ ಸಂಖ್ಯೆ 3. ಆಮ್ಲ ನೀರಿನಲ್ಲಿ ಕರಗಿದಾಗ ಶಾಖ ಬಿಡುಗಡೆ.
ಈ ಪ್ರಯೋಗಕ್ಕಾಗಿ ನಾವು ಈ ಕೆಳಗಿನ ಸಾಧನಗಳನ್ನು ತೆಗೆದುಕೊಂಡಿದ್ದೇವೆ: ಸಲ್ಫ್ಯೂರಿಕ್ ಆಮ್ಲ(98%), ನೀರು, ತಾಪಮಾನ ಸಂವೇದಕ, 100 ಮಿಲಿ ಬೀಕರ್. ಪ್ರಯೋಗದ ಸಮಯದಲ್ಲಿ, ಸಲ್ಫ್ಯೂರಿಕ್ ಆಮ್ಲದ ಸಣ್ಣ ಪ್ರಮಾಣದ (5 ಮಿಲಿ) 1 ಮಿಲಿ ಭಾಗಗಳಲ್ಲಿ ನೀರಿನಲ್ಲಿ ಕರಗಿದಾಗ, ತಾಪಮಾನದಲ್ಲಿ ಗಮನಾರ್ಹ ಏರಿಕೆ ಕಂಡುಬಂದಿದೆ.
ರಾಸಾಯನಿಕ ಕ್ರಿಯೆಯ ಪ್ರಕ್ರಿಯೆ:
ತೀರ್ಮಾನ: ಸಲ್ಫ್ಯೂರಿಕ್ ಆಮ್ಲವನ್ನು ನೀರಿನಲ್ಲಿ ಕರಗಿಸಿದಾಗ, ತಾಪಮಾನದಲ್ಲಿ ಗಮನಾರ್ಹ ಹೆಚ್ಚಳವನ್ನು ನಾವು ಗಮನಿಸಿದ್ದೇವೆ ಮತ್ತು ಇದು ರಾಸಾಯನಿಕ ಕ್ರಿಯೆಯ ಸಂಕೇತವಾಗಿದೆ.
ಪ್ರಯೋಗ ಸಂಖ್ಯೆ 4. ಉಪ್ಪು ನೀರಿನಲ್ಲಿ ಕರಗಿದಾಗ ಶಾಖದ ಹೀರಿಕೊಳ್ಳುವಿಕೆ.
ಉದ್ದೇಶ: ದ್ರಾವಣಗಳ ರಚನೆಯ ಸಮಯದಲ್ಲಿ ಶಾಖವನ್ನು ಹೀರಿಕೊಳ್ಳಬಹುದು ಎಂದು ಪ್ರದರ್ಶಿಸಲು.
ರಾಸಾಯನಿಕ ಕ್ರಿಯೆ:
ಪ್ರಯೋಗಕ್ಕಾಗಿ, ನಾವು 5 ಗ್ರಾಂ ಪೊಟ್ಯಾಸಿಯಮ್ ನೈಟ್ರೇಟ್ ಅನ್ನು ತೆಗೆದುಕೊಂಡು ಅದನ್ನು 10 ಮಿಲಿ ನೀರಿನಲ್ಲಿ ಕರಗಿಸಿ.
ತೀರ್ಮಾನ : ಪೊಟ್ಯಾಸಿಯಮ್ ನೈಟ್ರೇಟ್ ನೀರಿನಲ್ಲಿ ಕರಗಿದಾಗ ತಾಪಮಾನದಲ್ಲಿನ ಇಳಿಕೆಯನ್ನು ನಾವು ಗಮನಿಸಿದ್ದೇವೆ ಮತ್ತು ಇದು ರಾಸಾಯನಿಕ ಪರಸ್ಪರ ಕ್ರಿಯೆಯ ಸಂಕೇತವಾಗಿದೆ.
ವಿಸರ್ಜನೆಯ ಪ್ರಕ್ರಿಯೆಯ ಸಂಕೀರ್ಣತೆಯು ಕೇವಲ ಸಾಕ್ಷಿಯಾಗಿದೆ ಉಷ್ಣ ಪರಿಣಾಮಗಳು, ಆದರೆ ಬಣ್ಣ ಬದಲಾವಣೆಯಂತಹ ರಾಸಾಯನಿಕ ಪ್ರತಿಕ್ರಿಯೆಗಳ ಅಂತಹ ಚಿಹ್ನೆ.
ಅನುಭವ ಸಂಖ್ಯೆ 5 .ಉಪ್ಪು ವಿಸರ್ಜನೆಯ ಸಮಯದಲ್ಲಿ ಬಣ್ಣ ಬದಲಾವಣೆ.
ತಗೆದುಕೊಳ್ಳೋಣ ಬಿಳಿ ಪುಡಿತಾಮ್ರದ ಸಲ್ಫೇಟ್ ಮತ್ತು ಅದನ್ನು ನೀರಿನಲ್ಲಿ ಕರಗಿಸಿ. ಇದು ಪರಿಹಾರವನ್ನು ಸೃಷ್ಟಿಸುತ್ತದೆ ನೀಲಿ ಬಣ್ಣ. ವಿಸರ್ಜನೆಯ ಸಮಯದಲ್ಲಿ ರಾಸಾಯನಿಕ ಪ್ರಕ್ರಿಯೆಯು ಸಂಭವಿಸುತ್ತದೆ ಎಂದು ಇದು ಸಾಬೀತುಪಡಿಸುತ್ತದೆ - ಅಯಾನುಗಳ ಜಲಸಂಚಯನ:
ದ್ರಾವಣವು ಆವಿಯಾದರೆ, ನೀಲಿ ಹರಳುಗಳು ಹೊರಬರುತ್ತವೆ. ಸ್ಫಟಿಕಗಳ ಬಣ್ಣದ ಸಂರಕ್ಷಣೆಯು ದ್ರಾವಣಗಳಿಂದ ಉಪ್ಪಿನ ಸ್ಫಟಿಕೀಕರಣದ ಸಮಯದಲ್ಲಿ, ಹೈಡ್ರೀಕರಿಸಿದ ಅಯಾನುಗಳು ನಾಶವಾಗುವುದಿಲ್ಲ, ಆದರೆ ಸಂರಕ್ಷಿಸಲ್ಪಡುತ್ತವೆ ಎಂದು ಸೂಚಿಸುತ್ತದೆ.
ತೀರ್ಮಾನ: ಸ್ಫಟಿಕ ಲ್ಯಾಟಿಸ್ಗಳು ಹೈಡ್ರೀಕರಿಸಿದ ಅಯಾನುಗಳನ್ನು ಹೊಂದಿರುವ ಪದಾರ್ಥಗಳನ್ನು ಸ್ಫಟಿಕ ಹೈಡ್ರೇಟ್ಗಳು ಎಂದು ಕರೆಯಲಾಗುತ್ತದೆ ಮತ್ತು ಸ್ಫಟಿಕ ಹೈಡ್ರೇಟ್ನಲ್ಲಿ ಒಳಗೊಂಡಿರುವ ನೀರನ್ನು ಸ್ಫಟಿಕೀಕರಣ ನೀರು ಎಂದು ಕರೆಯಲಾಗುತ್ತದೆ.
ಅನುಭವ ಸಂಖ್ಯೆ 6 ಅಯೋಡಿನ್ ವಿಸರ್ಜನೆಯ ಸಮಯದಲ್ಲಿ ಬಣ್ಣ ಬದಲಾವಣೆ.
ಅಯೋಡಿನ್ ಅನ್ನು ವಿವಿಧ ದ್ರಾವಕಗಳಲ್ಲಿ ಕರಗಿಸುವ ಮೂಲಕ ನಾವು ಪ್ರಯೋಗವನ್ನು ನಡೆಸಿದ್ದೇವೆ. ಅಯೋಡಿನ್ ಆವಿಯನ್ನು ಹೊಂದಿರುತ್ತದೆ ನೇರಳೆ. ಅದೇ ಬಣ್ಣವು ಗ್ಯಾಸೋಲಿನ್ನಲ್ಲಿ ಅಯೋಡಿನ್ ದ್ರಾವಣದಲ್ಲಿ ಕಂಡುಬರುತ್ತದೆ. ನೀರಿನಲ್ಲಿ, ಅಯೋಡಿನ್ ದ್ರಾವಣವು ಹಳದಿಯಾಗಿರುತ್ತದೆ, ಬೆಂಜೀನ್ ಅಥವಾ ಆಲ್ಕೋಹಾಲ್ನಲ್ಲಿ ಇದು ಕಂದು ಬಣ್ಣದ್ದಾಗಿದೆ (ಇದು ಪರಿಚಿತ ಅಯೋಡಿನ್ ಟಿಂಚರ್ನ ಬಣ್ಣವಾಗಿದೆ), ಪಾಲಿವಿನೈಲ್ ಆಲ್ಕೋಹಾಲ್ನ ದ್ರಾವಣದಲ್ಲಿ ಅಯೋಡಿನ್ ನೀಲಿ ಬಣ್ಣದ್ದಾಗಿದೆ (ಇದು ಅಯೋಡಿನಾಲ್ ಔಷಧದ ಬಣ್ಣವಾಗಿದೆ). ಮತ್ತು ವಿಭಿನ್ನ ದ್ರಾವಕಗಳಲ್ಲಿ ಬಣ್ಣವು ಬದಲಾಗುವುದಿಲ್ಲ, ಅದು ರಾಸಾಯನಿಕವಾಗಿ ವಿಭಿನ್ನವಾಗಿ ವರ್ತಿಸುತ್ತದೆ.
ತೀರ್ಮಾನ: ದ್ರಾವಕ ಅಣುಗಳು ದ್ರಾವಕ ಅಣುಗಳೊಂದಿಗೆ ಬಂಧವನ್ನು ಹೊಂದಿದ್ದು, ಹೊಸವುಗಳ ರಚನೆಗೆ ಕಾರಣವಾಗುತ್ತದೆ. ರಾಸಾಯನಿಕ ಸಂಯುಕ್ತಗಳು.
6 ) ಫಲಿತಾಂಶಗಳ ವಿವರಣೆ. ಸಂಭವನೀಯ ತೀರ್ಮಾನಗಳು.
ವಿಸರ್ಜನೆಯ ಪ್ರಕ್ರಿಯೆ ಏನೆಂದು ನಾವು ಕಂಡುಕೊಂಡಿದ್ದೇವೆ - ಭೌತಿಕ ಅಥವಾ ರಾಸಾಯನಿಕ. ವಿಸರ್ಜನೆಯ ಪ್ರಕ್ರಿಯೆಯ ಸೈದ್ಧಾಂತಿಕ ಸಮಸ್ಯೆಗಳನ್ನು ನಾವು ಅಧ್ಯಯನ ಮಾಡಿದ್ದೇವೆ. ವಿಸರ್ಜನೆಯ ಸಮಯದಲ್ಲಿ ಭೌತಿಕ ಮತ್ತು ರಾಸಾಯನಿಕ ವಿದ್ಯಮಾನಗಳ ಚಿಹ್ನೆಗಳನ್ನು ನಾವು ಪರಿಶೀಲಿಸಿದ್ದೇವೆ. ಪರಿಗಣಿಸಲಾದ ಎಲ್ಲಾ ಗುಣಲಕ್ಷಣಗಳು ಮತ್ತು ಪ್ರಕ್ರಿಯೆಗಳನ್ನು ಪ್ರಾಯೋಗಿಕವಾಗಿ ದೃಢೀಕರಿಸಲಾಗಿದೆ. ಅಧ್ಯಯನದ ಪರಿಣಾಮವಾಗಿ, ವಿಸರ್ಜನೆಯ ಪ್ರಕ್ರಿಯೆಯು ಭೌತಿಕ ಮತ್ತು ರಾಸಾಯನಿಕ ಪ್ರಕ್ರಿಯೆಯಾಗಿದೆ ಎಂದು ನಾವು ಕಂಡುಕೊಂಡಿದ್ದೇವೆ ಮತ್ತು ಪರಿಹಾರಗಳು ಕರಗಿದ ವಸ್ತುವಿನ ಕಣಗಳು, ದ್ರಾವಕ ಮತ್ತು ಅವುಗಳ ಪರಸ್ಪರ ಕ್ರಿಯೆಯ ಉತ್ಪನ್ನಗಳನ್ನು ಒಳಗೊಂಡಿರುವ ಏಕರೂಪದ (ಏಕರೂಪದ) ವ್ಯವಸ್ಥೆಯಾಗಿದೆ - ಹೈಡ್ರೇಟ್ಗಳು. ನಾವು ಭೌತಿಕ ಮತ್ತು ನಡುವಿನ ರೇಖೆಯನ್ನು ಕಂಡುಕೊಂಡಿದ್ದೇವೆ ರಾಸಾಯನಿಕ ವಿದ್ಯಮಾನಗಳುಹೆಚ್ಚಾಗಿ ಷರತ್ತುಬದ್ಧ. ಇದನ್ನು ವಿಜ್ಞಾನಿಗಳು ಯಾದೃಚ್ಛಿಕವಾಗಿ ನಡೆಸಿದ್ದರು. ವಿಸರ್ಜನೆಯ ಪ್ರಕ್ರಿಯೆಯನ್ನು ಕೆಲವು ರೀತಿಯಲ್ಲಿ ಭೌತಿಕ ಮತ್ತು ಇತರರಲ್ಲಿ ರಾಸಾಯನಿಕ ಎಂದು ವರ್ಗೀಕರಿಸಬಹುದು. ಆದ್ದರಿಂದ, ಅಂತಹ ಪ್ರಕ್ರಿಯೆಗಳನ್ನು ಭೌತ-ರಾಸಾಯನಿಕ ವಿದ್ಯಮಾನಗಳು ಎಂದು ಕರೆಯಲು ಪ್ರಾರಂಭಿಸಿತು.
ಅಧ್ಯಯನದ ಉದ್ದೇಶವನ್ನು ಸಾಧಿಸಲಾಗಿದೆ ಎಂದು ನಿರ್ಣಯಿಸಲು ಸೂತ್ರೀಕರಿಸಿದ ತೀರ್ಮಾನಗಳು ನಮಗೆ ಅವಕಾಶ ಮಾಡಿಕೊಡುತ್ತವೆ. ಆದಾಗ್ಯೂ, ಇದು ನಮ್ಮ ಸಂಶೋಧನೆಯ ಅಂತ್ಯವಲ್ಲ; ಇದು ನಮ್ಮನ್ನು ಎದುರಿಸುತ್ತಿದೆ ಹೊಸ ಕೆಲಸ- ಏಕೆ ಜಲೀಯ ದ್ರಾವಣಗಳುಕೆಲವು ವಸ್ತುಗಳು ವಿದ್ಯುತ್ ಪ್ರವಾಹವನ್ನು ನಡೆಸುತ್ತವೆ, ಈ ವಿದ್ಯಮಾನದ ಕಾರಣವನ್ನು ಕಂಡುಹಿಡಿಯಿರಿ. ಆದರೆ ಅದು ವಿಭಿನ್ನ ಅಧ್ಯಯನವಾಗಲಿದೆ.
- ಪ್ರಸ್ತುತಿಗಾಗಿ ತಯಾರಿ ಸಂಶೋಧನಾ ವಸ್ತು. ವರದಿಯನ್ನು ಬರೆಯುವುದು.
ವರದಿ ಬರೆಯಲು ಅವಕಾಶಗಳನ್ನು ಬಳಸಲಾಯಿತು ಪಠ್ಯ ಸಂಪಾದಕಪದ. ಅಂತಿಮ ವಸ್ತುವನ್ನು ಪವರ್ ಪಾಯಿಂಟ್ ಸಂಪಾದಕದಲ್ಲಿ ಪ್ರಸ್ತುತಿಯ ರೂಪದಲ್ಲಿ ಪ್ರಸ್ತುತಪಡಿಸಲಾಗುತ್ತದೆ.
ಕೆಲಸದ ಪರಿಣಾಮವಾಗಿ, ಈ ಕೆಳಗಿನ ಸಾಹಿತ್ಯವನ್ನು ಬಳಸಲಾಯಿತು:
- ಅಲಿಕ್ಬೆಕೋವ್ ಎಲ್.ಯು. ಮನರಂಜನೆಯ ಕಾರ್ಯಗಳುಮತ್ತು ರಸಾಯನಶಾಸ್ತ್ರದಲ್ಲಿ ಪ್ರಯೋಗಗಳು ಎಂ. ಡ್ರೊಫಾ, 2006.
- ಗೊರೆವ್ ಎಲ್.ಎ. ಮನರಂಜನೆಯ ಪ್ರಯೋಗಗಳುಭೌತಶಾಸ್ತ್ರದಲ್ಲಿ. M. ಶಿಕ್ಷಣ, 1985
- ಮ್ಯಾಗಜೀನ್ "ಸೈನ್ಸ್ ಅಂಡ್ ಲೈಫ್", ನಂ. 5 2004.
- ಕುಜ್ನೆಟ್ಸೊವಾ L.M. ರಸಾಯನಶಾಸ್ತ್ರ 9 ನೇ ತರಗತಿ. M. ಮೆನೆಮೊಸಿನ್, 2003.
- ಓಲ್ಮಾ ಎನ್ಸೈಕ್ಲೋಪೀಡಿಯಾ. ವಸ್ತುವಿನ ರೂಪಾಂತರಗಳು. ರಸಾಯನಶಾಸ್ತ್ರ. M. ಓಲ್ಮಾ ಮೀಡಿಯಾ ಗ್ರೂಪ್, 2013.
- ಇಂಟರ್ನೆಟ್ ಸಂಪನ್ಮೂಲ.
ವಿಸರ್ಜನೆಯು ಒಂದು ವಸ್ತುವಿನ ಮತ್ತೊಂದು ವಸ್ತುವಿನ ಏಕರೂಪದ ವಿತರಣೆಯ ಪ್ರಕ್ರಿಯೆಯಾಗಿದೆ, ಇದರಲ್ಲಿ ದ್ರಾವಕವು ದ್ರಾವಕದ ಒಟ್ಟು ಸ್ಥಿತಿಗೆ ಹಾದುಹೋಗುತ್ತದೆ.
ಪರಿಹಾರವಾಗಿದೆ ರಾಸಾಯನಿಕ ವ್ಯವಸ್ಥೆ, ಹಲವಾರು ಪದಾರ್ಥಗಳಿಂದ ರೂಪುಗೊಂಡಿದೆ, ಅದರ ನಡುವೆ ಯಾವುದೇ ಇಂಟರ್ಫೇಸ್ಗಳಿಲ್ಲ.
ಭೌತಿಕ ಸಿದ್ಧಾಂತಪರಿಹಾರಗಳು:
ವಿಸರ್ಜನೆಯು ಪ್ರಸರಣದ ಪ್ರಕ್ರಿಯೆಯಾಗಿದೆ, ಪರಿಹಾರಗಳು ಏಕರೂಪದ ಮಿಶ್ರಣಗಳು
ರಾಸಾಯನಿಕ ಸಿದ್ಧಾಂತಪರಿಹಾರಗಳು:
ಕರಗುವಿಕೆಯು ನೀರಿನೊಂದಿಗೆ ದ್ರಾವಕದ ರಾಸಾಯನಿಕ ಪರಸ್ಪರ ಕ್ರಿಯೆಯ ಪ್ರಕ್ರಿಯೆಯಾಗಿದೆ - ಜಲಸಂಚಯನ, ದ್ರಾವಣಗಳು - ಸಂಯುಕ್ತಗಳು ಹೈಡ್ರೇಟ್ಗಳು
ಪದಾರ್ಥಗಳನ್ನು ಕರಗಿಸುವ ಪ್ರಕ್ರಿಯೆಯನ್ನು ಪರಿಗಣಿಸೋಣ.
ಉದಾಹರಣೆಗೆ, ನಾವು ಚಹಾಕ್ಕೆ ಸಕ್ಕರೆಯನ್ನು ಸೇರಿಸಿದರೆ, ಘನ ಪದಾರ್ಥದ ಪ್ರಮಾಣವು ಹೇಗೆ ಕ್ರಮೇಣ ಕಡಿಮೆಯಾಗುತ್ತದೆ ಎಂಬುದನ್ನು ನಾವು ಗಮನಿಸಬಹುದು. ಚಹಾ ತಣ್ಣಗಾಗಿದ್ದರೆ, ಸಕ್ಕರೆ ನಿಧಾನವಾಗಿ ಕರಗುತ್ತದೆ. ಇದಕ್ಕೆ ತದ್ವಿರುದ್ಧವಾಗಿ, ಚಹಾ ಬಿಸಿಯಾಗಿದ್ದರೆ ಮತ್ತು ಚಮಚದೊಂದಿಗೆ ಬೆರೆಸಿದರೆ, ನಂತರ ವಿಸರ್ಜನೆಯು ತ್ವರಿತವಾಗಿ ಸಂಭವಿಸುತ್ತದೆ. ಒಮ್ಮೆ ನೀರಿನಲ್ಲಿ, ಹರಳಾಗಿಸಿದ ಸಕ್ಕರೆ ಹರಳುಗಳ ಮೇಲ್ಮೈಯಲ್ಲಿರುವ ಸಕ್ಕರೆ ಅಣುಗಳು ನೀರಿನ ಅಣುಗಳೊಂದಿಗೆ ಬಂಧಗಳನ್ನು ರೂಪಿಸುತ್ತವೆ. ಈ ಸಂದರ್ಭದಲ್ಲಿ, ಹಲವಾರು ನೀರಿನ ಅಣುಗಳು ಒಂದು ಸಕ್ಕರೆ ಅಣುವಿಗೆ ಬಂಧಿಸುತ್ತವೆ. ನೀರಿನ ಅಣುಗಳ ಉಷ್ಣ ಚಲನೆಯು ಅವುಗಳಿಗೆ ಸಂಬಂಧಿಸಿದ ಸಕ್ಕರೆ ಅಣುಗಳನ್ನು ಸ್ಫಟಿಕದಿಂದ ಬೇರ್ಪಡಿಸಲು ಮತ್ತು ದ್ರಾವಕ ಅಣುಗಳ ದಪ್ಪಕ್ಕೆ ಚಲಿಸುವಂತೆ ಮಾಡುತ್ತದೆ. ಸ್ಫಟಿಕದಿಂದ ದ್ರಾವಣಕ್ಕೆ ಹಾದುಹೋದ ಸಕ್ಕರೆ ಅಣುಗಳು ಪ್ರಸರಣದಿಂದಾಗಿ ನೀರಿನ ಅಣುಗಳೊಂದಿಗೆ ದ್ರಾವಣದ ಸಂಪೂರ್ಣ ಪರಿಮಾಣದ ಉದ್ದಕ್ಕೂ ಚಲಿಸಬಹುದು. ದ್ರಾವಣವನ್ನು ಬಿಸಿಮಾಡಿದರೆ ಅಥವಾ ಬೆರೆಸಿದರೆ, ಪ್ರಸರಣವು ಹೆಚ್ಚು ತೀವ್ರವಾಗಿ ಸಂಭವಿಸುತ್ತದೆ ಮತ್ತು ಸಕ್ಕರೆ ವೇಗವಾಗಿ ಕರಗುತ್ತದೆ. ಸಕ್ಕರೆಯ ಅಣುಗಳನ್ನು ಸಮವಾಗಿ ವಿತರಿಸಲಾಗುತ್ತದೆ ಮತ್ತು ದ್ರಾವಣವು ಪರಿಮಾಣದ ಉದ್ದಕ್ಕೂ ಸಮಾನವಾಗಿ ಸಿಹಿಯಾಗಿರುತ್ತದೆ.
ಕರಗಿದಾಗ ವಸ್ತುಗಳು ಬದಲಾಗುವುದಿಲ್ಲ; ದ್ರಾವಣಗಳ ಆವಿಯಾದ ನಂತರ, ನಾವು ಕರಗಿದ ವಸ್ತುವನ್ನು ಘನ ಸ್ಥಿತಿಯಲ್ಲಿ ಪಡೆಯಬಹುದು. ವಿಸರ್ಜನೆಯ ಸಮಯದಲ್ಲಿ, ದ್ರಾವಣದ ಸ್ಫಟಿಕ ಜಾಲರಿಯು ನಾಶವಾಗುತ್ತದೆ ಮತ್ತು ಅದರ ಕಣಗಳು ದ್ರಾವಣದಲ್ಲಿ ಚಲಿಸುತ್ತವೆ, ಆದ್ದರಿಂದ, ವಿಸರ್ಜನೆಯು ಭೌತಿಕ ಪ್ರಕ್ರಿಯೆಯಾಗಿದೆ. ಅಂತಹ ಪ್ರಕ್ರಿಯೆಯನ್ನು ಕೈಗೊಳ್ಳಲು, ಶಕ್ತಿಯನ್ನು ವ್ಯಯಿಸುವುದು ಅವಶ್ಯಕ.
ಆದರೆ ದ್ರಾವಕ ಅಣುಗಳು ನೀರಿನ ಅಣುಗಳೊಂದಿಗೆ ಬಂಧಿಸಿದಾಗ, ಹೊಸ ರಾಸಾಯನಿಕ ಸಂಯುಕ್ತಗಳು ವಾಸ್ತವವಾಗಿ ರೂಪುಗೊಳ್ಳುತ್ತವೆ. ಈ ಆಣ್ವಿಕ ಸಹವರ್ತಿಗಳು ಸ್ಥಿರ ಸಂಯೋಜನೆಯನ್ನು ಹೊಂದಿಲ್ಲ. ಅವರ ಸಾಮಾನ್ಯ ಹೆಸರು- ಹೈಡ್ರೇಟ್. ನೀರಿನೊಂದಿಗೆ ವಸ್ತುಗಳನ್ನು ಬಂಧಿಸುವ ಪ್ರಕ್ರಿಯೆಯನ್ನು ಜಲಸಂಚಯನ ಎಂದು ಕರೆಯಲಾಗುತ್ತದೆ. ದ್ರಾವಣಗಳು ಆವಿಯಾದಾಗ, ಹೈಡ್ರೇಟ್ಗಳು ನಾಶವಾಗುತ್ತವೆ ಮತ್ತು ರೂಪುಗೊಳ್ಳುತ್ತವೆ ಸ್ಫಟಿಕದಂತಹ ವಸ್ತು. ಆದಾಗ್ಯೂ, ಕೆಲವು ವಸ್ತುಗಳು ಸ್ಥಿರವಾದ ಹೈಡ್ರೇಟ್ಗಳನ್ನು ರೂಪಿಸಲು ಸಮರ್ಥವಾಗಿವೆ, ಇದು ಸ್ಫಟಿಕದ ಸ್ಥಿತಿಯಲ್ಲಿಯೂ ಸಹ ನೀರನ್ನು ಹೊಂದಿರುತ್ತದೆ. ಅಂತಹ ವಸ್ತುಗಳನ್ನು ಸ್ಫಟಿಕದಂತಹ ಹೈಡ್ರೇಟ್ ಎಂದು ಕರೆಯಲಾಗುತ್ತದೆ. ನೀರನ್ನು ಎಚ್ಚರಿಕೆಯಿಂದ ಆವಿಯಾಗುವ ಮೂಲಕ ಅವುಗಳನ್ನು ದ್ರಾವಣದಿಂದ ಪ್ರತ್ಯೇಕಿಸಬಹುದು. ಅಂತಹ ಪದಾರ್ಥಗಳ ಸೂತ್ರಗಳಲ್ಲಿ, ಸ್ಫಟಿಕೀಕರಣದ ನೀರನ್ನು ಗುಣಾಕಾರ ಚಿಹ್ನೆಯೊಂದಿಗೆ ಸಂಯುಕ್ತದ ಸೂತ್ರದ ನಂತರ ಸೂಚಿಸಲಾಗುತ್ತದೆ. ಉದಾಹರಣೆಗೆ: CuSO 4 5H 2 O - ತಾಮ್ರದ ಸಲ್ಫೇಟ್, FeSO 4 7H 2 O - ಕಬ್ಬಿಣದ ಸಲ್ಫೇಟ್. ಹೈಡ್ರೇಟ್ ರಚನೆ, ಅಂದರೆ. ಹೊಸ ಪದಾರ್ಥಗಳು, ವಿಸರ್ಜನೆಯು ರಾಸಾಯನಿಕ ಪ್ರಕ್ರಿಯೆ ಎಂದು ಸೂಚಿಸುತ್ತದೆ.
ಈ ಪ್ರಕ್ರಿಯೆಯಲ್ಲಿ ಸಂಭವಿಸುವ ಉಷ್ಣ ವಿದ್ಯಮಾನಗಳ ಅಧ್ಯಯನವು ವಿಸರ್ಜನೆಯ ಪ್ರಕ್ರಿಯೆಯ ಸಾರವನ್ನು ಅರ್ಥಮಾಡಿಕೊಳ್ಳಲು ಸಹಾಯ ಮಾಡುತ್ತದೆ. ರಾಸಾಯನಿಕ ಕ್ರಿಯೆಗಳ ಚಿಹ್ನೆಗಳಲ್ಲಿ ಒಂದು ಶಾಖದ ಬಿಡುಗಡೆಯಾಗಿದೆ ಎಂದು ತಿಳಿದಿದೆ ಮತ್ತು ಭೌತಿಕ ವಿದ್ಯಮಾನಗಳಿಗೆ ಶಕ್ತಿಯನ್ನು ವ್ಯಯಿಸುವುದು ಅವಶ್ಯಕ. ಸಲ್ಫ್ಯೂರಿಕ್ ಆಮ್ಲದ ವಿಸರ್ಜನೆಯು ದ್ರಾವಣದ ಬಲವಾದ ತಾಪನದೊಂದಿಗೆ ಇರುತ್ತದೆ. ಇದು ನೀರು ಮತ್ತು ದ್ರಾವಕ ಅಣುಗಳ ನಡುವಿನ ರಾಸಾಯನಿಕ ಪರಸ್ಪರ ಕ್ರಿಯೆಯ ಪರಿಣಾಮವಾಗಿದೆ - ಜಲಸಂಚಯನವು ಶಕ್ತಿಯ ಬಿಡುಗಡೆಯೊಂದಿಗೆ ಇರುತ್ತದೆ. ಮತ್ತು ಅಮೋನಿಯಂ ನೈಟ್ರೇಟ್ನ ವಿಸರ್ಜನೆಯು ದ್ರಾವಣದ ತಂಪಾಗಿಸುವಿಕೆಯೊಂದಿಗೆ ಇರುತ್ತದೆ. ಈ ಸಂದರ್ಭದಲ್ಲಿ, ಹೈಡ್ರೇಟ್ಗಳ ಉತ್ಪಾದನೆಯ ಸಮಯದಲ್ಲಿ ಉತ್ಪತ್ತಿಯಾಗುವ ಶಕ್ತಿಗಿಂತ ಸ್ಫಟಿಕ ಜಾಲರಿಯ ವಿನಾಶದ ಭೌತಿಕ ಪ್ರಕ್ರಿಯೆಯಲ್ಲಿ ಹೆಚ್ಚಿನ ಶಕ್ತಿಯನ್ನು ವ್ಯಯಿಸಲಾಗುತ್ತದೆ.
ಮೇಲಿನ ಸಂಗತಿಗಳು ವಿಸರ್ಜನೆಯನ್ನು ಭೌತ ರಾಸಾಯನಿಕ ಪ್ರಕ್ರಿಯೆ ಎಂದು ಪರಿಗಣಿಸಬೇಕೆಂದು ಸೂಚಿಸುತ್ತವೆ.
ಮನೆಕೆಲಸ: ಪ್ಯಾರಾಗ್ರಾಫ್ 34, ವ್ಯಾಯಾಮ 2
ವ್ಯಾಖ್ಯಾನಗಳನ್ನು ಕಲಿಯಿರಿ
ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳು ಮತ್ತು ನಾನ್-ಎಲೆಕ್ಟ್ರೋಲೈಟ್ಗಳು.
ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳು- ಇವುಗಳು ದ್ರಾವಣಗಳು ಅಥವಾ ಕರಗುವಿಕೆಗಳು ವಿದ್ಯುತ್ ಪ್ರವಾಹವನ್ನು ನಡೆಸುವ ವಸ್ತುಗಳು.
ನಾನ್-ಎಲೆಕ್ಟ್ರೋಲೈಟ್ಸ್- ಇವುಗಳು ದ್ರಾವಣಗಳು ಅಥವಾ ಕರಗುವಿಕೆಗಳು ವಿದ್ಯುತ್ ಪ್ರವಾಹವನ್ನು ನಡೆಸದ ಪದಾರ್ಥಗಳಾಗಿವೆ.
ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯ ವಿಘಟನೆ- ಇದು ನೀರಿನಲ್ಲಿ ಕರಗಿದಾಗ ಅಥವಾ ಕರಗಿದಾಗ ಮುಕ್ತವಾಗಿ ಚಲಿಸುವ ಅಯಾನುಗಳಾಗಿ ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯದ ವಿಭಜನೆಯಾಗಿದೆ.
ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳುನೀರಿನಲ್ಲಿ ಕರಗಿದಾಗ ಅಥವಾ
ಕರಗುತ್ತಿದೆ ಒಡೆಯುತ್ತವೆ (ಬೇರ್ಪಡಿಸು) ಅಯಾನುಗಳಿಗೆ - ಧನಾತ್ಮಕ (ಕ್ಯಾಟೇಶನ್) ಮತ್ತು ಋಣಾತ್ಮಕ (ಅಯಾನುಗಳು) ಚಾರ್ಜ್ಡ್ ಕಣಗಳು.
ಅಯಾನುಗಳುಹೆಚ್ಚು ಸ್ಥಿರವಾಗಿರುತ್ತವೆ ಎಲೆಕ್ಟ್ರಾನಿಕ್ ರಾಜ್ಯಗಳುಪರಮಾಣುಗಳಿಗಿಂತ. ಅವು ಒಂದು ಪರಮಾಣುವಿನಿಂದ ಕೂಡಿರಬಹುದು - ಇದು ಸರಳ ಅಯಾನುಗಳು(Na +, Mg 2+, Al 3+, ಇತ್ಯಾದಿ) - ಅಥವಾ ಹಲವಾರು ಪರಮಾಣುಗಳಿಂದ - ಇದು ಸಂಕೀರ್ಣ ಅಯಾನುಗಳು(NO 3 -, SO 2- 4, RO Z- 4, ಇತ್ಯಾದಿ).
ದ್ರಾವಣಗಳಲ್ಲಿ ಮತ್ತು ಕರಗುತ್ತದೆ ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳು ವಿದ್ಯುಚ್ಛಕ್ತಿಯನ್ನು ನಡೆಸುತ್ತವೆ .
ಪ್ರಭಾವದಿಂದ ವಿದ್ಯುತ್ಅಯಾನುಗಳು ದಿಕ್ಕಿನ ಚಲನೆಯನ್ನು ಪಡೆದುಕೊಳ್ಳುತ್ತವೆ: ಧನಾತ್ಮಕ ಆವೇಶದ ಅಯಾನುಗಳು ಕ್ಯಾಥೋಡ್ ಕಡೆಗೆ ಚಲಿಸುತ್ತವೆ, ಋಣಾತ್ಮಕ ಆವೇಶವು ಆನೋಡ್ ಕಡೆಗೆ ಚಲಿಸುತ್ತದೆ. ಆದ್ದರಿಂದ, ಮೊದಲನೆಯದನ್ನು ಕ್ಯಾಟಯಾನ್ಸ್ ಎಂದು ಕರೆಯಲಾಗುತ್ತದೆ, ಎರಡನೆಯದು - ಅಯಾನುಗಳು. ಅಯಾನುಗಳ ದಿಕ್ಕಿನ ಚಲನೆಯು ವಿರುದ್ಧವಾಗಿ ಚಾರ್ಜ್ ಮಾಡಲಾದ ವಿದ್ಯುದ್ವಾರಗಳಿಂದ ಅವುಗಳ ಆಕರ್ಷಣೆಯ ಪರಿಣಾಮವಾಗಿ ಸಂಭವಿಸುತ್ತದೆ.
ವಿಘಟನೆ- ಹಿಂತಿರುಗಿಸಬಹುದಾದ ಪ್ರಕ್ರಿಯೆ: ಅಣುಗಳನ್ನು ಅಯಾನುಗಳಾಗಿ ವಿಘಟನೆಯೊಂದಿಗೆ ಸಮಾನಾಂತರವಾಗಿ (ವಿಘಟನೆ), ಅಯಾನುಗಳನ್ನು ಸಂಯೋಜಿಸುವ ಪ್ರಕ್ರಿಯೆಯು (ಸಂಘ) ಸಂಭವಿಸುತ್ತದೆ.
ಆದ್ದರಿಂದ, ವಿದ್ಯುದ್ವಿಭಜನೆಯ ವಿಘಟನೆಯ ಸಮೀಕರಣಗಳಲ್ಲಿ, ಸಮಾನ ಚಿಹ್ನೆಯ ಬದಲಿಗೆ, ರಿವರ್ಸಿಬಿಲಿಟಿ ಚಿಹ್ನೆಯನ್ನು ಬಳಸಲಾಗುತ್ತದೆ. ಉದಾಹರಣೆಗೆ, ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯ ಅಣುವಿನ KA ಯ ವಿಘಟನೆಯ ಸಮೀಕರಣವು ಕ್ಯಾಷನ್ K + ಮತ್ತು ಅಯಾನು A - ಇನ್ ಸಾಮಾನ್ಯ ನೋಟದಾಖಲಿಸಲಾಗಿದೆ
KA ↔ K + + A -
ಮನೆಕೆಲಸ: ಪ್ಯಾರಾಗ್ರಾಫ್ 35, ಉದಾ. 1,4,5, ವ್ಯಾಖ್ಯಾನಗಳನ್ನು ತಿಳಿಯಿರಿ
TED ಯ ಮೂಲ ನಿಬಂಧನೆಗಳು.
1. ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳು, ನೀರಿನಲ್ಲಿ ಕರಗಿದಾಗ, ಅಯಾನುಗಳಾಗಿ ವಿಭಜಿಸುತ್ತವೆ (ವಿಭಜಿಸಿ) - ಧನಾತ್ಮಕ ಮತ್ತು ಋಣಾತ್ಮಕ.
2. ವಿದ್ಯುತ್ ಪ್ರವಾಹದ ಪ್ರಭಾವದ ಅಡಿಯಲ್ಲಿ, ಅಯಾನುಗಳು ದಿಕ್ಕಿನ ಚಲನೆಯನ್ನು ಪಡೆದುಕೊಳ್ಳುತ್ತವೆ: ಧನಾತ್ಮಕ ಆವೇಶದ ಕಣಗಳು ಕ್ಯಾಥೋಡ್ ಕಡೆಗೆ ಚಲಿಸುತ್ತವೆ, ಋಣಾತ್ಮಕ ಆವೇಶದ ಕಣಗಳು ಆನೋಡ್ ಕಡೆಗೆ ಚಲಿಸುತ್ತವೆ. ಆದ್ದರಿಂದ, ಧನಾತ್ಮಕ ಆವೇಶದ ಕಣಗಳನ್ನು ಕ್ಯಾಟಯಾನ್ಸ್ ಎಂದು ಕರೆಯಲಾಗುತ್ತದೆ ಮತ್ತು ಋಣಾತ್ಮಕ ಆವೇಶದ ಕಣಗಳನ್ನು ಅಯಾನುಗಳು ಎಂದು ಕರೆಯಲಾಗುತ್ತದೆ.
3. ನಿರ್ದೇಶನದ ಚಲನೆಯು ಅವುಗಳ ವಿರುದ್ಧವಾಗಿ ಚಾರ್ಜ್ಡ್ ವಿದ್ಯುದ್ವಾರಗಳಿಂದ ಆಕರ್ಷಣೆಯ ಪರಿಣಾಮವಾಗಿ ಸಂಭವಿಸುತ್ತದೆ (ಕ್ಯಾಥೋಡ್ ಋಣಾತ್ಮಕವಾಗಿ ಚಾರ್ಜ್ ಆಗುತ್ತದೆ, ಮತ್ತು ಆನೋಡ್ ಧನಾತ್ಮಕವಾಗಿ ಚಾರ್ಜ್ ಆಗುತ್ತದೆ).
4. ಅಯಾನೀಕರಣವು ಹಿಂತಿರುಗಿಸಬಹುದಾದ ಪ್ರಕ್ರಿಯೆಯಾಗಿದೆ: ಅಣುಗಳ ವಿಘಟನೆಯೊಂದಿಗೆ ಸಮಾನಾಂತರವಾಗಿ ಅಯಾನುಗಳು (ವಿಯೋಜನೆ), ಅಯಾನುಗಳನ್ನು ಅಣುಗಳಾಗಿ ಸಂಯೋಜಿಸುವ ಪ್ರಕ್ರಿಯೆಯು (ಸಂಘ) ಸಂಭವಿಸುತ್ತದೆ.
ಎಲೆಕ್ಟ್ರೋಲೈಟಿಕ್ ಡಿಸೋಸಿಯೇಷನ್ ಸಿದ್ಧಾಂತದ ಆಧಾರದ ಮೇಲೆ, ನಾವು ನೀಡಬಹುದು ಕೆಳಗಿನ ವ್ಯಾಖ್ಯಾನಗಳುಮುಖ್ಯ ಸಂಪರ್ಕ ತರಗತಿಗಳಿಗೆ:
ಆಮ್ಲಗಳು ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳಾಗಿವೆ, ಅದರ ವಿಘಟನೆಯು ಕ್ಯಾಟಯಾನುಗಳಾಗಿ ಹೈಡ್ರೋಜನ್ ಅಯಾನುಗಳನ್ನು ಮಾತ್ರ ಉತ್ಪಾದಿಸುತ್ತದೆ. ಉದಾಹರಣೆಗೆ,
HCl → H + + Cl - ;
CH 3 COOH H + + CH 3 COO - .
ವಿಘಟನೆಯ ಸಮಯದಲ್ಲಿ ರೂಪುಗೊಳ್ಳುವ ಹೈಡ್ರೋಜನ್ ಕ್ಯಾಟಯಾನುಗಳ ಸಂಖ್ಯೆಯಿಂದ ಆಮ್ಲದ ಮೂಲಭೂತತೆಯನ್ನು ನಿರ್ಧರಿಸಲಾಗುತ್ತದೆ. ಹೀಗಾಗಿ, HCl, HNO 3 ಮೊನೊಬಾಸಿಕ್ ಆಮ್ಲಗಳು, H 2 SO 4, H 2 CO 3 ಡೈಬಾಸಿಕ್, H 3 PO 4, H 3 AsO 4 ಟ್ರಿಬಾಸಿಕ್.
ಬೇಸ್ಗಳು ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳಾಗಿವೆ, ಅದರ ವಿಘಟನೆಯು ಹೈಡ್ರಾಕ್ಸೈಡ್ ಅಯಾನುಗಳನ್ನು ಮಾತ್ರ ಅಯಾನುಗಳಾಗಿ ಉತ್ಪಾದಿಸುತ್ತದೆ. ಉದಾಹರಣೆಗೆ,
KOH → K + + OH - ,
NH 4 OH NH 4 + + OH - .
ನೀರಿನಲ್ಲಿ ಕರಗುವ ಮೂಲಗಳನ್ನು ಕ್ಷಾರಗಳು ಎಂದು ಕರೆಯಲಾಗುತ್ತದೆ.
ಬೇಸ್ನ ಆಮ್ಲೀಯತೆಯನ್ನು ಅದರ ಹೈಡ್ರಾಕ್ಸಿಲ್ ಗುಂಪುಗಳ ಸಂಖ್ಯೆಯಿಂದ ನಿರ್ಧರಿಸಲಾಗುತ್ತದೆ. ಉದಾಹರಣೆಗೆ, KOH, NaOH ಒಂದು-ಆಮ್ಲ ಬೇಸ್ಗಳು, Ca(OH) 2 ಎರಡು-ಆಮ್ಲ, Sn(OH) 4 ನಾಲ್ಕು-ಆಮ್ಲ, ಇತ್ಯಾದಿ.
ಲವಣಗಳು ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳಾಗಿವೆ, ಇವುಗಳ ವಿಘಟನೆಯು ಲೋಹದ ಕ್ಯಾಟಯಾನುಗಳನ್ನು (ಹಾಗೆಯೇ NH 4 + ಅಯಾನ್) ಮತ್ತು ಅಯಾನುಗಳನ್ನು ಉತ್ಪಾದಿಸುತ್ತದೆ ಆಮ್ಲದ ಉಳಿಕೆಗಳು. ಉದಾಹರಣೆಗೆ,
CaCl 2 → Ca 2+ + 2Cl - ,
NaF → Na + + F - .
ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳು, ಅದರ ವಿಘಟನೆಯ ಸಮಯದಲ್ಲಿ, ಪರಿಸ್ಥಿತಿಗಳನ್ನು ಅವಲಂಬಿಸಿ, ಹೈಡ್ರೋಜನ್ ಕ್ಯಾಟಯಾನುಗಳು ಮತ್ತು ಅಯಾನುಗಳನ್ನು ಏಕಕಾಲದಲ್ಲಿ ರಚಿಸಬಹುದು - ಹೈಡ್ರಾಕ್ಸೈಡ್ ಅಯಾನುಗಳನ್ನು ಆಂಫೋಟೆರಿಕ್ ಎಂದು ಕರೆಯಲಾಗುತ್ತದೆ. ಉದಾಹರಣೆಗೆ,
H 2 O H + +OH -,
Zn(OH) 2 Zn 2+ +2OH - ,
Zn(OH) 2 2H + +ZnO 2 2- ಅಥವಾ
Zn(OH) 2 + 2H 2 O 2- + 2H + .
ಮನೆಕೆಲಸ: ಪ್ಯಾರಾಗ್ರಾಫ್ 36, ಉದಾ. 2-5, ವ್ಯಾಖ್ಯಾನಗಳನ್ನು ಕಲಿಯಿರಿ
