ಎಥಿಲೀನ್ ಸರಣಿಯ ಅಪರ್ಯಾಪ್ತ ಅಥವಾ ಅಪರ್ಯಾಪ್ತ ಹೈಡ್ರೋಕಾರ್ಬನ್ಗಳು
(ಆಲ್ಕೆನ್ಸ್ ಅಥವಾ ಒಲೆಫಿನ್ಸ್)
ಆಲ್ಕೆನೆಸ್, ಅಥವಾ ಒಲೆಫಿನ್ಗಳು(ಲ್ಯಾಟಿನ್ ನಿಂದ ಓಲಿಫಿಯಾಂಟ್ - ಎಣ್ಣೆ - ಹಳೆಯ ಹೆಸರು, ಆದರೆ ರಾಸಾಯನಿಕ ಸಾಹಿತ್ಯದಲ್ಲಿ ವ್ಯಾಪಕವಾಗಿ ಬಳಸಲಾಗುತ್ತದೆ. ಈ ಹೆಸರಿಗೆ ಕಾರಣ ಎಥಿಲೀನ್ ಕ್ಲೋರೈಡ್ ಅನ್ನು ಪಡೆಯಲಾಗಿದೆ XVIII ಶತಮಾನ, - ದ್ರವ ಎಣ್ಣೆಯುಕ್ತ ವಸ್ತು.) - ಅಲಿಫ್ಯಾಟಿಕ್ ಅಪರ್ಯಾಪ್ತ ಹೈಡ್ರೋಕಾರ್ಬನ್ಗಳು, ಅಣುಗಳಲ್ಲಿ ಇಂಗಾಲದ ಪರಮಾಣುಗಳ ನಡುವೆ ಒಂದು ಡಬಲ್ ಬಂಧವಿದೆ.
ಆಲ್ಕೀನ್ಗಳು ಅವುಗಳ ಅಣುವಿನಲ್ಲಿ ಅವುಗಳ ಅನುಗುಣವಾದ ಆಲ್ಕೇನ್ಗಳಿಗಿಂತ ಕಡಿಮೆ ಹೈಡ್ರೋಜನ್ ಪರಮಾಣುಗಳನ್ನು ಹೊಂದಿರುತ್ತವೆ (ಅದೇ ಸಂಖ್ಯೆಯ ಇಂಗಾಲದ ಪರಮಾಣುಗಳೊಂದಿಗೆ), ಆದ್ದರಿಂದ ಅಂತಹ ಹೈಡ್ರೋಕಾರ್ಬನ್ಗಳನ್ನು ಕರೆಯಲಾಗುತ್ತದೆ ಅನಿಯಮಿತಅಥವಾ ಅಪರ್ಯಾಪ್ತ.
ಆಲ್ಕೀನ್ಗಳು ಸಾಮಾನ್ಯ ಸೂತ್ರದೊಂದಿಗೆ ಏಕರೂಪದ ಸರಣಿಯನ್ನು ರೂಪಿಸುತ್ತವೆ CnH2n
1. ಆಲ್ಕೀನ್ಗಳ ಏಕರೂಪದ ಸರಣಿ
|
ಇದರೊಂದಿಗೆ ಎನ್ ಎಚ್ 2 ಎನ್ ಕ್ಷಾರೀಯ |
ಹೆಸರುಗಳು, ಪ್ರತ್ಯಯ EH, ILENE |
|
C2H4 |
ಇದು en, ಇದು ಇಲೆನ್ |
|
C3H6 |
ಒಲವುಳ್ಳ |
|
C4H8 |
ಬ್ಯೂಟಿನ್ |
|
C5H10 |
ಪೆಂಟೆನ್ |
|
C6H12 |
ಹೆಕ್ಸೀನ್ |
ಹೋಮೋಲೋಗ್ಸ್:
ಇದರೊಂದಿಗೆಎಚ್ 2 = ಸಿಎಚ್ 2 ಈಥೀನ್
ಇದರೊಂದಿಗೆಎಚ್ 2 = ಸಿಎಚ್- ಸಿಎಚ್ 3 ಒಲವುಳ್ಳ
ಇದರೊಂದಿಗೆH 2 =CH-CH 2 -CH 3ಬ್ಯೂಟಿನ್-1
ಇದರೊಂದಿಗೆH 2 =CH-CH 2 -CH 2 -ಸಿಎಚ್ 3 ಪೆಂಟೆನ್-1
2. ಭೌತಿಕ ಗುಣಲಕ್ಷಣಗಳು
ಎಥಿಲೀನ್ (ಇಥೀನ್) - ಬಣ್ಣರಹಿತ ಅನಿಲತುಂಬಾ ಮಸುಕಾದ ಸಿಹಿ ವಾಸನೆಯೊಂದಿಗೆ, ಗಾಳಿಗಿಂತ ಸ್ವಲ್ಪ ಹಗುರವಾಗಿರುತ್ತದೆ, ನೀರಿನಲ್ಲಿ ಸ್ವಲ್ಪ ಕರಗುತ್ತದೆ.
C 2 – C 4 (ಅನಿಲಗಳು)
C 5 - C 17 (ದ್ರವಗಳು)
C 18 - (ಘನ)
· ಆಲ್ಕೀನ್ಗಳು ನೀರಿನಲ್ಲಿ ಕರಗುವುದಿಲ್ಲ, ಸಾವಯವ ದ್ರಾವಕಗಳಲ್ಲಿ ಕರಗುತ್ತವೆ (ಗ್ಯಾಸೋಲಿನ್, ಬೆಂಜೀನ್, ಇತ್ಯಾದಿ)
ನೀರಿಗಿಂತ ಹಗುರ
ಮಿಸ್ಟರ್ ಅನ್ನು ಹೆಚ್ಚಿಸುವುದರೊಂದಿಗೆ, ಕರಗುವ ಮತ್ತು ಕುದಿಯುವ ಬಿಂದುಗಳು ಹೆಚ್ಚಾಗುತ್ತವೆ
3. ಸರಳವಾದ ಆಲ್ಕೀನ್ ಆಗಿದೆ ಎಥಿಲೀನ್ - C2H4
ರಚನಾತ್ಮಕ ಮತ್ತು ಎಲೆಕ್ಟ್ರಾನಿಕ್ ಸೂತ್ರಎಥಿಲೀನ್ ರೂಪವನ್ನು ಹೊಂದಿದೆ:
ಎಥಿಲೀನ್ ಅಣುವಿನಲ್ಲಿ ಒಂದು ಹೈಬ್ರಿಡೈಸೇಶನ್ಗೆ ಒಳಗಾಗುತ್ತದೆ ರು- ಮತ್ತು ಎರಡು ಪ-ಸಿ ಪರಮಾಣುಗಳ ಕಕ್ಷೆಗಳು ( sp 2 -ಹೈಬ್ರಿಡೈಸೇಶನ್).
ಹೀಗಾಗಿ, ಪ್ರತಿ C ಪರಮಾಣುವಿನಲ್ಲಿ ಮೂರು ಹೈಬ್ರಿಡ್ ಆರ್ಬಿಟಲ್ಗಳು ಮತ್ತು ಒಂದು ಹೈಬ್ರಿಡ್ ಅಲ್ಲದವು ಪ- ಕಕ್ಷೆಗಳು. C ಪರಮಾಣುಗಳ ಎರಡು ಹೈಬ್ರಿಡ್ ಕಕ್ಷೆಗಳು ಪರಸ್ಪರ ಅತಿಕ್ರಮಿಸುತ್ತವೆ ಮತ್ತು C ಪರಮಾಣುಗಳ ನಡುವೆ ರೂಪುಗೊಳ್ಳುತ್ತವೆ
σ - ಬಂಧ. C ಪರಮಾಣುಗಳ ಉಳಿದ ನಾಲ್ಕು ಹೈಬ್ರಿಡ್ ಆರ್ಬಿಟಲ್ಗಳು ಒಂದೇ ಸಮತಲದಲ್ಲಿ ನಾಲ್ಕರೊಂದಿಗೆ ಅತಿಕ್ರಮಿಸುತ್ತವೆ ರು H ಪರಮಾಣುಗಳ ಕಕ್ಷೆಗಳು ಮತ್ತು ನಾಲ್ಕು σ - ಬಂಧಗಳನ್ನು ರೂಪಿಸುತ್ತವೆ. ಎರಡು ಹೈಬ್ರಿಡ್ ಅಲ್ಲದ ಪ-ಸಿ ಪರಮಾಣುಗಳ ಕಕ್ಷೆಗಳು σ-ಬಂಧ ಸಮತಲಕ್ಕೆ ಲಂಬವಾಗಿರುವ ಸಮತಲದಲ್ಲಿ ಪರಸ್ಪರ ಅತಿಕ್ರಮಿಸುತ್ತವೆ, ಅಂದರೆ. ಒಂದು ರೂಪುಗೊಂಡಿದೆ ಪ- ಸಂಪರ್ಕ.

ಅದರ ಸ್ವಭಾವದಿಂದ ಪ- ಸಂಪರ್ಕವು σ - ಸಂಪರ್ಕದಿಂದ ತೀವ್ರವಾಗಿ ಭಿನ್ನವಾಗಿದೆ; ಪ- ಅಣುವಿನ ಸಮತಲದ ಹೊರಗೆ ಎಲೆಕ್ಟ್ರಾನ್ ಮೋಡಗಳ ಅತಿಕ್ರಮಣದಿಂದಾಗಿ ಬಂಧವು ಕಡಿಮೆ ಬಲವಾಗಿರುತ್ತದೆ. ಕಾರಕಗಳ ಪ್ರಭಾವದ ಅಡಿಯಲ್ಲಿ ಪ- ಸಂಪರ್ಕವು ಸುಲಭವಾಗಿ ಮುರಿದುಹೋಗುತ್ತದೆ.
ಎಥಿಲೀನ್ ಅಣುವು ಸಮ್ಮಿತೀಯವಾಗಿದೆ; ಎಲ್ಲಾ ಪರಮಾಣುಗಳ ನ್ಯೂಕ್ಲಿಯಸ್ಗಳು ಒಂದೇ ಸಮತಲದಲ್ಲಿವೆ ಮತ್ತು ಬಂಧದ ಕೋನಗಳು 120 ° ಗೆ ಹತ್ತಿರದಲ್ಲಿವೆ; C ಪರಮಾಣುಗಳ ಕೇಂದ್ರಗಳ ನಡುವಿನ ಅಂತರವು 0.134 nm ಆಗಿದೆ.
ಪರಮಾಣುಗಳನ್ನು ಎರಡು ಬಂಧದಿಂದ ಸಂಪರ್ಕಿಸಿದರೆ, ಎಲೆಕ್ಟ್ರಾನ್ ಮೋಡಗಳಿಲ್ಲದೆ ಅವುಗಳ ತಿರುಗುವಿಕೆ ಅಸಾಧ್ಯ ಪ- ಸಂಪರ್ಕವನ್ನು ತೆರೆಯಲಾಗಿಲ್ಲ.
4. ಆಲ್ಕೀನ್ಗಳ ಐಸೋಮೆರಿಸಂ
ಜೊತೆಗೆ ಕಾರ್ಬನ್ ಅಸ್ಥಿಪಂಜರದ ರಚನಾತ್ಮಕ ಐಸೋಮೆರಿಸಂ ಆಲ್ಕೀನ್ಗಳನ್ನು ಮೊದಲನೆಯದಾಗಿ, ಇತರ ರೀತಿಯ ರಚನಾತ್ಮಕ ಐಸೋಮೆರಿಸಂನಿಂದ ನಿರೂಪಿಸಲಾಗಿದೆ - ಬಹು ಬಂಧ ಸ್ಥಾನ ಐಸೋಮೆರಿಸಂಮತ್ತು ಇಂಟರ್ಕ್ಲಾಸ್ ಐಸೋಮೆರಿಸಂ.
ಎರಡನೆಯದಾಗಿ, ಆಲ್ಕೀನ್ಗಳ ಸರಣಿಯಲ್ಲಿ ಇದೆ ಪ್ರಾದೇಶಿಕ ಐಸೋಮೆರಿಸಂ , ಗೆ ಸಂಬಂಧಿಸಿದಂತೆ ಬದಲಿಗಳ ವಿವಿಧ ಸ್ಥಾನಗಳೊಂದಿಗೆ ಸಂಬಂಧಿಸಿದೆ ಡಬಲ್ ಬಾಂಡ್, ಅದರ ಸುತ್ತಲೂ ಇಂಟ್ರಾಮೋಲಿಕ್ಯುಲರ್ ತಿರುಗುವಿಕೆ ಅಸಾಧ್ಯ.
ಆಲ್ಕೀನ್ಗಳ ರಚನಾತ್ಮಕ ಐಸೋಮೆರಿಸಂ
1. ಇಂಗಾಲದ ಅಸ್ಥಿಪಂಜರದ ಐಸೋಮೆರಿಸಂ (C 4 H 8 ರಿಂದ ಪ್ರಾರಂಭವಾಗುತ್ತದೆ):
2. ಡಬಲ್ ಬಾಂಡ್ನ ಸ್ಥಾನದ ಐಸೋಮೆರಿಸಂ (C 4 H 8 ರಿಂದ ಪ್ರಾರಂಭವಾಗುತ್ತದೆ):
3. C 3 H 6 ರಿಂದ ಪ್ರಾರಂಭವಾಗುವ ಸೈಕ್ಲೋಆಲ್ಕೇನ್ಗಳೊಂದಿಗೆ ಇಂಟರ್ಕ್ಲಾಸ್ ಐಸೋಮೆರಿಸಂ:
ಆಲ್ಕೀನ್ಗಳ ಪ್ರಾದೇಶಿಕ ಐಸೋಮೆರಿಸಂ
ಎರಡು ಬಂಧದ ಸುತ್ತ ಪರಮಾಣುಗಳ ತಿರುಗುವಿಕೆ ಅದನ್ನು ಮುರಿಯದೆ ಅಸಾಧ್ಯ. ಇದು p-ಬಂಧದ ರಚನಾತ್ಮಕ ವೈಶಿಷ್ಟ್ಯಗಳಿಂದಾಗಿ (p-ಎಲೆಕ್ಟ್ರಾನ್ ಮೋಡವು ಅಣುವಿನ ಸಮತಲದ ಮೇಲೆ ಮತ್ತು ಕೆಳಗೆ ಕೇಂದ್ರೀಕೃತವಾಗಿರುತ್ತದೆ). ಪರಮಾಣುಗಳ ಕಟ್ಟುನಿಟ್ಟಾದ ಲಗತ್ತಿಸುವಿಕೆಯಿಂದಾಗಿ ತಿರುಗುವ ಐಸೋಮೆರಿಸಂಡಬಲ್ ಬಾಂಡ್ ಬಗ್ಗೆ ಕಾಣಿಸುವುದಿಲ್ಲ. ಆದರೆ ಅದು ಸಾಧ್ಯವಾಗುತ್ತದೆ ಸಿಸ್-ಟ್ರಾನ್ಸ್-ಐಸೋಮೆರಿಸಂ.
ಡಬಲ್ ಬಾಂಡ್ನಲ್ಲಿರುವ ಎರಡು ಇಂಗಾಲದ ಪರಮಾಣುಗಳ ಮೇಲೆ ವಿಭಿನ್ನ ಪರ್ಯಾಯಗಳನ್ನು ಹೊಂದಿರುವ ಆಲ್ಕೀನ್ಗಳು ಎರಡು ಪ್ರಾದೇಶಿಕ ಐಸೋಮರ್ಗಳ ರೂಪದಲ್ಲಿ ಅಸ್ತಿತ್ವದಲ್ಲಿರಬಹುದು, ಇದು p-ಬಂಧದ ಸಮತಲಕ್ಕೆ ಸಂಬಂಧಿಸಿದಂತೆ ಬದಲಿಗಳ ಸ್ಥಳದಲ್ಲಿ ಭಿನ್ನವಾಗಿರುತ್ತದೆ. ಆದ್ದರಿಂದ, ಬ್ಯೂಟಿನ್ -2 ಅಣುವಿನಲ್ಲಿ CH 3 –CH=CH-CH 3 CH 3 ಗುಂಪುಗಳನ್ನು ಡಬಲ್ ಬಾಂಡ್ನ ಒಂದು ಬದಿಯಲ್ಲಿ ಇರಿಸಬಹುದು ಸಿಸ್-ಐಸೋಮರ್, ಅಥವಾ ವಿವಿಧ ಬದಿಗಳುವಿ ಟ್ರಾನ್ಸ್-ಐಸೋಮರ್.

ಗಮನ!
ಸಿಸ್-ಟ್ರಾನ್ಸ್- ಡಬಲ್ ಬಾಂಡ್ನಲ್ಲಿರುವ C ಪರಮಾಣುಗಳಲ್ಲಿ ಕನಿಷ್ಠ ಒಂದು 2 ಒಂದೇ ಬದಲಿಗಳನ್ನು ಹೊಂದಿದ್ದರೆ ಐಸೋಮೆರಿಸಂ ಕಾಣಿಸುವುದಿಲ್ಲ.
ಉದಾಹರಣೆಗೆ,
ಬ್ಯೂಟಿನ್-1 CH 2 = CH – CH 2 – CH 3ಹೊಂದಿಲ್ಲ ಸಿಸ್- ಮತ್ತು ಟ್ರಾನ್ಸ್-ಐಸೋಮರ್ಗಳು, ಏಕೆಂದರೆ 1 ನೇ C ಪರಮಾಣು ಎರಡು ಒಂದೇ H ಪರಮಾಣುಗಳಿಗೆ ಬಂಧಿತವಾಗಿದೆ.
ಐಸೋಮರ್ಗಳು ಸಿಸ್- ಮತ್ತು ಟ್ರಾನ್ಸ್- ದೈಹಿಕವಾಗಿ ಮಾತ್ರವಲ್ಲ
 ,
,
ಆದರೆ ರಾಸಾಯನಿಕ ಗುಣಲಕ್ಷಣಗಳು, ಏಕೆಂದರೆ ಅಣುವಿನ ಭಾಗಗಳನ್ನು ಬಾಹ್ಯಾಕಾಶದಲ್ಲಿ ಪರಸ್ಪರ ಹತ್ತಿರ ಅಥವಾ ದೂರಕ್ಕೆ ತರುವುದು ರಾಸಾಯನಿಕ ಪರಸ್ಪರ ಕ್ರಿಯೆಯನ್ನು ಉತ್ತೇಜಿಸುತ್ತದೆ ಅಥವಾ ತಡೆಯುತ್ತದೆ.
ಕೆಲವೊಮ್ಮೆ ಸಿಸ್-ಟ್ರಾನ್ಸ್-ಐಸೋಮೆರಿಸಂ ಅನ್ನು ನಿಖರವಾಗಿ ಕರೆಯಲಾಗುವುದಿಲ್ಲ ಜ್ಯಾಮಿತೀಯ ಐಸೋಮೆರಿಸಂ . ಅಚಾತುರ್ಯವೆಂದರೆ ಅದು ಎಲ್ಲಾಪ್ರಾದೇಶಿಕ ಐಸೋಮರ್ಗಳು ಅವುಗಳ ಜ್ಯಾಮಿತಿಯಲ್ಲಿ ಭಿನ್ನವಾಗಿರುತ್ತವೆ ಮತ್ತು ಮಾತ್ರವಲ್ಲ ಸಿಸ್- ಮತ್ತು ಟ್ರಾನ್ಸ್-.
5. ನಾಮಕರಣ
ಆಲ್ಕೆನೆಸ್ ಸರಳ ರಚನೆಆಲ್ಕೇನ್ಗಳಲ್ಲಿ -ಅನೆ ಪ್ರತ್ಯಯವನ್ನು ಬದಲಿಸುವ ಮೂಲಕ ಸಾಮಾನ್ಯವಾಗಿ ಕರೆಯಲಾಗುತ್ತದೆ -ಐಲೀನ್: ಈಥೇನ್ - ಎಥಿಲೀನ್,ಪ್ರೋಪೇನ್ - ಪ್ರೊಪಿಲೀನ್, ಇತ್ಯಾದಿ.
ಮೂಲಕ ವ್ಯವಸ್ಥಿತ ನಾಮಕರಣಎಥಿಲೀನ್ ಹೈಡ್ರೋಕಾರ್ಬನ್ಗಳ ಹೆಸರುಗಳನ್ನು ಅನುಗುಣವಾದ ಆಲ್ಕೇನ್ಗಳಲ್ಲಿ -ane ಪ್ರತ್ಯಯವನ್ನು -ene ಪ್ರತ್ಯಯದೊಂದಿಗೆ ಬದಲಾಯಿಸುವ ಮೂಲಕ ತಯಾರಿಸಲಾಗುತ್ತದೆ (ಆಲ್ಕೇನ್ - ಆಲ್ಕೀನ್, ಈಥೇನ್ - ಈಥೀನ್, ಪ್ರೋಪೇನ್ - ಪ್ರೊಪೀನ್, ಇತ್ಯಾದಿ). ಮುಖ್ಯ ಸರಪಳಿಯ ಆಯ್ಕೆ ಮತ್ತು ಹೆಸರಿಸುವ ಕ್ರಮವು ಆಲ್ಕೇನ್ಗಳಂತೆಯೇ ಇರುತ್ತದೆ. ಆದಾಗ್ಯೂ, ಸರಪಳಿಯು ಅಗತ್ಯವಾಗಿ ಡಬಲ್ ಬಾಂಡ್ ಅನ್ನು ಒಳಗೊಂಡಿರಬೇಕು. ಸರಪಳಿಯ ಸಂಖ್ಯೆಯು ಈ ಸಂಪರ್ಕವು ಹತ್ತಿರವಿರುವ ಅಂತ್ಯದಿಂದ ಪ್ರಾರಂಭವಾಗುತ್ತದೆ. ಉದಾಹರಣೆಗೆ:

ಅಪರ್ಯಾಪ್ತ (ಆಲ್ಕೀನ್) ರಾಡಿಕಲ್ಗಳನ್ನು ಕ್ಷುಲ್ಲಕ ಹೆಸರುಗಳಿಂದ ಅಥವಾ ವ್ಯವಸ್ಥಿತ ನಾಮಕರಣದಿಂದ ಕರೆಯಲಾಗುತ್ತದೆ:
(H 2 C=CH-)ವಿನೈಲ್ ಅಥವಾ ಎಥೆನೈಲ್
(H 2 C=CH-CH 2) ಅಲೈಲ್
ಸಾಮಾನ್ಯ ಸೂತ್ರಆಲ್ಕೀನ್ಗಳು: CnH2n(ಎನ್ 2)
ಆಲ್ಕೀನ್ಗಳ ಏಕರೂಪದ ಸರಣಿಯ ಮೊದಲ ಪ್ರತಿನಿಧಿಗಳು:

ಆಲ್ಕೆನ್ಗಳ ಸೂತ್ರಗಳನ್ನು ಆಲ್ಕೇನ್ಗಳ ಅನುಗುಣವಾದ ಸೂತ್ರಗಳಿಂದ ತಯಾರಿಸಬಹುದು ( ಸ್ಯಾಚುರೇಟೆಡ್ ಹೈಡ್ರೋಕಾರ್ಬನ್ಗಳು) ಆಲ್ಕೇನ್ಗಳ ಹೆಸರುಗಳು ಅನುಗುಣವಾದ ಆಲ್ಕೇನ್ನ ಪ್ರತ್ಯಯವನ್ನು -ene ಅಥವಾ –ylene ನೊಂದಿಗೆ ಬದಲಿಸುವ ಮೂಲಕ ರೂಪುಗೊಳ್ಳುತ್ತವೆ: ಬ್ಯುಟೇನ್ - ಬ್ಯುಟಿಲೀನ್, ಪೆಂಟೇನ್ - ಪೆಂಟೆನ್, ಇತ್ಯಾದಿ. ಡಬಲ್ ಬಾಂಡ್ ಹೊಂದಿರುವ ಕಾರ್ಬನ್ ಪರಮಾಣುವಿನ ಸಂಖ್ಯೆಯನ್ನು ಹೆಸರಿನ ನಂತರ ಅರೇಬಿಕ್ ಅಂಕಿಯಿಂದ ಸೂಚಿಸಲಾಗುತ್ತದೆ.
ಡಬಲ್ ಬಾಂಡ್ ರಚನೆಯಲ್ಲಿ ತೊಡಗಿರುವ ಕಾರ್ಬನ್ ಪರಮಾಣುಗಳು ಎಸ್ಪಿ-ಹೈಬ್ರಿಡೈಸೇಶನ್ ಸ್ಥಿತಿಯಲ್ಲಿವೆ. ಹೈಬ್ರಿಡ್ ಕಕ್ಷೆಗಳಿಂದ ರೂಪುಗೊಂಡ ಮೂರು -ಬಂಧಗಳು ಮತ್ತು ಪರಸ್ಪರ 120 ° ಕೋನದಲ್ಲಿ ಒಂದೇ ಸಮತಲದಲ್ಲಿ ನೆಲೆಗೊಂಡಿವೆ. ಹೈಬ್ರಿಡ್ ಅಲ್ಲದ ಪಿ-ಕಕ್ಷೆಗಳ ಪಾರ್ಶ್ವ ಅತಿಕ್ರಮಣದಿಂದ ಹೆಚ್ಚುವರಿ-ಬಂಧವು ರೂಪುಗೊಳ್ಳುತ್ತದೆ:

C=C ಡಬಲ್ ಬಾಂಡ್ನ ಉದ್ದವು (0.133 nm) ಉದ್ದಕ್ಕಿಂತ ಕಡಿಮೆಯಾಗಿದೆ ಏಕ ಬಂಧ(0.154 nm) ಡಬಲ್ ಬಾಂಡ್ನ ಶಕ್ತಿಯು ಒಂದೇ ಬಂಧದ ಶಕ್ತಿಗಿಂತ ಎರಡು ಪಟ್ಟು ಕಡಿಮೆಯಿರುತ್ತದೆ ಏಕೆಂದರೆ -ಬಂಧದ ಶಕ್ತಿಯು -ಬಂಧದ ಶಕ್ತಿಗಿಂತ ಕಡಿಮೆಯಾಗಿದೆ.
ಆಲ್ಕೀನ್ ಐಸೋಮರ್ಗಳು
ಎಥಿಲೀನ್ ಹೊರತುಪಡಿಸಿ ಎಲ್ಲಾ ಆಲ್ಕೀನ್ಗಳು ಐಸೋಮರ್ಗಳನ್ನು ಹೊಂದಿರುತ್ತವೆ. ಆಲ್ಕೀನ್ಗಳನ್ನು ಇಂಗಾಲದ ಅಸ್ಥಿಪಂಜರದ ಐಸೋಮೆರಿಸಂ, ಡಬಲ್ ಬಾಂಡ್ನ ಸ್ಥಾನದ ಐಸೋಮೆರಿಸಂ, ಇಂಟರ್ಕ್ಲಾಸ್ ಮತ್ತು ಪ್ರಾದೇಶಿಕ ಐಸೋಮೆರಿಸಂ ಮೂಲಕ ನಿರೂಪಿಸಲಾಗಿದೆ.
ಪ್ರೋಪೀನ್ನ ಇಂಟರ್ಕ್ಲಾಸ್ ಐಸೋಮರ್ (C 3 H 6) ಸೈಕ್ಲೋಪ್ರೋಪೇನ್ ಆಗಿದೆ. ಬ್ಯುಟೀನ್ (C 4 H 8) ನಿಂದ ಪ್ರಾರಂಭಿಸಿ, ಐಸೋಮೆರಿಸಂ ಡಬಲ್ ಬಾಂಡ್ (ಬ್ಯುಟೀನ್-1 ಮತ್ತು ಬ್ಯುಟೀನ್-2), ಕಾರ್ಬನ್ ಅಸ್ಥಿಪಂಜರದ ಐಸೋಮೆರಿಸಂ (ಮೀಥೈಲ್ಪ್ರೊಪೀನ್ ಅಥವಾ ಐಸೊಬ್ಯುಟಿಲೀನ್) ಸ್ಥಾನದಲ್ಲಿ ಕಾಣಿಸಿಕೊಳ್ಳುತ್ತದೆ. ಪ್ರಾದೇಶಿಕ ಐಸೋಮೆರಿಸಂ(ಸಿಸ್-ಬ್ಯುಟೀನ್-2 ಮತ್ತು ಟ್ರಾನ್ಸ್-ಬ್ಯೂಟಿನ್-2). ಸಿಸ್ ಐಸೋಮರ್ಗಳಲ್ಲಿ, ಬದಲಿಗಳು ಒಂದು ಬದಿಯಲ್ಲಿವೆ ಮತ್ತು ಟ್ರಾನ್ಸ್ ಐಸೋಮರ್ಗಳಲ್ಲಿ, ಅವು ಡಬಲ್ ಬಾಂಡ್ನ ವಿರುದ್ಧ ಬದಿಗಳಲ್ಲಿವೆ.
ರಾಸಾಯನಿಕ ಗುಣಲಕ್ಷಣಗಳುಮತ್ತು ರಾಸಾಯನಿಕ ಚಟುವಟಿಕೆಆಲ್ಕೀನ್ಗಳನ್ನು ಅವುಗಳ ಅಣುಗಳಲ್ಲಿ ಎರಡು ಬಂಧದ ಉಪಸ್ಥಿತಿಯಿಂದ ನಿರ್ಧರಿಸಲಾಗುತ್ತದೆ. ಆಲ್ಕೀನ್ಗಳಿಗೆ ಅತ್ಯಂತ ಸಾಮಾನ್ಯವಾದ ಪ್ರತಿಕ್ರಿಯೆಗಳು ಎಲೆಕ್ಟ್ರೋಫಿಲಿಕ್ ಸೇರ್ಪಡೆಯಾಗಿದೆ: ಹೈಡ್ರೊಹಾಲೊಜೆನೇಶನ್, ಹೈಡ್ರೇಶನ್, ಹ್ಯಾಲೊಜೆನೇಶನ್, ಹೈಡ್ರೋಜನೀಕರಣ, ಪಾಲಿಮರೀಕರಣ.
ಡಬಲ್ ಬಾಂಡ್ಗೆ ಗುಣಾತ್ಮಕ ಪ್ರತಿಕ್ರಿಯೆ - ಬಣ್ಣ ಬದಲಾವಣೆ ಬ್ರೋಮಿನ್ ನೀರು:
"ಆಲ್ಕೀನ್ಗಳ ಸೂತ್ರ" ವಿಷಯದ ಕುರಿತು ಸಮಸ್ಯೆಗಳನ್ನು ಪರಿಹರಿಸುವ ಉದಾಹರಣೆಗಳು
ಉದಾಹರಣೆ 1
| ವ್ಯಾಯಾಮ | C 3 H 5 Cl ಸಂಯೋಜನೆಯನ್ನು ಹೊಂದಿರುವ ವಸ್ತುವು ಬ್ರೋಮಿನ್ ನೀರನ್ನು ಡಿಕಲರ್ ಮಾಡಲು ಎಷ್ಟು ಐಸೋಮರ್ಗಳನ್ನು ಹೊಂದಿದೆ? ಬರೆಯಿರಿ ರಚನಾತ್ಮಕ ಸೂತ್ರಗಳುಈ ಐಸೋಮರ್ಗಳು |
| ಪರಿಹಾರ | C 3 H 5 Cl ಎಂಬುದು ಹೈಡ್ರೋಕಾರ್ಬನ್ C 3 H 6 ನ ಏಕವರ್ಣದ ಉತ್ಪನ್ನವಾಗಿದೆ. ಈ ಸೂತ್ರವು ಪ್ರೊಪೀನ್, ಒಂದು ಡಬಲ್ ಬಾಂಡ್ ಹೊಂದಿರುವ ಹೈಡ್ರೋಕಾರ್ಬನ್ ಅಥವಾ ಸೈಕ್ಲೋಪ್ರೊಪೇನ್ (ಸೈಕ್ಲಿಕ್ ಹೈಡ್ರೋಕಾರ್ಬನ್) ಗೆ ಅನುರೂಪವಾಗಿದೆ. ಈ ವಸ್ತುಬ್ರೋಮಿನ್ ನೀರನ್ನು ಬಣ್ಣ ಮಾಡುತ್ತದೆ, ಅಂದರೆ ಇದು ಎರಡು ಬಂಧವನ್ನು ಹೊಂದಿರುತ್ತದೆ. ಮೂರು ಕಾರ್ಬನ್ ಪರಮಾಣುಗಳು ಈ ರಚನೆಯನ್ನು ಮಾತ್ರ ರಚಿಸಬಹುದು: ಇಂಗಾಲದ ಅಸ್ಥಿಪಂಜರದ ಐಸೋಮೆರಿಸಂ ಮತ್ತು ಡಬಲ್ ಬಂಧದ ಸ್ಥಾನವು ಅಂತಹ ಸಂಖ್ಯೆಯ ಇಂಗಾಲದ ಪರಮಾಣುಗಳೊಂದಿಗೆ ಅಸಾಧ್ಯವಾಗಿದೆ. ಕೊಟ್ಟಿರುವ ಅಣುವಿನಲ್ಲಿ ರಚನಾತ್ಮಕ ಐಸೋಮೆರಿಸಂ ಎರಡು ಬಂಧಕ್ಕೆ ಸಂಬಂಧಿಸಿದಂತೆ ಕ್ಲೋರಿನ್ ಪರಮಾಣುವಿನ ಸ್ಥಾನದಲ್ಲಿನ ಬದಲಾವಣೆಯಿಂದ ಮಾತ್ರ ಸಾಧ್ಯ: 1-ಕ್ಲೋರೊಪ್ರೊಪಿನ್ಗೆ, ಸಿಸ್-ಟ್ರಾನ್ಸ್ ಐಸೋಮೆರಿಸಂ ಸಾಧ್ಯ: |
| ಉತ್ತರ | ಸಮಸ್ಯೆಯ ಪರಿಸ್ಥಿತಿಗಳನ್ನು 4 ಐಸೋಮರ್ಗಳಿಂದ ತೃಪ್ತಿಪಡಿಸಲಾಗಿದೆ |
ಉದಾಹರಣೆ 2
| ವ್ಯಾಯಾಮ | 11.2 ಲೀ (ಎನ್.ಎಸ್.) ಪರಿಮಾಣದೊಂದಿಗೆ ಐಸೊಮೆರಿಕ್ ಹೈಡ್ರೋಕಾರ್ಬನ್ಗಳ ಮಿಶ್ರಣ (21 ಹೈಡ್ರೋಜನ್ ಸಾಂದ್ರತೆಯೊಂದಿಗೆ) ಬ್ರೋಮಿನ್ ನೀರು. ಫಲಿತಾಂಶವು ಅನುಗುಣವಾದ ಡಿಬ್ರೊಮೊ ಉತ್ಪನ್ನದ 40.4 ಗ್ರಾಂ ಆಗಿತ್ತು. ಈ ಹೈಡ್ರೋಕಾರ್ಬನ್ಗಳು ಯಾವ ರಚನೆಯನ್ನು ಹೊಂದಿವೆ? ಮಿಶ್ರಣದಲ್ಲಿ ಅವುಗಳ ಪರಿಮಾಣದ ವಿಷಯವನ್ನು ನಿರ್ಧರಿಸಿ (% ನಲ್ಲಿ). |
| ಪರಿಹಾರ | ಹೈಡ್ರೋಕಾರ್ಬನ್ಗಳ ಸಾಮಾನ್ಯ ಸೂತ್ರವು C x H y ಆಗಿದೆ. ಹೈಡ್ರೋಕಾರ್ಬನ್ಗಳ ಮೋಲಾರ್ ದ್ರವ್ಯರಾಶಿಯನ್ನು ಲೆಕ್ಕಾಚಾರ ಮಾಡೋಣ: ಆದ್ದರಿಂದ, ಹೈಡ್ರೋಕಾರ್ಬನ್ಗಳ ಸೂತ್ರವು C 3 H 6 ಆಗಿದೆ. ಕೇವಲ ಎರಡು ಪದಾರ್ಥಗಳು ಈ ಸೂತ್ರವನ್ನು ಹೊಂದಿವೆ - ಪ್ರೋಪೇನ್ ಮತ್ತು ಸೈಕ್ಲೋಪ್ರೊಪೇನ್. ಪ್ರೋಪೀನ್ ಮಾತ್ರ ಬ್ರೋಮಿನ್ ನೀರಿನಿಂದ ಪ್ರತಿಕ್ರಿಯಿಸುತ್ತದೆ: ಡಿಬ್ರೊಮೊ ಉತ್ಪನ್ನದ ವಸ್ತುವಿನ ಪ್ರಮಾಣವನ್ನು ಲೆಕ್ಕಾಚಾರ ಮಾಡೋಣ: ಪ್ರತಿಕ್ರಿಯೆ ಸಮೀಕರಣದ ಪ್ರಕಾರ: n (ಪ್ರೋಪೀನ್) ಮೋಲ್ ಮಿಶ್ರಣದಲ್ಲಿನ ಹೈಡ್ರೋಕಾರ್ಬನ್ಗಳ ಒಟ್ಟು ಪ್ರಮಾಣವು ಇದಕ್ಕೆ ಸಮಾನವಾಗಿರುತ್ತದೆ: |
4. ಆಲ್ಕೀನ್ಗಳ ರಾಸಾಯನಿಕ ಗುಣಲಕ್ಷಣಗಳು
ಎಥಿಲೀನ್ನಲ್ಲಿ (146 kcal/mol) ಡಬಲ್ ಕಾರ್ಬನ್-ಇಂಗಾಲದ ಬಂಧದ ಶಕ್ತಿಯು ಈಥೇನ್ನಲ್ಲಿ (2 88 = 176 kcal/mol) ಒಂದೇ C-C ಬಂಧದ ಶಕ್ತಿಗಿಂತ ಎರಡು ಪಟ್ಟು ಕಡಿಮೆಯಿರುತ್ತದೆ. ಎಥಿಲೀನ್ನಲ್ಲಿ ಸಿ-ಸಿ ಬಂಧ ಬಲವಾದ ಸಂಪರ್ಕಗಳುಆದ್ದರಿಂದ, ಎರಡು ಹೊಸ ಸರಳ -ಬಂಧಗಳ ರಚನೆಯೊಂದಿಗೆ -ಬಂಧದ ಸೀಳುವಿಕೆಯೊಂದಿಗೆ ಆಲ್ಕೀನ್ಗಳ ಪ್ರತಿಕ್ರಿಯೆಗಳು ಉಷ್ಣಬಲವಾಗಿ ಅನುಕೂಲಕರ ಪ್ರಕ್ರಿಯೆಯಾಗಿದೆ. ಉದಾಹರಣೆಗೆ, ಅನಿಲ ಹಂತದಲ್ಲಿ, ಲೆಕ್ಕಹಾಕಿದ ಡೇಟಾದ ಪ್ರಕಾರ, ಕೆಳಗಿನ ಎಲ್ಲಾ ಪ್ರತಿಕ್ರಿಯೆಗಳು ಅವುಗಳ ನಿಜವಾದ ಕಾರ್ಯವಿಧಾನವನ್ನು ಲೆಕ್ಕಿಸದೆ ಗಮನಾರ್ಹವಾದ ನಕಾರಾತ್ಮಕ ಎಂಥಾಲ್ಪಿಯೊಂದಿಗೆ ಎಕ್ಸೋಥರ್ಮಿಕ್ ಆಗಿರುತ್ತವೆ.
ಆಣ್ವಿಕ ಕಕ್ಷೆಗಳ ಸಿದ್ಧಾಂತದ ದೃಷ್ಟಿಕೋನದಿಂದ, -ಬಂಧವು -ಬಂಧಕ್ಕಿಂತ ಹೆಚ್ಚು ಪ್ರತಿಕ್ರಿಯಾತ್ಮಕವಾಗಿದೆ ಎಂದು ಸಹ ತೀರ್ಮಾನಿಸಬಹುದು. ಎಥಿಲೀನ್ನ ಆಣ್ವಿಕ ಕಕ್ಷೆಗಳನ್ನು ಪರಿಗಣಿಸೋಣ (ಚಿತ್ರ 2).

ವಾಸ್ತವವಾಗಿ, ಎಥಿಲೀನ್ನ ಬಂಧದ ಕಕ್ಷೆಯು ಹೆಚ್ಚು ಹೊಂದಿದೆ ಹೆಚ್ಚಿನ ಶಕ್ತಿ, ಬಂಧಕ-ಕಕ್ಷೆಗಿಂತ, ಮತ್ತು ಪ್ರತಿಯಾಗಿ, ಎಥಿಲೀನ್ನ ಪ್ರತಿಬಂಧಕ *-ಕಕ್ಷೆಯು C=C ಬಂಧದ ಪ್ರತಿಬಂಧಕ *-ಆರ್ಬಿಟಲ್ನ ಕೆಳಗೆ ಇರುತ್ತದೆ. ಸಾಮಾನ್ಯ ಪರಿಸ್ಥಿತಿಗಳಲ್ಲಿ, ಎಥಿಲೀನ್ನ *- ಮತ್ತು *-ಆರ್ಬಿಟಲ್ಗಳು ಖಾಲಿಯಿರುತ್ತವೆ. ಪರಿಣಾಮವಾಗಿ, ಎಥಿಲೀನ್ ಮತ್ತು ಇತರ ಆಲ್ಕೀನ್ಗಳ ಗಡಿ ಕಕ್ಷೆಗಳು ಅವುಗಳನ್ನು ನಿರ್ಧರಿಸುತ್ತವೆ ಪ್ರತಿಕ್ರಿಯಾತ್ಮಕತೆಕಕ್ಷೆಗಳು ಇರುತ್ತವೆ.
4.1. ಆಲ್ಕೀನ್ಗಳ ವೇಗವರ್ಧಕ ಹೈಡ್ರೋಜನೀಕರಣ
ಎಥಿಲೀನ್ ಮತ್ತು ಇತರ ಆಲ್ಕೀನ್ಗಳ ಹೈಡ್ರೋಜನೀಕರಣವು ಆಲ್ಕೇನ್ಗಳಿಗೆ ಶಾಖದ ಬಿಡುಗಡೆಯೊಂದಿಗೆ ಇರುತ್ತದೆ ಎಂಬ ವಾಸ್ತವದ ಹೊರತಾಗಿಯೂ, ಈ ಪ್ರತಿಕ್ರಿಯೆಯು ಕೆಲವು ವೇಗವರ್ಧಕಗಳ ಉಪಸ್ಥಿತಿಯಲ್ಲಿ ಮಾತ್ರ ಗಮನಾರ್ಹ ದರದಲ್ಲಿ ಸಂಭವಿಸುತ್ತದೆ. ವೇಗವರ್ಧಕ, ವ್ಯಾಖ್ಯಾನದಿಂದ, ಪ್ರತಿಕ್ರಿಯೆಯ ಉಷ್ಣ ಪರಿಣಾಮವನ್ನು ಪರಿಣಾಮ ಬೀರುವುದಿಲ್ಲ, ಮತ್ತು ಅದರ ಪಾತ್ರವನ್ನು ಸಕ್ರಿಯಗೊಳಿಸುವ ಶಕ್ತಿಯನ್ನು ಕಡಿಮೆ ಮಾಡಲು ಕಡಿಮೆಯಾಗುತ್ತದೆ. ಆಲ್ಕೀನ್ಗಳ ವೈವಿಧ್ಯಮಯ ಮತ್ತು ಏಕರೂಪದ ವೇಗವರ್ಧಕ ಹೈಡ್ರೋಜನೀಕರಣದ ನಡುವೆ ವ್ಯತ್ಯಾಸವನ್ನು ಕಂಡುಹಿಡಿಯುವುದು ಅವಶ್ಯಕ. ವೈವಿಧ್ಯಮಯ ಹೈಡ್ರೋಜನೀಕರಣದಲ್ಲಿ, ನುಣ್ಣಗೆ ನೆಲದ ಲೋಹದ ವೇಗವರ್ಧಕಗಳನ್ನು ಬಳಸಲಾಗುತ್ತದೆ - ಪ್ಲಾಟಿನಮ್, ಪಲ್ಲಾಡಿಯಮ್, ರುಥೇನಿಯಮ್, ರೋಡಿಯಮ್, ಆಸ್ಮಿಯಮ್ ಮತ್ತು ನಿಕಲ್, ಅಥವಾ ಶುದ್ಧ ರೂಪ, ಅಥವಾ ಜಡ ವಾಹಕಗಳ ಮೇಲೆ ಠೇವಣಿ ಇಡಲಾಗಿದೆ - BaSO 4, CaCO 3, ಸಕ್ರಿಯ ಇಂಗಾಲ, Al 2 O 3, ಇತ್ಯಾದಿ. ಇವೆಲ್ಲವೂ ಕರಗುವುದಿಲ್ಲ ಸಾವಯವ ಪರಿಸರಗಳುಮತ್ತು ವೈವಿಧ್ಯಮಯ ವೇಗವರ್ಧಕಗಳಾಗಿ ಕಾರ್ಯನಿರ್ವಹಿಸುತ್ತವೆ. ಅವುಗಳಲ್ಲಿ ಅತ್ಯಂತ ಸಕ್ರಿಯವಾದವು ರುಥೇನಿಯಮ್ ಮತ್ತು ರೋಢಿಯಮ್, ಆದರೆ ಪ್ಲಾಟಿನಮ್ ಮತ್ತು ನಿಕಲ್ ಹೆಚ್ಚು ವ್ಯಾಪಕವಾಗಿದೆ. ಪ್ಲಾಟಿನಮ್ ಅನ್ನು ಸಾಮಾನ್ಯವಾಗಿ ಕಪ್ಪು ಡೈಆಕ್ಸೈಡ್ PtO 2 ರೂಪದಲ್ಲಿ ಬಳಸಲಾಗುತ್ತದೆ, ಇದನ್ನು ಸಾಮಾನ್ಯವಾಗಿ ಆಡಮ್ಸ್ ವೇಗವರ್ಧಕ ಎಂದು ಕರೆಯಲಾಗುತ್ತದೆ. ಕ್ಲೋರೊಪ್ಲಾಟಿನಿಕ್ ಆಮ್ಲ H 2 PtCl 6 ಅನ್ನು ಬೆಸೆಯುವ ಮೂಲಕ ಪ್ಲಾಟಿನಂ ಡೈಆಕ್ಸೈಡ್ ಅನ್ನು ಪಡೆಯಲಾಗುತ್ತದೆ. 6H 2 O ಅಥವಾ ಅಮೋನಿಯಂ ಹೆಕ್ಸಾಕ್ಲೋರೋಪ್ಲಾಟಿನೇಟ್ (NH 4) 2 PtCl 6 ಜೊತೆಗೆ ಸೋಡಿಯಂ ನೈಟ್ರೇಟ್. ಆಡಮ್ಸ್ ವೇಗವರ್ಧಕದೊಂದಿಗೆ ಆಲ್ಕೀನ್ಗಳ ಹೈಡ್ರೋಜನೀಕರಣವನ್ನು ಸಾಮಾನ್ಯವಾಗಿ ಸಾಮಾನ್ಯ ಒತ್ತಡದಲ್ಲಿ ಮತ್ತು ಆಲ್ಕೋಹಾಲ್, ಅಸಿಟಿಕ್ ಆಮ್ಲ, ಈಥೈಲ್ ಅಸಿಟೇಟ್ನಲ್ಲಿ 20-50 0 ಸಿ ತಾಪಮಾನದಲ್ಲಿ ನಡೆಸಲಾಗುತ್ತದೆ. ಹೈಡ್ರೋಜನ್ ಅನ್ನು ಹಾದುಹೋದಾಗ, ಪ್ಲಾಟಿನಂ ಡೈಆಕ್ಸೈಡ್ ಅನ್ನು ಪ್ರತಿಕ್ರಿಯೆಯ ಪಾತ್ರೆಯಲ್ಲಿ ನೇರವಾಗಿ ಪ್ಲಾಟಿನಂ ಕಪ್ಪುಗೆ ತಗ್ಗಿಸಲಾಗುತ್ತದೆ, ಇದು ಹೈಡ್ರೋಜನೀಕರಣವನ್ನು ವೇಗವರ್ಧಿಸುತ್ತದೆ. ಇತರ ಹೆಚ್ಚು ಸಕ್ರಿಯವಾಗಿರುವ ಪ್ಲಾಟಿನಂ ಗುಂಪಿನ ಲೋಹಗಳನ್ನು ಜಡ ಬೆಂಬಲಗಳಲ್ಲಿ ಬಳಸಲಾಗುತ್ತದೆ, ಉದಾಹರಣೆಗೆ, Pd/C ಅಥವಾ Pd/BaSO 4, Ru/Al 2 O 3; Rh/C ಇತ್ಯಾದಿ. ನಿಕಲ್ ಅನ್ನು ಸಾಮಾನ್ಯವಾಗಿ "ರಾನಿ ನಿಕಲ್" ಎಂದು ಕರೆಯುವ ರೂಪದಲ್ಲಿ ಬಳಸಲಾಗುತ್ತದೆ. ಈ ವೇಗವರ್ಧಕವನ್ನು ಪಡೆಯಲು, ನಿಕಲ್-ಅಲ್ಯೂಮಿನಿಯಂ ಮಿಶ್ರಲೋಹವನ್ನು ಬಿಸಿ ಜಲೀಯ ಕ್ಷಾರದೊಂದಿಗೆ ಸಂಸ್ಕರಿಸಲಾಗುತ್ತದೆ ಮತ್ತು ಬಹುತೇಕ ಎಲ್ಲಾ ಅಲ್ಯೂಮಿನಿಯಂ ಅನ್ನು ತೆಗೆದುಹಾಕಲಾಗುತ್ತದೆ ಮತ್ತು ನಂತರ ತಟಸ್ಥ ಪ್ರತಿಕ್ರಿಯೆಯವರೆಗೆ ನೀರಿನಿಂದ ಮಾಡಲಾಗುತ್ತದೆ. ವೇಗವರ್ಧಕವು ರಂಧ್ರದ ರಚನೆಯನ್ನು ಹೊಂದಿದೆ ಮತ್ತು ಆದ್ದರಿಂದ ಇದನ್ನು ಅಸ್ಥಿಪಂಜರದ ನಿಕಲ್ ವೇಗವರ್ಧಕ ಎಂದೂ ಕರೆಯುತ್ತಾರೆ. ರಾನಿ ನಿಕಲ್ ಮೇಲಿನ ಆಲ್ಕೀನ್ಗಳ ಹೈಡ್ರೋಜನೀಕರಣಕ್ಕೆ ವಿಶಿಷ್ಟವಾದ ಪರಿಸ್ಥಿತಿಗಳು 5-10 ಎಟಿಎಮ್ ಮತ್ತು 50-100 0 ಸಿ ತಾಪಮಾನದ ಕ್ರಮದ ಒತ್ತಡವನ್ನು ಬಳಸಬೇಕಾಗುತ್ತದೆ, ಅಂದರೆ ಈ ವೇಗವರ್ಧಕವು ಪ್ಲಾಟಿನಮ್ ಗುಂಪಿನ ಲೋಹಗಳಿಗಿಂತ ಕಡಿಮೆ ಸಕ್ರಿಯವಾಗಿದೆ, ಆದರೆ ಇದು ಅಗ್ಗವಾಗಿದೆ. . ಅಸಿಕ್ಲಿಕ್ ಮತ್ತು ಸೈಕ್ಲಿಕ್ ಆಲ್ಕೀನ್ಗಳ ಭಿನ್ನಜಾತಿಯ ವೇಗವರ್ಧಕ ಹೈಡ್ರೋಜನೀಕರಣದ ಕೆಲವು ವಿಶಿಷ್ಟ ಉದಾಹರಣೆಗಳನ್ನು ಕೆಳಗೆ ನೀಡಲಾಗಿದೆ:

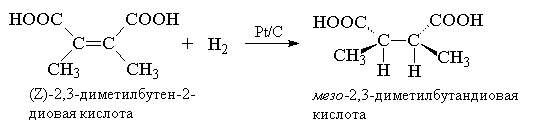
ವೇಗವರ್ಧಕ ಲೋಹದ ಮೇಲ್ಮೈಯಿಂದ ದ್ವಿಬಂಧದ ಕಾರ್ಬನ್ ಪರಮಾಣುಗಳಿಗೆ ಎರಡೂ ಹೈಡ್ರೋಜನ್ ಪರಮಾಣುಗಳನ್ನು ಸೇರಿಸುವುದರಿಂದ, ಸಾಮಾನ್ಯವಾಗಿ ಎರಡು ಬಂಧದ ಒಂದು ಬದಿಯಲ್ಲಿ ಸೇರ್ಪಡೆ ಸಂಭವಿಸುತ್ತದೆ. ಈ ರೀತಿಯ ಸಂಪರ್ಕವನ್ನು ಕರೆಯಲಾಗುತ್ತದೆ ಸಿನ್- ಪ್ರವೇಶ. ಎರಡು ಕಾರಕ ತುಣುಕುಗಳನ್ನು ಒಟ್ಟಿಗೆ ಸೇರಿಸುವ ಸಂದರ್ಭಗಳಲ್ಲಿ ವಿವಿಧ ಕಡೆಬಹು ಬಂಧ (ಡಬಲ್ ಅಥವಾ ಟ್ರಿಪಲ್) ಸಂಭವಿಸುತ್ತದೆ ವಿರೋಧಿ- ಪ್ರವೇಶ. ನಿಯಮಗಳು ಸಿನ್- ಮತ್ತು ವಿರೋಧಿ- ಪದಗಳಿಗೆ ಅರ್ಥದಲ್ಲಿ ಸಮನಾಗಿರುತ್ತದೆ ಸಿಸ್- ಮತ್ತು ಟ್ರಾನ್ಸ್-. ಗೊಂದಲ ಮತ್ತು ನಿಯಮಗಳ ತಪ್ಪುಗ್ರಹಿಕೆಯನ್ನು ತಪ್ಪಿಸಲು ಸಿನ್- ಮತ್ತು ವಿರೋಧಿ- ಸಂಪರ್ಕದ ಪ್ರಕಾರ ಮತ್ತು ನಿಯಮಗಳನ್ನು ಉಲ್ಲೇಖಿಸಿ ಸಿಸ್- ಮತ್ತು ಟ್ರಾನ್ಸ್- ತಲಾಧಾರದ ರಚನೆಗೆ.
ಆಲ್ಕೀನ್ಗಳಲ್ಲಿನ ಡಬಲ್ ಬಾಂಡ್ ಅನೇಕ ಇತರ ಕ್ರಿಯಾತ್ಮಕ ಗುಂಪುಗಳಿಗೆ (C=O, COOR, CN, ಇತ್ಯಾದಿ) ಹೋಲಿಸಿದರೆ ಹೆಚ್ಚಿನ ದರದಲ್ಲಿ ಹೈಡ್ರೋಜನೀಕರಿಸಲ್ಪಟ್ಟಿದೆ ಮತ್ತು ಆದ್ದರಿಂದ ಹೈಡ್ರೋಜನೀಕರಣವನ್ನು ನಡೆಸಿದರೆ C=C ಡಬಲ್ ಬಾಂಡ್ನ ಹೈಡ್ರೋಜನೀಕರಣವು ಸಾಮಾನ್ಯವಾಗಿ ಆಯ್ದ ಪ್ರಕ್ರಿಯೆಯಾಗಿದೆ. ಒಳಗೆ ಸೌಮ್ಯ ಪರಿಸ್ಥಿತಿಗಳು(0-20 0 ಸಿ ಮತ್ತು ನಲ್ಲಿ ವಾತಾವರಣದ ಒತ್ತಡ) ಕೆಲವು ವಿಶಿಷ್ಟ ಉದಾಹರಣೆಗಳನ್ನು ಕೆಳಗೆ ನೀಡಲಾಗಿದೆ:


ಈ ಪರಿಸ್ಥಿತಿಗಳಲ್ಲಿ ಬೆಂಜೀನ್ ರಿಂಗ್ ಕಡಿಮೆಯಾಗುವುದಿಲ್ಲ.
ದೊಡ್ಡ ಮತ್ತು ಪ್ರಮುಖ ಪ್ರಮುಖ ಸಾಧನೆವೇಗವರ್ಧಕ ಹೈಡ್ರೋಜನೀಕರಣದಲ್ಲಿ ಕರಗುವ ಲೋಹದ ಸಂಕೀರ್ಣಗಳ ಆವಿಷ್ಕಾರವಾಗಿದ್ದು ಅದು ಏಕರೂಪದ ದ್ರಾವಣದಲ್ಲಿ ಹೈಡ್ರೋಜನೀಕರಣವನ್ನು ವೇಗವರ್ಧಿಸುತ್ತದೆ. ಲೋಹದ ವೇಗವರ್ಧಕಗಳ ಮೇಲ್ಮೈಯಲ್ಲಿ ವೈವಿಧ್ಯಮಯ ಹೈಡ್ರೋಜನೀಕರಣವು ಹಲವಾರು ಗಮನಾರ್ಹ ಅನಾನುಕೂಲಗಳನ್ನು ಹೊಂದಿದೆ, ಉದಾಹರಣೆಗೆ ಆಲ್ಕೀನ್ಗಳ ಐಸೋಮರೈಸೇಶನ್ ಮತ್ತು ಏಕ ಕಾರ್ಬನ್-ಕಾರ್ಬನ್ ಬಂಧಗಳ ಸೀಳುವಿಕೆ (ಹೈಡ್ರೋಜೆನೊಲಿಸಿಸ್). ಏಕರೂಪದ ಹೈಡ್ರೋಜನೀಕರಣವು ಈ ಅನಾನುಕೂಲಗಳನ್ನು ಹೊಂದಿಲ್ಲ. ಹಿಂದೆ ಹಿಂದಿನ ವರ್ಷಗಳುಏಕರೂಪದ ಹೈಡ್ರೋಜನೀಕರಣ ವೇಗವರ್ಧಕಗಳ ಒಂದು ದೊಡ್ಡ ಗುಂಪು - ವಿವಿಧ ಲಿಗಂಡ್ಗಳನ್ನು ಹೊಂದಿರುವ ಪರಿವರ್ತನೆಯ ಲೋಹದ ಸಂಕೀರ್ಣಗಳು - ಪಡೆಯಲಾಗಿದೆ. ಏಕರೂಪದ ಹೈಡ್ರೋಜನೀಕರಣಕ್ಕೆ ಉತ್ತಮ ವೇಗವರ್ಧಕಗಳು ರೋಡಿಯಮ್ (I) ಮತ್ತು ರುಥೇನಿಯಮ್ (III) ಕ್ಲೋರೈಡ್ಗಳ ಟ್ರಿಫಿನೈಲ್ಫಾಸ್ಫೈನ್ - ಟ್ರಿಸ್ (ಟ್ರಿಫೆನೈಲ್ಫಾಸ್ಫೈನ್) ರೋಡಿಯಮ್ ಕ್ಲೋರೈಡ್ (Ph 3 P) 3 RhCl (ವಿಲ್ಕಿನ್ಸನ್ ವೇಗವರ್ಧಕ) ಮತ್ತು ಟ್ರಿಸ್ (ಟ್ರಿಫಿನೈಲ್ಫಾಸ್ಫಿನ್) (Phiphenylphosphine) ) 3 RuHCl. ರೋಢಿಯಮ್ (III) ಕ್ಲೋರೈಡ್ ಅನ್ನು ಟ್ರಿಫಿನೈಲ್ಫಾಸ್ಫೈನ್ನೊಂದಿಗೆ ಪ್ರತಿಕ್ರಿಯಿಸುವ ಮೂಲಕ ಹೆಚ್ಚು ಪ್ರವೇಶಿಸಬಹುದಾದ ರೋಢಿಯಮ್ ಸಂಕೀರ್ಣವನ್ನು ಪಡೆಯಲಾಗುತ್ತದೆ. ವಿಲ್ಕಿನ್ಸನ್ನ ರೋಢಿಯಮ್ ಸಂಕೀರ್ಣವನ್ನು ಡಬಲ್ ಬಾಂಡ್ ಅನ್ನು ಹೈಡ್ರೋಜನೀಕರಿಸಲು ಬಳಸಲಾಗುತ್ತದೆ ಸಾಮಾನ್ಯ ಪರಿಸ್ಥಿತಿಗಳು.

ಏಕರೂಪದ ವೇಗವರ್ಧಕಗಳ ಒಂದು ಪ್ರಮುಖ ಪ್ರಯೋಜನವೆಂದರೆ ಅವುಗಳ ಹೈಡ್ರೋಜನೀಕರಣದ ದರಗಳಲ್ಲಿನ ದೊಡ್ಡ ವ್ಯತ್ಯಾಸಗಳಿಂದಾಗಿ ಟ್ರೈ- ಮತ್ತು ಟೆಟ್ರಾ-ಬದಲಿ ಡಬಲ್ ಬಾಂಡ್ನ ಉಪಸ್ಥಿತಿಯಲ್ಲಿ ಮೊನೊ- ಅಥವಾ ಡಿಸಬ್ಸ್ಟಿಟ್ಯೂಟೆಡ್ ಡಬಲ್ ಬಾಂಡ್ ಅನ್ನು ಆಯ್ದವಾಗಿ ಕಡಿಮೆ ಮಾಡುವ ಸಾಮರ್ಥ್ಯ.

ಏಕರೂಪದ ವೇಗವರ್ಧಕಗಳ ಸಂದರ್ಭದಲ್ಲಿ, ಹೈಡ್ರೋಜನ್ ಸೇರ್ಪಡೆ ಕೂಡ ಸಂಭವಿಸುತ್ತದೆ ಸಿನ್- ಪ್ರವೇಶ. ಆದ್ದರಿಂದ ಚೇತರಿಕೆ ಸಿಸ್ಈ ಪರಿಸ್ಥಿತಿಗಳಲ್ಲಿ ಡ್ಯೂಟೇರಿಯಂನೊಂದಿಗೆ -ಬ್ಯುಟೀನ್ -2 ಕಾರಣವಾಗುತ್ತದೆ ಮೆಸೊ-2,3-ಡಿಡ್ಯೂಟ್ರೊಬ್ಯುಟೇನ್.

4.2. ಡೈಮೈಡ್ ಬಳಸಿ ಡಬಲ್ ಬಾಂಡ್ನ ಕಡಿತ
ಡೈಮೈಡ್ NH=NH ಅನ್ನು ಬಳಸಿಕೊಂಡು ಅನುಗುಣವಾದ ಆಲ್ಕೇನ್ಗಳಿಗೆ ಆಲ್ಕೀನ್ಗಳ ಕಡಿತವನ್ನು ಯಶಸ್ವಿಯಾಗಿ ಸಾಧಿಸಬಹುದು.
ಡೈಮೈಡ್ ಅನ್ನು ಎರಡು ಮುಖ್ಯ ವಿಧಾನಗಳಿಂದ ಪಡೆಯಲಾಗುತ್ತದೆ: Cu 2+ ಅಯಾನುಗಳ ಉಪಸ್ಥಿತಿಯಲ್ಲಿ ಹೈಡ್ರೋಜನ್ ಪೆರಾಕ್ಸೈಡ್ನೊಂದಿಗೆ ಹೈಡ್ರಾಜಿನ್ ಉತ್ಕರ್ಷಣ ಅಥವಾ Ni-Raney (ಹೈಡ್ರಾಜಿನ್ ಡಿಹೈಡ್ರೋಜನೇಶನ್) ನೊಂದಿಗೆ ಹೈಡ್ರಾಜಿನ್ ಪ್ರತಿಕ್ರಿಯೆ. ಕ್ರಿಯೆಯ ಮಿಶ್ರಣದಲ್ಲಿ ಆಲ್ಕೀನ್ ಇದ್ದರೆ, ಅದರ ದ್ವಿಬಂಧವು ಹೆಚ್ಚು ಅಸ್ಥಿರವಾದ ಡೈಮೈಡ್ನಿಂದ ಹೈಡ್ರೋಜನೀಕರಿಸಲ್ಪಡುತ್ತದೆ. ಈ ವಿಧಾನದ ವಿಶಿಷ್ಟ ಲಕ್ಷಣವೆಂದರೆ ಕಟ್ಟುನಿಟ್ಟಾದ ಸಿನ್- ಪುನಃಸ್ಥಾಪನೆ ಪ್ರಕ್ರಿಯೆಯ ಸ್ಟೀರಿಯೊಸ್ಪೆಸಿಫಿಸಿಟಿ. ಈ ಪ್ರತಿಕ್ರಿಯೆಯು ಬಾಹ್ಯಾಕಾಶದಲ್ಲಿ ಪ್ರತಿಕ್ರಿಯಿಸುವ ಅಣುಗಳ ಕಟ್ಟುನಿಟ್ಟಾದ ದೃಷ್ಟಿಕೋನದೊಂದಿಗೆ ಆವರ್ತಕ ಸಕ್ರಿಯ ಸಂಕೀರ್ಣದ ಮೂಲಕ ಮುಂದುವರಿಯುತ್ತದೆ ಎಂದು ನಂಬಲಾಗಿದೆ.

4.3. ಆಲ್ಕೀನ್ಗಳ ಡಬಲ್ ಬಾಂಡ್ನಲ್ಲಿ ಎಲೆಕ್ಟ್ರೋಫಿಲಿಕ್ ಸೇರ್ಪಡೆ ಪ್ರತಿಕ್ರಿಯೆಗಳು
ಆಲ್ಕೀನ್ಗಳ ಗಡಿ HOMO ಮತ್ತು LUMO ಕಕ್ಷೆಗಳು ಆಕ್ರಮಿತ ಮತ್ತು ಖಾಲಿ * ಕಕ್ಷೆಗಳಾಗಿವೆ. ಪರಿಣಾಮವಾಗಿ, -ಆರ್ಬಿಟಲ್ ಎಲೆಕ್ಟ್ರೋಫೈಲ್ಗಳೊಂದಿಗಿನ ಪ್ರತಿಕ್ರಿಯೆಗಳಲ್ಲಿ (E +) ಭಾಗವಹಿಸುತ್ತದೆ, ಮತ್ತು C=C ಬಂಧದ *-ಆರ್ಬಿಟಲ್ ನ್ಯೂಕ್ಲಿಯೊಫೈಲ್ಗಳೊಂದಿಗಿನ ಪ್ರತಿಕ್ರಿಯೆಗಳಲ್ಲಿ ಭಾಗವಹಿಸುತ್ತದೆ (Nu -) (ಚಿತ್ರ 3 ನೋಡಿ). ಹೆಚ್ಚಿನ ಸಂದರ್ಭಗಳಲ್ಲಿ, ಸರಳ ಆಲ್ಕೀನ್ಗಳು ಎಲೆಕ್ಟ್ರೋಫೈಲ್ಗಳೊಂದಿಗೆ ಸುಲಭವಾಗಿ ಪ್ರತಿಕ್ರಿಯಿಸುತ್ತವೆ, ಆದರೆ ನ್ಯೂಕ್ಲಿಯೊಫೈಲ್ಗಳೊಂದಿಗೆ ಬಹಳ ಕಷ್ಟದಿಂದ ಪ್ರತಿಕ್ರಿಯಿಸುತ್ತವೆ. ಸಾಮಾನ್ಯವಾಗಿ ಹೆಚ್ಚಿನ ಎಲೆಕ್ಟ್ರೋಫೈಲ್ಗಳ LUMO ಶಕ್ತಿಯಲ್ಲಿ ಆಲ್ಕೀನ್ಗಳ -HOMO ಶಕ್ತಿಗೆ ಹತ್ತಿರದಲ್ಲಿದೆ ಎಂಬ ಅಂಶದಿಂದ ಇದನ್ನು ವಿವರಿಸಲಾಗಿದೆ, ಆದರೆ ಹೆಚ್ಚಿನ ನ್ಯೂಕ್ಲಿಯೊಫೈಲ್ಗಳ HOMO ಗಮನಾರ್ಹವಾಗಿ *-LUMO ಗಿಂತ ಕೆಳಗಿರುತ್ತದೆ.

ಕಠಿಣ ಪರಿಸ್ಥಿತಿಗಳಲ್ಲಿ ಸರಳವಾದ ಆಲ್ಕೀನ್ಗಳು ಬಲವಾದ ನ್ಯೂಕ್ಲಿಯೊಫಿಲಿಕ್ ಏಜೆಂಟ್ಗಳೊಂದಿಗೆ (ಕಾರ್ಬನಿಯನ್ಗಳು) ಮಾತ್ರ ಪ್ರತಿಕ್ರಿಯಿಸುತ್ತವೆ, ಆದಾಗ್ಯೂ, ಎಲೆಕ್ಟ್ರಾನ್-ಹಿಂತೆಗೆದುಕೊಳ್ಳುವ ಗುಂಪುಗಳನ್ನು ಆಲ್ಕೀನ್ಗಳಾಗಿ ಪರಿಚಯಿಸುವುದು, ಉದಾಹರಣೆಗೆ, NO 2, COR, ಇತ್ಯಾದಿ, * ಮಟ್ಟದಲ್ಲಿ ಇಳಿಕೆಗೆ ಕಾರಣವಾಗುತ್ತದೆ. ಆಲ್ಕೀನ್ ಸರಾಸರಿ ಶಕ್ತಿಯ ನ್ಯೂಕ್ಲಿಯೊಫೈಲ್ಗಳೊಂದಿಗೆ ಪ್ರತಿಕ್ರಿಯಿಸುವ ಸಾಮರ್ಥ್ಯವನ್ನು ಪಡೆಯುತ್ತದೆ (ಅಮೋನಿಯಾ, RO - , Nє C - , ಎನೋಲೇಟ್ ಅಯಾನ್, ಇತ್ಯಾದಿ).
ಆಲ್ಕೀನ್ನೊಂದಿಗೆ ಎಲೆಕ್ಟ್ರೋಫಿಲಿಕ್ ಏಜೆಂಟ್ E + ನ ಪರಸ್ಪರ ಕ್ರಿಯೆಯ ಪರಿಣಾಮವಾಗಿ, ಕಾರ್ಬೋಕೇಶನ್ ರಚನೆಯಾಗುತ್ತದೆ, ಇದು ಹೆಚ್ಚು ಪ್ರತಿಕ್ರಿಯಾತ್ಮಕವಾಗಿರುತ್ತದೆ. ನ್ಯೂಕ್ಲಿಯೊಫಿಲಿಕ್ ಏಜೆಂಟ್ ನು ಕ್ಷಿಪ್ರ ಸೇರ್ಪಡೆಯಿಂದ ಕಾರ್ಬೋಕೇಶನ್ ಮತ್ತಷ್ಟು ಸ್ಥಿರಗೊಳ್ಳುತ್ತದೆ - :


ನಿಧಾನ ಹಂತವು ಎಲೆಕ್ಟ್ರೋಫೈಲ್ನ ಸೇರ್ಪಡೆಯಾಗಿರುವುದರಿಂದ, ಯಾವುದೇ ಧ್ರುವೀಯ ಏಜೆಂಟ್ ಇ + ನು - ಅನ್ನು ಸೇರಿಸುವ ಪ್ರಕ್ರಿಯೆಯು ಆಲ್ಕೀನ್ನ ಬಹು ಬಂಧಕ್ಕೆ ಎಲೆಕ್ಟ್ರೋಫಿಲಿಕ್ ಸೇರ್ಪಡೆ ಎಂದು ನಿಖರವಾಗಿ ಪರಿಗಣಿಸಬೇಕು. ಈ ಪ್ರಕಾರದ ಹೆಚ್ಚಿನ ಸಂಖ್ಯೆಯ ಪ್ರತಿಕ್ರಿಯೆಗಳು ತಿಳಿದಿವೆ, ಅಲ್ಲಿ ಎಲೆಕ್ಟ್ರೋಫಿಲಿಕ್ ಏಜೆಂಟ್ನ ಪಾತ್ರವನ್ನು ಹ್ಯಾಲೊಜೆನ್ಗಳು, ಹೈಡ್ರೋಜನ್ ಹಾಲೈಡ್ಗಳು, ನೀರು, ಡೈವಲೆಂಟ್ ಪಾದರಸ ಲವಣಗಳು ಮತ್ತು ಇತರ ಧ್ರುವ ಕಾರಕಗಳಿಂದ ಆಡಲಾಗುತ್ತದೆ. ಕಾರ್ಯವಿಧಾನಗಳ ವರ್ಗೀಕರಣದಲ್ಲಿ ಡಬಲ್ ಬಾಂಡ್ಗೆ ಎಲೆಕ್ಟ್ರೋಫಿಲಿಕ್ ಸೇರ್ಪಡೆ ಸಾವಯವ ಪ್ರತಿಕ್ರಿಯೆಗಳುಜಾಹೀರಾತು E ಚಿಹ್ನೆಯನ್ನು ಹೊಂದಿದೆ ( ಜೊತೆಗೆ ಎಲೆಕ್ಟ್ರೋಫಿಲಿಕ್) ಮತ್ತು, ಪ್ರತಿಕ್ರಿಯಿಸುವ ಅಣುಗಳ ಸಂಖ್ಯೆಯನ್ನು ಅವಲಂಬಿಸಿ, Ad E 2 (ದ್ವಿಅಣು ಪ್ರತಿಕ್ರಿಯೆ) ಅಥವಾ Ad E 3 (ಟ್ರಿಮೋಲಿಕ್ಯುಲರ್ ಪ್ರತಿಕ್ರಿಯೆ) ಎಂದು ಗೊತ್ತುಪಡಿಸಲಾಗುತ್ತದೆ.
4.3.a ಹ್ಯಾಲೊಜೆನ್ಗಳ ಸೇರ್ಪಡೆ
ಆಲ್ಕೀನ್ಗಳು ಬ್ರೋಮಿನ್ ಮತ್ತು ಕ್ಲೋರಿನ್ನೊಂದಿಗೆ ಪ್ರತಿಕ್ರಿಯಿಸಿ ಒಂದು ಹ್ಯಾಲೊಜೆನ್ ಅಣುವಿನ ಎರಡು ಬಂಧದಲ್ಲಿ ಸಂಕಲನ ಉತ್ಪನ್ನಗಳನ್ನು ರೂಪಿಸಲು ಪರಿಮಾಣಾತ್ಮಕತೆಗೆ ಹತ್ತಿರವಾದ ಇಳುವರಿಯೊಂದಿಗೆ. ಫ್ಲೋರಿನ್ ತುಂಬಾ ಸಕ್ರಿಯವಾಗಿದೆ ಮತ್ತು ಆಲ್ಕೀನ್ಗಳ ನಾಶಕ್ಕೆ ಕಾರಣವಾಗುತ್ತದೆ. ಹೆಚ್ಚಿನ ಸಂದರ್ಭಗಳಲ್ಲಿ ಆಲ್ಕೀನ್ಗಳಿಗೆ ಅಯೋಡಿನ್ ಸೇರ್ಪಡೆಯಾಗಿದೆ ಹಿಂತಿರುಗಿಸಬಹುದಾದ ಪ್ರತಿಕ್ರಿಯೆ, ಇದರ ಸಮತೋಲನವನ್ನು ಮೂಲ ಕಾರಕಗಳ ಕಡೆಗೆ ವರ್ಗಾಯಿಸಲಾಗುತ್ತದೆ.


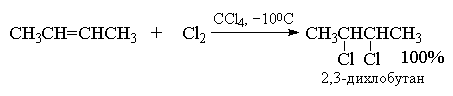
CCL4 ನಲ್ಲಿನ ಬ್ರೋಮಿನ್ ದ್ರಾವಣದ ಕ್ಷಿಪ್ರ ಬಣ್ಣ ತೆಗೆಯುವಿಕೆಯು ಅಪರ್ಯಾಪ್ತತೆಗೆ ಸರಳವಾದ ಪರೀಕ್ಷೆಗಳಲ್ಲಿ ಒಂದಾಗಿದೆ, ಏಕೆಂದರೆ ಆಲ್ಕೀನ್ಗಳು, ಆಲ್ಕೈನ್ಗಳು ಮತ್ತು ಡೈನ್ಗಳು ಬ್ರೋಮಿನ್ನೊಂದಿಗೆ ತ್ವರಿತವಾಗಿ ಪ್ರತಿಕ್ರಿಯಿಸುತ್ತವೆ.
ಆಲ್ಕೀನ್ಗಳಿಗೆ ಬ್ರೋಮಿನ್ ಮತ್ತು ಕ್ಲೋರಿನ್ನ ಸೇರ್ಪಡೆಯು ಆಮೂಲಾಗ್ರ ಕಾರ್ಯವಿಧಾನಕ್ಕಿಂತ ಅಯಾನಿಕ್ನಿಂದ ಸಂಭವಿಸುತ್ತದೆ. ಹ್ಯಾಲೊಜೆನ್ ಸೇರ್ಪಡೆಯ ದರವು ವಿಕಿರಣ, ಆಮ್ಲಜನಕದ ಉಪಸ್ಥಿತಿ ಮತ್ತು ಮೂಲಭೂತ ಪ್ರಕ್ರಿಯೆಗಳನ್ನು ಪ್ರಾರಂಭಿಸುವ ಅಥವಾ ಪ್ರತಿಬಂಧಿಸುವ ಇತರ ಕಾರಕಗಳ ಮೇಲೆ ಅವಲಂಬಿತವಾಗಿಲ್ಲ ಎಂಬ ಅಂಶದಿಂದ ಈ ತೀರ್ಮಾನವು ಅನುಸರಿಸುತ್ತದೆ. ಹೆಚ್ಚಿನ ಸಂಖ್ಯೆಯ ಪ್ರಾಯೋಗಿಕ ದತ್ತಾಂಶವನ್ನು ಆಧರಿಸಿ, ಹಲವಾರು ಅನುಕ್ರಮ ಹಂತಗಳನ್ನು ಒಳಗೊಂಡಂತೆ ಈ ಪ್ರತಿಕ್ರಿಯೆಗೆ ಕಾರ್ಯವಿಧಾನವನ್ನು ಪ್ರಸ್ತಾಪಿಸಲಾಗಿದೆ. ಮೊದಲ ಹಂತದಲ್ಲಿ, ಹ್ಯಾಲೊಜೆನ್ ಅಣುವಿನ ಧ್ರುವೀಕರಣವು ಎಲೆಕ್ಟ್ರಾನ್ಗಳನ್ನು ಬಂಧಿಸುವ ಕ್ರಿಯೆಯ ಅಡಿಯಲ್ಲಿ ಸಂಭವಿಸುತ್ತದೆ. ಹ್ಯಾಲೊಜೆನ್ ಪರಮಾಣು, ಒಂದು ನಿರ್ದಿಷ್ಟ ಭಾಗಶಃ ಧನಾತ್ಮಕ ಆವೇಶವನ್ನು ಪಡೆದುಕೊಳ್ಳುತ್ತದೆ, -ಬಂಧದ ಎಲೆಕ್ಟ್ರಾನ್ಗಳೊಂದಿಗೆ ಅಸ್ಥಿರ ಮಧ್ಯಂತರವನ್ನು ರೂಪಿಸುತ್ತದೆ, ಇದನ್ನು -ಕಾಂಪ್ಲೆಕ್ಸ್ ಅಥವಾ ಚಾರ್ಜ್ ಟ್ರಾನ್ಸ್ಫರ್ ಕಾಂಪ್ಲೆಕ್ಸ್ ಎಂದು ಕರೆಯಲಾಗುತ್ತದೆ. ಸಂಕೀರ್ಣದಲ್ಲಿ ಹ್ಯಾಲೊಜೆನ್ ಯಾವುದೇ ನಿರ್ದಿಷ್ಟ ಇಂಗಾಲದ ಪರಮಾಣುವಿನೊಂದಿಗೆ ನಿರ್ದೇಶಿತ ಬಂಧವನ್ನು ರೂಪಿಸುವುದಿಲ್ಲ ಎಂದು ಗಮನಿಸಬೇಕು; ಈ ಸಂಕೀರ್ಣದಲ್ಲಿ, ಎಲೆಕ್ಟ್ರಾನ್ ಜೋಡಿಯ ದಾನಿ-ಸ್ವೀಕರಿಸುವ ಪರಸ್ಪರ ಕ್ರಿಯೆ - ದಾನಿಯಾಗಿ ಬಂಧ ಮತ್ತು ಸ್ವೀಕಾರಕವಾಗಿ ಹ್ಯಾಲೊಜೆನ್ ಅನ್ನು ಸರಳವಾಗಿ ಅರಿತುಕೊಳ್ಳಲಾಗುತ್ತದೆ.

ಮುಂದೆ, ಕಾಂಪ್ಲೆಕ್ಸ್ ಆವರ್ತಕ ಬ್ರೋಮೋನಿಯಮ್ ಅಯಾನ್ ಆಗಿ ರೂಪಾಂತರಗೊಳ್ಳುತ್ತದೆ. ಈ ಆವರ್ತಕ ಕ್ಯಾಷನ್ ರಚನೆಯ ಸಮಯದಲ್ಲಿ, ಹೆಟೆರೊಲೈಟಿಕ್ ಸೀಳು ಸಂಭವಿಸುತ್ತದೆ Br-Br ಬಾಂಡ್ಗಳುಮತ್ತು ಖಾಲಿ ಆರ್ಹೈಬ್ರಿಡೈಸ್ಡ್ ಇಂಗಾಲದ ಪರಮಾಣುವಿನ sp 2 ಕಕ್ಷೆಯು ಇದರೊಂದಿಗೆ ಅತಿಕ್ರಮಿಸುತ್ತದೆ ಆರ್ಹ್ಯಾಲೊಜೆನ್ ಪರಮಾಣುವಿನ ಎಲೆಕ್ಟ್ರಾನ್ಗಳ "ಒಂಟಿ ಜೋಡಿ" ಕಕ್ಷೆಯು ಆವರ್ತಕ ಬ್ರೋಮೋನಿಯಮ್ ಅಯಾನನ್ನು ರೂಪಿಸುತ್ತದೆ.

ಕೊನೆಯ, ಮೂರನೇ ಹಂತದಲ್ಲಿ, ಬ್ರೋಮಿನ್ ಅಯಾನ್, ನ್ಯೂಕ್ಲಿಯೊಫಿಲಿಕ್ ಏಜೆಂಟ್ ಆಗಿ, ಬ್ರೋಮೋನಿಯಮ್ ಅಯಾನಿನ ಕಾರ್ಬನ್ ಪರಮಾಣುಗಳಲ್ಲಿ ಒಂದನ್ನು ಆಕ್ರಮಿಸುತ್ತದೆ. ಬ್ರೋಮೈಡ್ ಅಯಾನಿನ ನ್ಯೂಕ್ಲಿಯೊಫಿಲಿಕ್ ದಾಳಿಯು ಮೂರು-ಸದಸ್ಯರ ಉಂಗುರವನ್ನು ತೆರೆಯಲು ಮತ್ತು ವಿಸಿನಲ್ ಡೈಬ್ರೊಮೈಡ್ ರಚನೆಗೆ ಕಾರಣವಾಗುತ್ತದೆ ( ವಿಕ್- ಹತ್ತಿರ). ಈ ಹಂತವನ್ನು ಔಪಚಾರಿಕವಾಗಿ ಕಾರ್ಬನ್ ಪರಮಾಣುವಿನಲ್ಲಿ SN 2 ನ ನ್ಯೂಕ್ಲಿಯೊಫಿಲಿಕ್ ಪರ್ಯಾಯವಾಗಿ ಪರಿಗಣಿಸಬಹುದು, ಅಲ್ಲಿ ಹೊರಹೋಗುವ ಗುಂಪು Br+ ಆಗಿದೆ.
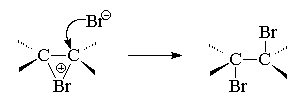
ಆಲ್ಕೀನ್ಗಳ ಡಬಲ್ ಬಾಂಡ್ಗೆ ಹ್ಯಾಲೊಜೆನ್ಗಳನ್ನು ಸೇರಿಸುವುದು ಔಪಚಾರಿಕವಾಗಿ ಸರಳವಾದ ಮಾದರಿ ಪ್ರತಿಕ್ರಿಯೆಗಳಲ್ಲಿ ಒಂದಾಗಿದೆ, ಇದರ ಉದಾಹರಣೆಯನ್ನು ಬಳಸಿಕೊಂಡು ಪ್ರಕ್ರಿಯೆಯ ವಿವರವಾದ ಕಾರ್ಯವಿಧಾನದ ಬಗ್ಗೆ ತರ್ಕಬದ್ಧ ತೀರ್ಮಾನಗಳನ್ನು ತೆಗೆದುಕೊಳ್ಳಲು ಅನುವು ಮಾಡಿಕೊಡುವ ಮುಖ್ಯ ಅಂಶಗಳ ಪ್ರಭಾವವನ್ನು ಪರಿಗಣಿಸಬಹುದು. ಯಾವುದೇ ಪ್ರತಿಕ್ರಿಯೆಯ ಕಾರ್ಯವಿಧಾನದ ಬಗ್ಗೆ ತಿಳುವಳಿಕೆಯುಳ್ಳ ತೀರ್ಮಾನಗಳನ್ನು ಮಾಡಲು, ನೀವು ಡೇಟಾವನ್ನು ಹೊಂದಿರಬೇಕು: 1) ಪ್ರತಿಕ್ರಿಯೆ ಚಲನಶಾಸ್ತ್ರ; 2) ಸ್ಟೀರಿಯೊಕೆಮಿಸ್ಟ್ರಿ (ಪ್ರತಿಕ್ರಿಯೆಯ ಸ್ಟೀರಿಯೊಕೆಮಿಕಲ್ ಫಲಿತಾಂಶ); 3) ಸಂಬಂಧಿತ, ಸ್ಪರ್ಧಾತ್ಮಕ ಪ್ರಕ್ರಿಯೆಯ ಉಪಸ್ಥಿತಿ ಅಥವಾ ಅನುಪಸ್ಥಿತಿ; 4) ಪ್ರತಿಕ್ರಿಯೆ ದರದ ಮೇಲೆ ಮೂಲ ತಲಾಧಾರದಲ್ಲಿ ಬದಲಿಗಳ ಪ್ರಭಾವ; 5) ಲೇಬಲ್ ಮಾಡಲಾದ ತಲಾಧಾರಗಳು ಮತ್ತು (ಅಥವಾ) ಕಾರಕಗಳ ಬಳಕೆ; 6) ಪ್ರತಿಕ್ರಿಯೆಯ ಸಮಯದಲ್ಲಿ ಮರುಜೋಡಣೆಗಳ ಸಾಧ್ಯತೆ; 7) ಪ್ರತಿಕ್ರಿಯೆ ದರದ ಮೇಲೆ ದ್ರಾವಕದ ಪರಿಣಾಮ.
ಆಲ್ಕೀನ್ಗಳ ಹ್ಯಾಲೊಜೆನೇಶನ್ನ ಉದಾಹರಣೆಯನ್ನು ಬಳಸಿಕೊಂಡು ನಾವು ಈ ಅಂಶಗಳನ್ನು ಪರಿಗಣಿಸೋಣ. ಚಲನಶಾಸ್ತ್ರದ ದತ್ತಾಂಶವು ಪ್ರತಿ ಘಟಕಕ್ಕೆ ಪ್ರತಿಕ್ರಿಯೆಯ ಕ್ರಮವನ್ನು ಸ್ಥಾಪಿಸಲು ಸಾಧ್ಯವಾಗಿಸುತ್ತದೆ ಮತ್ತು ಈ ಆಧಾರದ ಮೇಲೆ, ಪ್ರತಿಕ್ರಿಯೆಯ ಒಟ್ಟಾರೆ ಆಣ್ವಿಕತೆಯ ಬಗ್ಗೆ ತೀರ್ಮಾನವನ್ನು ತೆಗೆದುಕೊಳ್ಳಿ, ಅಂದರೆ, ಪ್ರತಿಕ್ರಿಯಿಸುವ ಅಣುಗಳ ಸಂಖ್ಯೆ.
ಆಲ್ಕೀನ್ಗಳ ಬ್ರೋಮಿನೇಷನ್ಗಾಗಿ, ಪ್ರತಿಕ್ರಿಯೆ ದರವನ್ನು ಸಾಮಾನ್ಯವಾಗಿ ಈ ಕೆಳಗಿನ ಸಮೀಕರಣದಿಂದ ವಿವರಿಸಲಾಗುತ್ತದೆ:
v = k`[ಆಲ್ಕೀನ್] + k``[ಆಲ್ಕೀನ್] 2,
ಇದರಲ್ಲಿ ಅಪರೂಪದ ಸಂದರ್ಭಗಳಲ್ಲಿಗೆ ಸರಳಗೊಳಿಸುತ್ತದೆ
v = k`[ಆಲ್ಕೀನ್].
ಚಲನಾ ದತ್ತಾಂಶದ ಆಧಾರದ ಮೇಲೆ, ಒಂದು ಅಥವಾ ಎರಡು ಬ್ರೋಮಿನ್ ಅಣುಗಳು ದರ-ನಿರ್ಧರಿಸುವ ಹಂತದಲ್ಲಿ ತೊಡಗಿಕೊಂಡಿವೆ ಎಂದು ತೀರ್ಮಾನಿಸಬಹುದು. ಬ್ರೋಮಿನ್ನಲ್ಲಿನ ಎರಡನೇ ಕ್ರಮವೆಂದರೆ ಅದು ಬ್ರೋಮೈಡ್ ಅಯಾನು Br ಅಲ್ಲ - ಅದು ಬ್ರೋಮೋನಿಯಮ್ ಅಯಾನುಗಳೊಂದಿಗೆ ಪ್ರತಿಕ್ರಿಯಿಸುತ್ತದೆ, ಆದರೆ ಬ್ರೋಮಿನ್ ಮತ್ತು ಬ್ರೋಮೈಡ್ ಅಯಾನುಗಳ ಪರಸ್ಪರ ಕ್ರಿಯೆಯಿಂದ ರೂಪುಗೊಂಡ ಟ್ರೈಬ್ರೋಮೈಡ್ ಅಯಾನು:
![]()
ಈ ಸಮತೋಲನವನ್ನು ಬಲಕ್ಕೆ ವರ್ಗಾಯಿಸಲಾಗಿದೆ. ಚಲನಶಾಸ್ತ್ರದ ಡೇಟಾವು ರಚನೆಯ ಬಗ್ಗೆ ಯಾವುದೇ ಇತರ ತೀರ್ಮಾನಗಳನ್ನು ಅನುಮತಿಸುವುದಿಲ್ಲ ಪರಿವರ್ತನೆಯ ಸ್ಥಿತಿಮತ್ತು ಡಬಲ್ ಬಾಂಡ್ನಲ್ಲಿ ಹ್ಯಾಲೊಜೆನ್ ಸೇರ್ಪಡೆಯ ಪ್ರತಿಕ್ರಿಯೆಯಲ್ಲಿ ಎಲೆಕ್ಟ್ರೋಫಿಲಿಕ್ ಕಣದ ಸ್ವರೂಪ. ಈ ಕ್ರಿಯೆಯ ಕಾರ್ಯವಿಧಾನದ ಬಗ್ಗೆ ಅತ್ಯಮೂಲ್ಯವಾದ ಮಾಹಿತಿಯನ್ನು ಸೇರ್ಪಡೆಯ ಸ್ಟೀರಿಯೊಕೆಮಿಸ್ಟ್ರಿಯ ಡೇಟಾದಿಂದ ಒದಗಿಸಲಾಗಿದೆ. ಡಬಲ್ ಬಾಂಡ್ಗೆ ಹ್ಯಾಲೊಜೆನ್ ಅನ್ನು ಸೇರಿಸುವುದು ಸ್ಟೀರಿಯೊಸ್ಪೆಸಿಫಿಕ್ ಪ್ರಕ್ರಿಯೆಯಾಗಿದೆ (ಒಂದು ಪ್ರಕ್ರಿಯೆಯಲ್ಲಿ ಸಂಭವನೀಯ ಸ್ಟೀರಿಯೊಐಸೋಮರ್ಗಳಲ್ಲಿ ಒಂದನ್ನು ಮಾತ್ರ ರಚಿಸಲಾಗುತ್ತದೆ; ಸ್ಟೀರಿಯೊಸೆಲೆಕ್ಟಿವ್ ಪ್ರಕ್ರಿಯೆಯಲ್ಲಿ, ಒಂದು ಸ್ಟೀರಿಯೊಮರ್ನ ಆದ್ಯತೆಯ ರಚನೆಯನ್ನು ಗಮನಿಸಬಹುದು) ವಿರೋಧಿಆಲ್ಕೀನ್ಗಳು ಮತ್ತು ಸೈಕ್ಲೋಆಲ್ಕೀನ್ಗಳಿಗೆ ಸೇರ್ಪಡೆಗಳು, ಇದರಲ್ಲಿ ಡಬಲ್ ಬಂಧವು ಸಂಯೋಜಿತವಾಗಿಲ್ಲ ಬೆಂಜೀನ್ ಉಂಗುರ. ಫಾರ್ ಸಿಸ್- ಮತ್ತು ಟ್ರಾನ್ಸ್-ಬ್ಯುಟೀನ್-2, ಪೆಂಟೆನ್-2, ಹೆಕ್ಸೇನ್-3, ಸೈಕ್ಲೋಹೆಕ್ಸೇನ್, ಸೈಕ್ಲೋಪೆಂಟೀನ್ ಮತ್ತು ಇತರ ಆಲ್ಕೀನ್ಗಳ ಐಸೋಮರ್ಗಳು, ಬ್ರೋಮಿನ್ ಸೇರ್ಪಡೆಯು ಪ್ರತ್ಯೇಕವಾಗಿ ಸಂಭವಿಸುತ್ತದೆ ವಿರೋಧಿ- ಪ್ರವೇಶ. ಈ ಸಂದರ್ಭದಲ್ಲಿ, ಸೈಕ್ಲೋಹೆಕ್ಸೆನ್ ಸಂದರ್ಭದಲ್ಲಿ, ಮಾತ್ರ ಟ್ರಾನ್ಸ್-1,2-ಡೈಬ್ರೊಮೊಸೈಕ್ಲೋಹೆಕ್ಸೇನ್ (ಎನ್ಯಾಂಟಿಯೋಮರ್ಗಳ ಮಿಶ್ರಣ).

1,2-ಡೈಬ್ರೊಮೊಸೈಕ್ಲೋಹೆಕ್ಸೇನ್ನಲ್ಲಿನ ಬ್ರೋಮಿನ್ ಪರಮಾಣುಗಳ ಟ್ರಾನ್ಸ್ ವ್ಯವಸ್ಥೆಯು ಸೈಕ್ಲೋಹೆಕ್ಸೇನ್ ರಿಂಗ್ನ ಸರಾಸರಿ ಸಮತಲಕ್ಕೆ (ಗಣನೆಗೆ ತೆಗೆದುಕೊಳ್ಳದೆಯೇ) ಹೋಲಿಸಿದರೆ ಸರಳೀಕೃತ ರೀತಿಯಲ್ಲಿ ಚಿತ್ರಿಸಬಹುದು. ಹೊಂದಾಣಿಕೆಗಳು):
ಬ್ರೋಮಿನ್ ಸೈಕ್ಲೋಹೆಕ್ಸೆನ್ನೊಂದಿಗೆ ಸಂಯೋಜಿಸಿದಾಗ, ಅದು ಆರಂಭದಲ್ಲಿ ರೂಪುಗೊಳ್ಳುತ್ತದೆ ಟ್ರಾನ್ಸ್-1,2-ಡೈಬ್ರೊಮೊಸೈಕ್ಲೋಹೆಕ್ಸೇನ್ ಇನ್ a,a-ಅನುರೂಪತೆ, ಇದು ತಕ್ಷಣವೇ ಶಕ್ತಿಯುತವಾಗಿ ಹೆಚ್ಚು ಅನುಕೂಲಕರವಾಗಿ ರೂಪಾಂತರಗೊಳ್ಳುತ್ತದೆ ಅವಳು- ಹೊಂದಾಣಿಕೆ. ವಿರೋಧಿಡಬಲ್ ಬಾಂಡ್ಗೆ ಹ್ಯಾಲೊಜೆನ್ಗಳ ಸೇರ್ಪಡೆಯು ಒಂದು ಹ್ಯಾಲೊಜೆನ್ ಅಣುವಿನ ಒಂದು ಹಂತದ ಸಿಂಕ್ರೊನಸ್ ಸೇರ್ಪಡೆಯ ಕಾರ್ಯವಿಧಾನವನ್ನು ಎರಡು ಬಂಧಕ್ಕೆ ತಿರಸ್ಕರಿಸಲು ನಮಗೆ ಅನುಮತಿಸುತ್ತದೆ, ಇದು ಕೇವಲ ಸಂಭವಿಸಬಹುದು ಸಿನ್- ಪ್ರವೇಶ. ವಿರೋಧಿ-ಒಂದು ಹ್ಯಾಲೊಜೆನ್ನ ಸೇರ್ಪಡೆಯು ತೆರೆದ ಕಾರ್ಬೋಕೇಶನ್ RCH + -CH 2 Hal ಅನ್ನು ಮಧ್ಯಂತರವಾಗಿ ರೂಪಿಸುವುದರೊಂದಿಗೆ ಅಸಮಂಜಸವಾಗಿದೆ. ತೆರೆದ ಕಾರ್ಬೋಕೇಶನ್ನಲ್ಲಿ, C-C ಬಂಧದ ಸುತ್ತ ಮುಕ್ತ ತಿರುಗುವಿಕೆ ಸಾಧ್ಯ, ಇದು Br ಅಯಾನ್ನ ದಾಳಿಗೆ ಕಾರಣವಾಗುತ್ತದೆ - ಉತ್ಪನ್ನಗಳ ಮಿಶ್ರಣದ ರಚನೆಗೆ ವಿರೋಧಿ- ಮತ್ತು ಆದ್ದರಿಂದ ಸಿನ್- ಪ್ರವೇಶಗಳು. ಸ್ಟಿರಿಯೊಸ್ಪೆಸಿಫಿಕ್ ವಿರೋಧಿ- ಹ್ಯಾಲೊಜೆನ್ಗಳ ಸೇರ್ಪಡೆಯಾಗಿತ್ತು ಮುಖ್ಯ ಕಾರಣಬ್ರೋಮೋನಿಯಮ್ ಅಥವಾ ಕ್ಲೋರೋನಿಯಮ್ ಅಯಾನುಗಳ ಪರಿಕಲ್ಪನೆಯನ್ನು ಪ್ರತ್ಯೇಕ ಮಧ್ಯಂತರ ಜಾತಿಗಳಾಗಿ ರಚಿಸುವುದು. ಈ ಪರಿಕಲ್ಪನೆಯು ನಿಯಮವನ್ನು ಸಂಪೂರ್ಣವಾಗಿ ಪೂರೈಸುತ್ತದೆ ವಿರೋಧಿ-ಜೊತೆಗೆ, ಹ್ಯಾಲೈಡ್ ಅಯಾನಿನ ನ್ಯೂಕ್ಲಿಯೊಫಿಲಿಕ್ ದಾಳಿಯು ಸಾಧ್ಯವಿರುವುದರಿಂದ ವಿರೋಧಿ-S N 2 ಯಾಂತ್ರಿಕತೆಯ ಮೂಲಕ ಹಾಲೈಡ್ ಅಯಾನಿನ ಎರಡು ಇಂಗಾಲದ ಪರಮಾಣುಗಳಲ್ಲಿ ಯಾವುದಾದರೂ ಒಂದು ಬದಿಯಲ್ಲಿ.

ಅಸಮಪಾರ್ಶ್ವದ ಪರ್ಯಾಯ ಆಲ್ಕೀನ್ಗಳ ಸಂದರ್ಭದಲ್ಲಿ, ಇದು ಎರಡು ಎನ್ಆಂಟಿಯೋಮರ್ಗಳಿಗೆ ಕಾರಣವಾಗುತ್ತದೆ ಮೂವರುಬ್ರೋಮಿನ್ ಅನ್ನು ಸೇರಿಸಿದಾಗ ರೂಪ ಸಿಸ್-ಐಸೋಮರ್ ಅಥವಾ ಎನಾಂಟಿಯೋಮರ್ ಎರಿಥ್ರೋ- ಹ್ಯಾಲೊಜೆನೇಶನ್ ಮೇಲೆ ರೂಪಗಳು ಟ್ರಾನ್ಸ್-ಐಸೋಮರ್. ಬ್ರೋಮಿನ್ ಅನ್ನು ಸೇರಿಸಿದಾಗ ಇದನ್ನು ವಾಸ್ತವವಾಗಿ ಗಮನಿಸಬಹುದು, ಉದಾಹರಣೆಗೆ, ಸಿಸ್- ಮತ್ತು ಟ್ರಾನ್ಸ್ಪೆಂಟೆನ್-2 ನ ಐಸೋಮರ್ಗಳು.
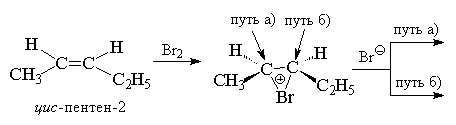



ಸಮ್ಮಿತೀಯ ಆಲ್ಕೀನ್ಗಳ ಬ್ರೋಮಿನೇಷನ್ ಸಂದರ್ಭದಲ್ಲಿ, ಉದಾಹರಣೆಗೆ, ಸಿಸ್- ಅಥವಾ ಟ್ರಾನ್ಸ್-ಹೆಕ್ಸೀನ್-3 ರಚನೆಯಾಗಬೇಕು ಅಥವಾ ರೇಸ್ಮೇಟ್ ( ಡಿ,ಎಲ್-ಫಾರ್ಮ್), ಅಥವಾ ಮೆಸೊ- ಅಂತಿಮ ಡೈಬ್ರೊಮೈಡ್ನ ರೂಪ, ಇದನ್ನು ವಾಸ್ತವವಾಗಿ ಗಮನಿಸಲಾಗಿದೆ.


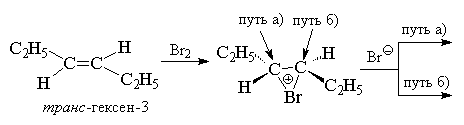

ಕಡಿಮೆ ತಾಪಮಾನದಲ್ಲಿ ನ್ಯೂಕ್ಲಿಯೊಫಿಲಿಕ್ ಅಲ್ಲದ, ಅಸಡ್ಡೆ ಪರಿಸರದಲ್ಲಿ ಹ್ಯಾಲೊಜೆನಿಯಮ್ ಅಯಾನುಗಳ ಅಸ್ತಿತ್ವದ ಸ್ವತಂತ್ರ, ನೇರ ಪುರಾವೆಗಳಿವೆ. NMR ಸ್ಪೆಕ್ಟ್ರೋಸ್ಕೋಪಿಯನ್ನು ಬಳಸಿಕೊಂಡು, ಬ್ರೋಮೋನಿಯಮ್ ಅಯಾನುಗಳ ರಚನೆಯು 3-ಬ್ರೊಮೊ-2-ಮೀಥೈಲ್-2-ಫ್ಲೋರೊಬ್ಯುಟೇನ್ನ ಅಯಾನೀಕರಣದ ಸಮಯದಲ್ಲಿ ಬಹಳ ಕ್ರಿಯೆಯ ಅಡಿಯಲ್ಲಿ ದಾಖಲಿಸಲ್ಪಟ್ಟಿದೆ. ಬಲವಾದ ಆಮ್ಲ-80 0 C ನಲ್ಲಿ ದ್ರವ ಸಲ್ಫರ್ ಡೈಆಕ್ಸೈಡ್ನ ದ್ರಾವಣದಲ್ಲಿ ಲೆವಿಸ್ ಆಂಟಿಮನಿ ಪೆಂಟಾಫ್ಲೋರೈಡ್.

ನ್ಯೂಕ್ಲಿಯೊಫಿಲಿಕ್ ಅಲ್ಲದ ಪರಿಸರದಲ್ಲಿ -80 0 C ನಲ್ಲಿ ಈ ಕ್ಯಾಷನ್ ಸಾಕಷ್ಟು ಸ್ಥಿರವಾಗಿರುತ್ತದೆ, ಆದರೆ ಯಾವುದೇ ನ್ಯೂಕ್ಲಿಯೊಫಿಲಿಕ್ ಏಜೆಂಟ್ಗಳ ಕ್ರಿಯೆಯಿಂದ ಅಥವಾ ಬಿಸಿಯಾದ ಮೇಲೆ ತಕ್ಷಣವೇ ನಾಶವಾಗುತ್ತದೆ.
ನ್ಯೂಕ್ಲಿಯೊಫೈಲ್ಗಳ ಕ್ರಿಯೆಯ ಅಡಿಯಲ್ಲಿ ಸ್ಟೆರಿಕ್ ಅಡೆತಡೆಗಳು ಅವುಗಳ ತೆರೆಯುವಿಕೆಯನ್ನು ತಡೆಗಟ್ಟಿದರೆ ಆವರ್ತಕ ಬ್ರೋಮೋನಿಯಮ್ ಅಯಾನುಗಳನ್ನು ಕೆಲವೊಮ್ಮೆ ಶುದ್ಧ ರೂಪದಲ್ಲಿ ಪ್ರತ್ಯೇಕಿಸಬಹುದು:

ವಿಶೇಷ ಪರಿಸ್ಥಿತಿಗಳಲ್ಲಿ ಸಾಕಷ್ಟು ಸ್ಥಿರವಾಗಿರುವ ಬ್ರೋಮೋನಿಯಮ್ ಅಯಾನುಗಳ ಅಸ್ತಿತ್ವದ ಸಾಧ್ಯತೆಯು ಆಲ್ಕೋಹಾಲ್, ಅಸಿಟಿಕ್ ಆಮ್ಲ ಮತ್ತು ಇತರ ಎಲೆಕ್ಟ್ರಾನ್ಗಳಲ್ಲಿನ ಆಲ್ಕೀನ್ನ ಡಬಲ್ ಬಾಂಡ್ಗೆ ಬ್ರೋಮಿನ್ ಸೇರ್ಪಡೆಯ ಪ್ರತಿಕ್ರಿಯೆಯಲ್ಲಿ ಅವುಗಳ ರಚನೆಯ ನೇರ ಪುರಾವೆಯಾಗಿ ಕಾರ್ಯನಿರ್ವಹಿಸುವುದಿಲ್ಲ ಎಂಬುದು ಸ್ಪಷ್ಟವಾಗಿದೆ. - ದ್ರಾವಕಗಳನ್ನು ದಾನ ಮಾಡುವುದು. ಅಂತಹ ಡೇಟಾವನ್ನು ಡಬಲ್ ಬಾಂಡ್ನಲ್ಲಿ ಎಲೆಕ್ಟ್ರೋಫಿಲಿಕ್ ಸೇರ್ಪಡೆ ಪ್ರಕ್ರಿಯೆಯಲ್ಲಿ ಹ್ಯಾಲೊಜೆನಿಯಮ್ ಅಯಾನುಗಳ ರಚನೆಯ ಮೂಲಭೂತ ಸಾಧ್ಯತೆಯ ಸ್ವತಂತ್ರ ದೃಢೀಕರಣವಾಗಿ ಮಾತ್ರ ಪರಿಗಣಿಸಬೇಕು.
ಹಾಲೈಡ್ ಅಯಾನಿನ ಪರಿಕಲ್ಪನೆಯು ಡಬಲ್ ಬಾಂಡ್ಗೆ ಅಯೋಡಿನ್ನ ಸೇರ್ಪಡೆಯ ಹಿಮ್ಮುಖತೆಗೆ ತರ್ಕಬದ್ಧ ವಿವರಣೆಯನ್ನು ನೀಡಲು ನಮಗೆ ಅನುಮತಿಸುತ್ತದೆ. ಹ್ಯಾಲೋಜೆನಿಯಮ್ ಕ್ಯಾಷನ್ ಮೂರು ಎಲೆಕ್ಟ್ರೋಫಿಲಿಕ್ ಕೇಂದ್ರಗಳನ್ನು ಹ್ಯಾಲೈಡ್ ಅಯಾನ್ನಿಂದ ನ್ಯೂಕ್ಲಿಯೊಫಿಲಿಕ್ ದಾಳಿಗೆ ಪ್ರವೇಶಿಸಬಹುದು: ಎರಡು ಕಾರ್ಬನ್ ಪರಮಾಣುಗಳು ಮತ್ತು ಹ್ಯಾಲೊಜೆನ್ ಪರಮಾಣು. ಕ್ಲೋರೋನಿಯಮ್ ಅಯಾನುಗಳ ಸಂದರ್ಭದಲ್ಲಿ, Cl - ಅಯಾನ್ ಕ್ಯಾಷನ್ನ ಕಾರ್ಬನ್ ಕೇಂದ್ರಗಳ ಮೇಲೆ ಪ್ರಾಶಸ್ತ್ಯವಾಗಿ ಅಥವಾ ಪ್ರತ್ಯೇಕವಾಗಿ ದಾಳಿ ಮಾಡುತ್ತದೆ. ಬ್ರೋಮೋನಿಯಮ್ ಕ್ಯಾಷನ್ಗಾಗಿ, ಎರಡೂ ಕಾರ್ಬನ್ ಪರಮಾಣುಗಳ ಮೇಲೆ ಮತ್ತು ಬ್ರೋಮಿನ್ ಪರಮಾಣುವಿನ ಮೇಲೆ ಬ್ರೋಮೈಡ್ ಅಯಾನಿನ ದಾಳಿಯಿಂದಾಗಿ ಹ್ಯಾಲೊಜೆನಿಯಮ್ ಅಯಾನು ತೆರೆಯುವ ಎರಡೂ ದಿಕ್ಕುಗಳು ಸಮಾನವಾಗಿ ಸಂಭವನೀಯವಾಗಿರುತ್ತವೆ. ಬ್ರೋಮೋನಿಯಮ್ ಅಯಾನಿನ ಬ್ರೋಮಿನ್ ಪರಮಾಣುವಿನ ಮೇಲೆ ನ್ಯೂಕ್ಲಿಯೊಫಿಲಿಕ್ ದಾಳಿಯು ಆರಂಭಿಕ ಕಾರಕಗಳಾದ ಬ್ರೋಮಿನ್ ಮತ್ತು ಆಲ್ಕೀನ್ಗಳಿಗೆ ಕಾರಣವಾಗುತ್ತದೆ:

ಅಯೋಡಿನ್ ಪರಮಾಣುವಿನ ಮೇಲೆ ಅಯೋಡೈಡ್ ಅಯಾನಿನ ದಾಳಿಯ ಪರಿಣಾಮವಾಗಿ ಅಯೋಡೋನಿಯಮ್ ಅಯಾನು ಪ್ರಧಾನವಾಗಿ ಬಹಿರಂಗಗೊಳ್ಳುತ್ತದೆ ಮತ್ತು ಆದ್ದರಿಂದ ಆರಂಭಿಕ ಕಾರಕಗಳು ಮತ್ತು ಅಯೋಡೋನಿಯಮ್ ಅಯಾನುಗಳ ನಡುವಿನ ಸಮತೋಲನವನ್ನು ಎಡಕ್ಕೆ ವರ್ಗಾಯಿಸಲಾಗುತ್ತದೆ.

ಇದರ ಜೊತೆಯಲ್ಲಿ, ಅಂತಿಮ ಸೇರ್ಪಡೆ ಉತ್ಪನ್ನವಾದ ವಿಸಿನಲ್ ಡಯೋಡೈಡ್, ದ್ರಾವಣದಲ್ಲಿ ಇರುವ ಟ್ರಯೋಡೈಡ್ ಅಯಾನ್ನಿಂದ ಅಯೋಡಿನ್ ಪರಮಾಣುವಿನಲ್ಲಿ ನ್ಯೂಕ್ಲಿಯೊಫಿಲಿಕ್ ದಾಳಿಗೆ ಒಳಗಾಗಬಹುದು, ಇದು ಆರಂಭಿಕ ಕಾರಕಗಳಾದ ಆಲ್ಕೀನ್ ಮತ್ತು ಅಯೋಡಿನ್ ರಚನೆಗೆ ಕಾರಣವಾಗುತ್ತದೆ. ಬೇರೆ ರೀತಿಯಲ್ಲಿ ಹೇಳುವುದಾದರೆ, ಸಂಕಲನ ಕ್ರಿಯೆಯ ಪರಿಸ್ಥಿತಿಗಳಲ್ಲಿ, ಪರಿಣಾಮವಾಗಿ ಬರುವ ವಿಸಿನಲ್ ಡಯೋಡೈಡ್ ಅನ್ನು ಟ್ರೈಯೋಡೈಡ್ ಅಯಾನಿನ ಕ್ರಿಯೆಯ ಅಡಿಯಲ್ಲಿ ಡಿಯೋಡಿನೇಟ್ ಮಾಡಲಾಗುತ್ತದೆ. ವಿಸಿನಲ್ ಡೈಕ್ಲೋರೈಡ್ಗಳು ಮತ್ತು ಡೈಬ್ರೊಮೈಡ್ಗಳು ಕ್ರಮವಾಗಿ ಆಲ್ಕೀನ್ಗಳಿಗೆ ಕ್ಲೋರಿನ್ ಅಥವಾ ಬ್ರೋಮಿನ್ ಸೇರ್ಪಡೆಯ ಪರಿಸ್ಥಿತಿಗಳಲ್ಲಿ ಡಿಹಲೋಜೆನೇಟ್ ಆಗುವುದಿಲ್ಲ.
ಕ್ಲೋರಿನ್ ಅಥವಾ ಬ್ರೋಮಿನ್ನ ವಿರೋಧಿ ಸೇರ್ಪಡೆ ಅಲ್ಕೆನ್ಗಳ ವಿಶಿಷ್ಟ ಲಕ್ಷಣವಾಗಿದೆ, ಇದರಲ್ಲಿ ದ್ವಿಬಂಧವು ಬೆಂಜೀನ್ ರಿಂಗ್ನ -ಎಲೆಕ್ಟ್ರಾನ್ಗಳೊಂದಿಗೆ ಸಂಯೋಜಿತವಾಗಿಲ್ಲ. ಸ್ಟೈರೀನ್, ಸ್ಟಿಲ್ಬೀನ್ ಮತ್ತು ಅವುಗಳ ಉತ್ಪನ್ನಗಳ ಜೊತೆಗೆ ವಿರೋಧಿ- ಪ್ರವೇಶ ನಡೆಯುತ್ತದೆ ಮತ್ತು ಸಿನ್- ಹ್ಯಾಲೊಜೆನ್ ಸೇರ್ಪಡೆ, ಇದು ಧ್ರುವೀಯ ಪರಿಸರದಲ್ಲಿ ಪ್ರಬಲವಾಗಬಹುದು.

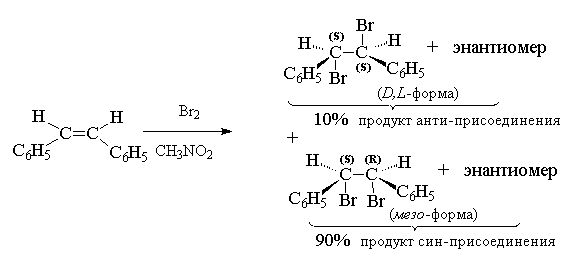
ನ್ಯೂಕ್ಲಿಯೊಫಿಲಿಕ್ ದ್ರಾವಕ ಪರಿಸರದಲ್ಲಿ ಡಬಲ್ ಬಾಂಡ್ಗೆ ಹ್ಯಾಲೊಜೆನ್ ಅನ್ನು ಸೇರಿಸುವ ಸಂದರ್ಭಗಳಲ್ಲಿ, ಹ್ಯಾಲೊಜೆನಿಯಮ್ ಅಯಾನಿನ ಮೂರು-ಸದಸ್ಯ ರಿಂಗ್ ಅನ್ನು ತೆರೆಯುವಲ್ಲಿ ದ್ರಾವಕವು ಹ್ಯಾಲೈಡ್ ಅಯಾನ್ನೊಂದಿಗೆ ಪರಿಣಾಮಕಾರಿಯಾಗಿ ಸ್ಪರ್ಧಿಸುತ್ತದೆ:

ದ್ರಾವಕ ಅಥವಾ ಇತರ "ಬಾಹ್ಯ" ನ್ಯೂಕ್ಲಿಯೊಫಿಲಿಕ್ ಏಜೆಂಟ್ ಭಾಗವಹಿಸುವಿಕೆಯೊಂದಿಗೆ ಸೇರ್ಪಡೆ ಉತ್ಪನ್ನಗಳ ರಚನೆಯನ್ನು ಸಂಯೋಜಿತ ಸೇರ್ಪಡೆ ಪ್ರತಿಕ್ರಿಯೆ ಎಂದು ಕರೆಯಲಾಗುತ್ತದೆ. ಬ್ರೋಮಿನ್ ಮತ್ತು ಸ್ಟೈರೀನ್ ಮೆಥನಾಲ್ನಲ್ಲಿ ಪ್ರತಿಕ್ರಿಯಿಸಿದಾಗ, ಎರಡು ಉತ್ಪನ್ನಗಳು ರೂಪುಗೊಳ್ಳುತ್ತವೆ: ವಿಸಿನಲ್ ಡೈಬ್ರೊಮೈಡ್ ಮತ್ತು ಬ್ರೋಮಿನ್ ಎಸ್ಟರ್, ಇವುಗಳ ಅನುಪಾತವು ಮೆಥನಾಲ್ನಲ್ಲಿನ ಬ್ರೋಮಿನ್ ಸಾಂದ್ರತೆಯನ್ನು ಅವಲಂಬಿಸಿರುತ್ತದೆ.
ಹೆಚ್ಚು ದುರ್ಬಲಗೊಳಿಸಿದ ದ್ರಾವಣದಲ್ಲಿ, ಸಂಯೋಜಿತ ಸೇರ್ಪಡೆ ಉತ್ಪನ್ನವು ಪ್ರಾಬಲ್ಯ ಹೊಂದಿದೆ, ಆದರೆ ಕೇಂದ್ರೀಕೃತ ದ್ರಾವಣದಲ್ಲಿ, ಇದಕ್ಕೆ ವಿರುದ್ಧವಾಗಿ, ವಿಸಿನಲ್ ಡೈಬ್ರೊಮೈಡ್ ಮೇಲುಗೈ ಸಾಧಿಸುತ್ತದೆ. ಜಲೀಯ ದ್ರಾವಣದಲ್ಲಿ, ಹ್ಯಾಲೋಹೈಡ್ರಿನ್ (-ಕಾರ್ಬನ್ ಪರಮಾಣುವಿನಲ್ಲಿ ಹ್ಯಾಲೊಜೆನ್ ಹೊಂದಿರುವ ಆಲ್ಕೋಹಾಲ್) - ಸಂಯೋಜಿತ ಸೇರ್ಪಡೆಯ ಉತ್ಪನ್ನ - ಯಾವಾಗಲೂ ಮೇಲುಗೈ ಸಾಧಿಸುತ್ತದೆ.

ಅವಳ-ಕನ್ಫಾರ್ಮರ್ ಟ್ರಾನ್ಸ್-2-ಕ್ಲೋರೊಸೈಕ್ಲೋಹೆಕ್ಸಾನಾಲ್ ಅನ್ನು O-H ಹೈಡ್ರೋಜನ್ ಬಂಧದಿಂದ ಮತ್ತಷ್ಟು ಸ್ಥಿರಗೊಳಿಸಲಾಗುತ್ತದೆ . . . Cl. ಅಸಮಪಾರ್ಶ್ವದ ಆಲ್ಕೀನ್ಗಳ ಸಂದರ್ಭದಲ್ಲಿ, ಸಂಯೋಜಿತ ಸಂಕಲನ ಪ್ರತಿಕ್ರಿಯೆಗಳಲ್ಲಿ, ಹ್ಯಾಲೊಜೆನ್ ಯಾವಾಗಲೂ ಹೆಚ್ಚಿನ ಸಂಖ್ಯೆಯ ಹೈಡ್ರೋಜನ್ ಪರಮಾಣುಗಳನ್ನು ಹೊಂದಿರುವ ಇಂಗಾಲದ ಪರಮಾಣುವಿಗೆ ಮತ್ತು ನ್ಯೂಕ್ಲಿಯೊಫಿಲಿಕ್ ಏಜೆಂಟ್ ಅನ್ನು ಕಡಿಮೆ ಸಂಖ್ಯೆಯ ಹೈಡ್ರೋಜನ್ ಪರಮಾಣುಗಳನ್ನು ಹೊಂದಿರುವ ಕಾರ್ಬನ್ಗೆ ಸೇರಿಸುತ್ತದೆ. ಸೇರುವ ಗುಂಪುಗಳ ವಿಭಿನ್ನ ವ್ಯವಸ್ಥೆಯನ್ನು ಹೊಂದಿರುವ ಐಸೊಮೆರಿಕ್ ಉತ್ಪನ್ನವು ರೂಪುಗೊಂಡಿಲ್ಲ. ಇದರರ್ಥ ಮಧ್ಯಂತರವಾಗಿ ರೂಪುಗೊಂಡ ಸೈಕ್ಲಿಕ್ ಹ್ಯಾಲೊಜೆನೊನಿಯಮ್ ಅಯಾನು ಎರಡು ಬಂಧಗಳೊಂದಿಗೆ ಅಸಮಪಾರ್ಶ್ವದ ರಚನೆಯನ್ನು ಹೊಂದಿರಬೇಕು C 1 -Hal ಮತ್ತು C 2 -Hal ಶಕ್ತಿ ಮತ್ತು ಶಕ್ತಿ ಮತ್ತು ಹೆಚ್ಚಿನವುಗಳಲ್ಲಿ ಭಿನ್ನವಾಗಿರುತ್ತವೆ ಧನಾತ್ಮಕ ಆವೇಶಆಂತರಿಕ ಇಂಗಾಲದ ಪರಮಾಣು C2 ನಲ್ಲಿ, ಇದನ್ನು ಸಚಿತ್ರವಾಗಿ ಎರಡು ರೀತಿಯಲ್ಲಿ ವ್ಯಕ್ತಪಡಿಸಬಹುದು:

ಆದ್ದರಿಂದ, ಹ್ಯಾಲೊಜೆನಿಯಮ್ ಅಯಾನಿನ C2 ಕಾರ್ಬನ್ ಪರಮಾಣು ದ್ರಾವಕದಿಂದ ನ್ಯೂಕ್ಲಿಯೊಫಿಲಿಕ್ ದಾಳಿಗೆ ಒಳಪಟ್ಟಿರುತ್ತದೆ, ಇದು ಹೆಚ್ಚು ಬದಲಿ ಮತ್ತು ಸ್ಟೆರಿಕಲ್ ಕಡಿಮೆ ಪ್ರವೇಶಿಸಬಹುದಾದ ವಾಸ್ತವತೆಯ ಹೊರತಾಗಿಯೂ.


ಬ್ರೋಮೊಹೈಡ್ರಿನ್ಗಳ ಸಂಶ್ಲೇಷಣೆಗೆ ಉತ್ತಮ ಪೂರ್ವಸಿದ್ಧತಾ ವಿಧಾನವೆಂದರೆ ಎನ್-ಬ್ರೊಮೊಸಸಿನಿಮೈಡ್ (ಎನ್-ಬ್ರೊಮೊಸಸಿನಿಮೈಡ್) ಅನ್ನು ಬಳಸಿಕೊಂಡು ಆಲ್ಕೀನ್ಗಳ ಹೈಡ್ರಾಕ್ಸಿಬ್ರೊಮಿನೇಷನ್ ಎನ್.ಬಿ.ಎಸ್.ಡೈಮಿಥೈಲ್ ಸಲ್ಫಾಕ್ಸೈಡ್ನ ಬೈನರಿ ಮಿಶ್ರಣದಲ್ಲಿ ( DMSO) ಮತ್ತು ನೀರು.

ಈ ಪ್ರತಿಕ್ರಿಯೆಯನ್ನು ನೀರಿನಲ್ಲಿ ಅಥವಾ ಇಲ್ಲದೆ ನಡೆಸಬಹುದು DMSO, ಆದಾಗ್ಯೂ, ಈ ಸಂದರ್ಭದಲ್ಲಿ ಬ್ರೋಮೊಹೈಡ್ರಿನ್ಗಳ ಇಳುವರಿಯು ಸ್ವಲ್ಪ ಕಡಿಮೆಯಾಗಿದೆ.



ಆಲ್ಕೀನ್ಗಳ ಹ್ಯಾಲೊಜೆನೇಶನ್ ಕ್ರಿಯೆಯಲ್ಲಿ ಸಂಯೋಜಿತ ಸೇರ್ಪಡೆ ಉತ್ಪನ್ನಗಳ ರಚನೆಯು ಒಂದು ಹ್ಯಾಲೊಜೆನ್ ಅಣುವಿನ ಸೇರ್ಪಡೆಯ ಸಿಂಕ್ರೊನಸ್ ಕಾರ್ಯವಿಧಾನವನ್ನು ತಿರಸ್ಕರಿಸಲು ನಮಗೆ ಅನುಮತಿಸುತ್ತದೆ. ಡಬಲ್ ಬಾಂಡ್ಗೆ ಸಂಯೋಜಿತ ಸೇರ್ಪಡೆಯು ಹ್ಯಾಲೊಜೆನಿಯಮ್ ಕ್ಯಾಶನ್ ಅನ್ನು ಮಧ್ಯಂತರವಾಗಿ ಒಳಗೊಂಡಿರುವ ಎರಡು-ಹಂತದ ಕಾರ್ಯವಿಧಾನದೊಂದಿಗೆ ಉತ್ತಮ ಒಪ್ಪಂದದಲ್ಲಿದೆ.
ಡಬಲ್ ಬಾಂಡ್ಗೆ ಎಲೆಕ್ಟ್ರೋಫಿಲಿಕ್ ಸೇರ್ಪಡೆಯ ಪ್ರತಿಕ್ರಿಯೆಗಾಗಿ, ಎಲೆಕ್ಟ್ರಾನ್-ದಾನ ಮಾಡುವ ಆಲ್ಕೈಲ್ ಬದಲಿಗಳ ಉಪಸ್ಥಿತಿಯಲ್ಲಿ ಪ್ರತಿಕ್ರಿಯೆ ದರದಲ್ಲಿ ಹೆಚ್ಚಳ ಮತ್ತು ಡಬಲ್ ಬಾಂಡ್ನಲ್ಲಿ ಎಲೆಕ್ಟ್ರಾನ್-ಹಿಂತೆಗೆದುಕೊಳ್ಳುವ ಬದಲಿಗಳ ಉಪಸ್ಥಿತಿಯಲ್ಲಿ ಇಳಿಕೆ ನಿರೀಕ್ಷಿಸಬೇಕು. ವಾಸ್ತವವಾಗಿ, ಎಥಿಲೀನ್ನಿಂದ ಅದರ ಮೀಥೈಲ್-ಬದಲಿ ಉತ್ಪನ್ನಗಳಿಗೆ ಚಲಿಸುವಾಗ ಡಬಲ್ ಬಾಂಡ್ಗೆ ಕ್ಲೋರಿನ್ ಮತ್ತು ಬ್ರೋಮಿನ್ ಸೇರ್ಪಡೆಯ ದರವು ತೀವ್ರವಾಗಿ ಹೆಚ್ಚಾಗುತ್ತದೆ. ಉದಾಹರಣೆಗೆ, ಬ್ರೋಮಿನ್ ಅನ್ನು ಟೆಟ್ರಾಮೆಥಿಲೀನ್ಗೆ ಸೇರಿಸುವ ದರವು 1-ಬ್ಯುಟೀನ್ಗೆ ಅದರ ಸೇರ್ಪಡೆಯ ದರಕ್ಕಿಂತ 10 5 ಪಟ್ಟು ಹೆಚ್ಚು. ಈ ಅಗಾಧವಾದ ವೇಗವರ್ಧನೆಯು ಸಂಕ್ರಮಣ ಸ್ಥಿತಿಯ ಹೆಚ್ಚಿನ ಧ್ರುವೀಯತೆಯನ್ನು ಸ್ಪಷ್ಟವಾಗಿ ಸೂಚಿಸುತ್ತದೆ ಮತ್ತು ಪರಿವರ್ತನೆಯ ಸ್ಥಿತಿಯಲ್ಲಿ ಹೆಚ್ಚಿನ ಮಟ್ಟದ ಚಾರ್ಜ್ ಬೇರ್ಪಡಿಕೆ ಮತ್ತು ಸೇರ್ಪಡೆಯ ಎಲೆಕ್ಟ್ರೋಫಿಲಿಕ್ ಕಾರ್ಯವಿಧಾನಕ್ಕೆ ಅನುಗುಣವಾಗಿರುತ್ತದೆ.
ಕೆಲವು ಸಂದರ್ಭಗಳಲ್ಲಿ, ಎಲೆಕ್ಟ್ರಾನ್-ದಾನ ಮಾಡುವ ಬದಲಿಗಳನ್ನು ಹೊಂದಿರುವ ಆಲ್ಕೆನ್ಗಳಿಗೆ ಕ್ಲೋರಿನ್ ಸೇರಿಸುವಿಕೆಯು ಕ್ಲೋರೈಡ್ ಅಯಾನು ಸೇರಿಸುವ ಬದಲು ಮಧ್ಯಂತರ ಸಂಯುಕ್ತದಿಂದ ಪ್ರೋಟಾನ್ನ ಅಮೂರ್ತತೆಯೊಂದಿಗೆ ಇರುತ್ತದೆ. ಪ್ರೋಟಾನ್ನ ಅಮೂರ್ತತೆಯು ಕ್ಲೋರಿನ್-ಬದಲಿ ಆಲ್ಕೀನ್ ರಚನೆಗೆ ಕಾರಣವಾಗುತ್ತದೆ, ಇದನ್ನು ಔಪಚಾರಿಕವಾಗಿ ಡಬಲ್ ಬಾಂಡ್ ವಲಸೆಯೊಂದಿಗೆ ನೇರ ಪರ್ಯಾಯವಾಗಿ ಪರಿಗಣಿಸಬಹುದು. ಆದಾಗ್ಯೂ, ಐಸೊಟೋಪ್ ಲೇಬಲಿಂಗ್ನ ಪ್ರಯೋಗಗಳು ಹೆಚ್ಚಿನದನ್ನು ಸೂಚಿಸುತ್ತವೆ ಸಂಕೀರ್ಣ ಸ್ವಭಾವರೂಪಾಂತರಗಳು ಇಲ್ಲಿ ನಡೆಯುತ್ತಿವೆ. ಐಸೊಬ್ಯುಟಿಲೀನ್ ಅನ್ನು 0 0 C ನಲ್ಲಿ ಕ್ಲೋರಿನೇಟ್ ಮಾಡಿದಾಗ, ನಿರೀಕ್ಷಿತ ಡೈಕ್ಲೋರೈಡ್ನ ಬದಲಾಗಿ 2-ಮೀಥೈಲ್-3-ಕ್ಲೋರೋಪ್ರೊಪೀನ್ (ಮೆಟಾಲಿಲ್ ಕ್ಲೋರೈಡ್) ರಚನೆಯಾಗುತ್ತದೆ, ಇದು ಡಬಲ್ ಬಾಂಡ್ನಲ್ಲಿ ಸೇರ್ಪಡೆಯ ಉತ್ಪನ್ನವಾಗಿದೆ.

ಔಪಚಾರಿಕವಾಗಿ, ಒಂದು ಪರ್ಯಾಯವಿದೆ ಎಂದು ತೋರುತ್ತದೆ, ಒಂದು ಪ್ರವೇಶವಲ್ಲ. 14 ಸಿ ಐಸೊಟೋಪ್ನೊಂದಿಗೆ ಸ್ಥಾನ 1 ರಲ್ಲಿ ಐಸೊಬ್ಯುಟಿಲೀನ್ ಅನ್ನು ಬಳಸಿಕೊಂಡು ಈ ಪ್ರತಿಕ್ರಿಯೆಯ ಅಧ್ಯಯನವು ಕ್ಲೋರಿನ್ನೊಂದಿಗೆ ಹೈಡ್ರೋಜನ್ನ ನೇರ ಬದಲಿ ಸಂಭವಿಸುವುದಿಲ್ಲ ಎಂದು ತೋರಿಸಿದೆ, ಏಕೆಂದರೆ ಪರಿಣಾಮವಾಗಿ ಮೆಟಾಲಿಲ್ ಕ್ಲೋರೈಡ್ನಲ್ಲಿ ಲೇಬಲ್ 14 CH 2 Cl ಗುಂಪಿನಲ್ಲಿದೆ. ಈ ಫಲಿತಾಂಶವನ್ನು ರೂಪಾಂತರಗಳ ಕೆಳಗಿನ ಅನುಕ್ರಮದಿಂದ ವಿವರಿಸಬಹುದು:

ಕೆಲವು ಸಂದರ್ಭಗಳಲ್ಲಿ, ಆಲ್ಕೈಲ್ ಗುಂಪಿನ 1,2-ವಲಸೆ ಕೂಡ ಸಂಭವಿಸಬಹುದು

CCL 4 (ಧ್ರುವೀಯವಲ್ಲದ ದ್ರಾವಕ) ನಲ್ಲಿ ಈ ಪ್ರತಿಕ್ರಿಯೆಯು ಸುಮಾರು 100% ಡೈಕ್ಲೋರೈಡ್ ಅನ್ನು ನೀಡುತ್ತದೆ ಬಿ- ಡಬಲ್ ಬಾಂಡ್ನಲ್ಲಿ ಸಾಮಾನ್ಯ ಸೇರ್ಪಡೆಯ ಉತ್ಪನ್ನ (ಮರುಜೋಡಣೆ ಇಲ್ಲದೆ).
ಈ ಪ್ರಕಾರದ ಅಸ್ಥಿಪಂಜರದ ಮರುಜೋಡಣೆಗಳು ಮಧ್ಯಂತರ ಕಣಗಳಾಗಿ ತೆರೆದ ಕಾರ್ಬೋಕೇಶನ್ಗಳನ್ನು ಒಳಗೊಂಡಿರುವ ಪ್ರಕ್ರಿಯೆಗಳಿಗೆ ಹೆಚ್ಚು ವಿಶಿಷ್ಟವಾಗಿದೆ. ಈ ಸಂದರ್ಭಗಳಲ್ಲಿ ಕ್ಲೋರಿನ್ ಅನ್ನು ಸೇರಿಸುವುದು ಕ್ಲೋರೋನಿಯಮ್ ಅಯಾನಿನ ಮೂಲಕ ಅಲ್ಲ, ಆದರೆ ತೆರೆದ ಕಾರ್ಬೋಕೇಶನ್ಗೆ ಹತ್ತಿರವಿರುವ ಕ್ಯಾಟಯಾನಿಕ್ ಕಣದ ಮೂಲಕ ಸಂಭವಿಸುತ್ತದೆ. ಅದೇ ಸಮಯದಲ್ಲಿ, ಡಬಲ್ ಬಾಂಡ್ನಲ್ಲಿ ಹ್ಯಾಲೊಜೆನ್ಗಳು ಮತ್ತು ಮಿಶ್ರ ಹ್ಯಾಲೊಜೆನ್ಗಳನ್ನು ಸೇರಿಸುವ ಪ್ರಕ್ರಿಯೆಗಳಲ್ಲಿ ಅಸ್ಥಿಪಂಜರದ ಮರುಜೋಡಣೆಗಳು ಅಪರೂಪದ ವಿದ್ಯಮಾನವಾಗಿದೆ ಎಂದು ಗಮನಿಸಬೇಕು: ಕ್ಲೋರಿನ್ ಸೇರ್ಪಡೆಯ ಸಮಯದಲ್ಲಿ ಅವುಗಳನ್ನು ಹೆಚ್ಚಾಗಿ ಗಮನಿಸಲಾಗುತ್ತದೆ ಮತ್ತು ಸೇರ್ಪಡೆಯ ಸಮಯದಲ್ಲಿ ಕಡಿಮೆ ಬಾರಿ ಬ್ರೋಮಿನ್. ಧ್ರುವೀಯವಲ್ಲದ ದ್ರಾವಕಗಳಿಂದ (CCl 4) ಧ್ರುವೀಯ ಪದಗಳಿಗಿಂತ (ನೈಟ್ರೋಮೆಥೇನ್, ಅಸಿಟೋನೈಟ್ರೈಲ್) ಚಲಿಸುವಾಗ ಅಂತಹ ಮರುಜೋಡಣೆಗಳ ಸಂಭವನೀಯತೆಯು ಹೆಚ್ಚಾಗುತ್ತದೆ.
ಸ್ಟೀರಿಯೊಕೆಮಿಸ್ಟ್ರಿ, ಸಂಯೋಜಿತ ಸೇರ್ಪಡೆ, ಆಲ್ಕೀನ್ನಲ್ಲಿನ ಬದಲಿಗಳ ಪ್ರಭಾವ, ಹಾಗೆಯೇ ಡಬಲ್ ಬಾಂಡ್ನಲ್ಲಿ ಹ್ಯಾಲೊಜೆನ್ಗಳ ಸಂಕಲನ ಪ್ರತಿಕ್ರಿಯೆಗಳಲ್ಲಿನ ಮರುಜೋಡಣೆಗಳ ಕುರಿತು ಪ್ರಸ್ತುತಪಡಿಸಿದ ಡೇಟಾವನ್ನು ಸಂಕ್ಷಿಪ್ತಗೊಳಿಸುವುದು, ಅವುಗಳು ಎಲೆಕ್ಟ್ರೋಫಿಲಿಕ್ ಸೇರ್ಪಡೆಯ ಕಾರ್ಯವಿಧಾನದೊಂದಿಗೆ ಉತ್ತಮ ಒಪ್ಪಂದದಲ್ಲಿವೆ ಎಂದು ಗಮನಿಸಬೇಕು. ಆವರ್ತಕ ಹ್ಯಾಲೊಜೆನಿಯಮ್ ಅಯಾನು. ಎರಡು ಹ್ಯಾಲೊಜೆನ್ ಪರಮಾಣುಗಳ ಬಂಧದ ಧ್ರುವೀಯತೆಯಿಂದ ಸೇರ್ಪಡೆಯ ಹಂತಗಳನ್ನು ನಿರ್ಧರಿಸುವ ಆಲ್ಕೀನ್ಗಳಿಗೆ ಮಿಶ್ರ ಹ್ಯಾಲೊಜೆನ್ಗಳ ಸೇರ್ಪಡೆಯ ಡೇಟಾವನ್ನು ಅದೇ ರೀತಿಯಲ್ಲಿ ಅರ್ಥೈಸಬಹುದು.
ವ್ಯಾಖ್ಯಾನ
ಆಲ್ಕೆನೆಸ್ಎಂದು ಕರೆಯುತ್ತಾರೆ ಅಪರ್ಯಾಪ್ತ ಹೈಡ್ರೋಕಾರ್ಬನ್ಗಳು, ಅದರ ಅಣುಗಳು ಒಂದು ಡಬಲ್ ಬಂಧವನ್ನು ಹೊಂದಿರುತ್ತವೆ. ಎಥಿಲೀನ್ ಅನ್ನು ಉದಾಹರಣೆಯಾಗಿ ಬಳಸುವ ಆಲ್ಕೀನ್ ಅಣುವಿನ ರಚನೆಯನ್ನು ಅಂಜೂರದಲ್ಲಿ ತೋರಿಸಲಾಗಿದೆ. 1.
ಅಕ್ಕಿ. 1. ಎಥಿಲೀನ್ ಅಣುವಿನ ರಚನೆ.
ಮೂಲಕ ಭೌತಿಕ ಗುಣಲಕ್ಷಣಗಳುಅಣುವಿನಲ್ಲಿ ಅದೇ ಸಂಖ್ಯೆಯ ಇಂಗಾಲದ ಪರಮಾಣುಗಳನ್ನು ಹೊಂದಿರುವ ಆಲ್ಕೇನ್ಗಳಿಂದ ಆಲ್ಕೀನ್ಗಳು ಸ್ವಲ್ಪ ಭಿನ್ನವಾಗಿರುತ್ತವೆ. ಕೆಳಗಿನ ಹೋಮೋಲಾಗ್ಗಳು C 2 - C 4 ನಲ್ಲಿ ಸಾಮಾನ್ಯ ಪರಿಸ್ಥಿತಿಗಳು- ಅನಿಲಗಳು; ಸಿ 5 - ಸಿ 17 - ದ್ರವಗಳು; ಹೆಚ್ಚಿನ ಹೋಮೋಲಾಗ್ಗಳು - ಘನವಸ್ತುಗಳು. ಆಲ್ಕೀನ್ಗಳು ನೀರಿನಲ್ಲಿ ಕರಗುವುದಿಲ್ಲ. ಸಾವಯವ ದ್ರಾವಕಗಳಲ್ಲಿ ಹೆಚ್ಚು ಕರಗುತ್ತದೆ.
ಆಲ್ಕೀನ್ಗಳ ತಯಾರಿಕೆ
ಉದ್ಯಮದಲ್ಲಿ, ತೈಲ ಸಂಸ್ಕರಣೆಯ ಸಮಯದಲ್ಲಿ ಆಲ್ಕೀನ್ಗಳನ್ನು ಪಡೆಯಲಾಗುತ್ತದೆ: ಅಲ್ಕೇನ್ಗಳ ಬಿರುಕು ಮತ್ತು ನಿರ್ಜಲೀಕರಣ. ಪ್ರಯೋಗಾಲಯ ವಿಧಾನಗಳುನಾವು ಆಲ್ಕೀನ್ಗಳ ಉತ್ಪಾದನೆಯನ್ನು ಎರಡು ಗುಂಪುಗಳಾಗಿ ವಿಂಗಡಿಸಿದ್ದೇವೆ:
- ಎಲಿಮಿನೇಷನ್ ಪ್ರತಿಕ್ರಿಯೆಗಳು
- ಆಲ್ಕೋಹಾಲ್ಗಳ ನಿರ್ಜಲೀಕರಣ
CH 3 -CH 2 -OH → CH 2 =CH 2 + H 2 O (H 2 SO 4 (conc), t 0 = 170).
- ಮೊನೊಹಲೋಲ್ಕನೆಸ್ನ ಡಿಹೈಡ್ರೊಹಾಲೊಜೆನೇಶನ್
CH 3 -CH(Br)-CH 2 -CH 3 + NaOH ಮದ್ಯ → CH 3 -CH=CH-CH 3 + NaBr + H 2 O (t 0).
- ಡೈಹಲೋಲ್ಕನೆಸ್ ಆಫ್ ಡಿಹಲೋಜೆನೇಶನ್
CH 3 -CH(Cl)-CH(Cl)-CH 2 -CH 3 + Zn(Mg) → CH 3 -CH=CH-CH 2 -CH 3 + ZnCl 2 (MgCl 2).
- ಆಲ್ಕೈನ್ಗಳ ಅಪೂರ್ಣ ಹೈಡ್ರೋಜನೀಕರಣ
CH≡CH + H 2 →CH 2 =CH 2 (Pd, t 0).
ಆಲ್ಕೀನ್ಗಳ ರಾಸಾಯನಿಕ ಗುಣಲಕ್ಷಣಗಳು
ಆಲ್ಕೀನ್ಗಳು ಹೆಚ್ಚು ಪ್ರತಿಕ್ರಿಯಾತ್ಮಕ ಸಾವಯವ ಸಂಯುಕ್ತಗಳಾಗಿವೆ. ಇದನ್ನು ಅವರ ರಚನೆಯಿಂದ ವಿವರಿಸಲಾಗಿದೆ. ಆಲ್ಕೀನ್ಗಳ ರಸಾಯನಶಾಸ್ತ್ರವು ಡಬಲ್ ಬಾಂಡ್ಗಳ ರಸಾಯನಶಾಸ್ತ್ರವಾಗಿದೆ. ವಿಶಿಷ್ಟ ಪ್ರತಿಕ್ರಿಯೆಗಳುಆಲ್ಕೀನ್ಗಳಿಗೆ - ಎಲೆಕ್ಟ್ರೋಫಿಲಿಕ್ ಸೇರ್ಪಡೆ ಪ್ರತಿಕ್ರಿಯೆಗಳು.
ಆಲ್ಕೀನ್ಗಳ ರಾಸಾಯನಿಕ ರೂಪಾಂತರಗಳು ವಿಭಜನೆಯೊಂದಿಗೆ ಮುಂದುವರಿಯುತ್ತವೆ:
1) π - ಎಸ್-ಎಸ್ ಸಂಪರ್ಕಗಳು(ಸೇರ್ಪಡೆ, ಪಾಲಿಮರೀಕರಣ ಮತ್ತು ಆಕ್ಸಿಡೀಕರಣ)
- ಹೈಡ್ರೋಜನೀಕರಣ
CH 3 -CH=CH 2 + H 2 → CH 3 -CH 2 -CH 2 (ಕ್ಯಾಟ್ = Pt).
- ಹ್ಯಾಲೊಜೆನೇಶನ್
CH 3 -CH 2 -CH=CH 2 + Br 2 → CH 3 -CH 2 -CH(Br)-CH 2 Br.
- ಹೈಡ್ರೊಹಾಲೊಜೆನೇಶನ್ (ಮಾರ್ಕೊವ್ನಿಕೋವ್ ನಿಯಮದ ಪ್ರಕಾರ ಮುಂದುವರಿಯುತ್ತದೆ: ಹೈಡ್ರೋಜನ್ ಪರಮಾಣು ಹೆಚ್ಚು ಹೈಡ್ರೋಜನೀಕರಿಸಿದ ಕಾರ್ಬನ್ ಪರಮಾಣುವಿಗೆ ಆದ್ಯತೆಯಾಗಿ ಅಂಟಿಕೊಳ್ಳುತ್ತದೆ)
CH 3 -CH=CH 2 + H-Cl → CH 3 -CH(Cl)-CH 3 .
- ಜಲಸಂಚಯನ
CH 2 =CH 2 + H-OH → CH 3 -CH 2 -OH (H + , t 0).
- ಪಾಲಿಮರೀಕರಣ
nCH 2 =CH 2 → -[-CH 2 -CH 2 -]- n (ಕ್ಯಾಟ್, ಟಿ 0).
- ಆಕ್ಸಿಡೀಕರಣ
CH 2 =CH 2 + 2KMnO 4 + 2KOH → HO-CH 2 -CH 2 -OH + 2K 2 MnO 4;
2CH 2 =CH 2 + O 2 → 2C 2 OH 4 (ಎಪಾಕ್ಸೈಡ್) (ಕ್ಯಾಟ್ = Ag,t 0);
2CH 2 =CH 2 + O 2 → 2CH 3 -C(O)H (ಕ್ಯಾಟ್ = PdCl 2, CuCl).
2) σ- ಮತ್ತು π-C-C ಬಂಧಗಳು
CH 3 -CH=CH-CH 2 -CH 3 + 4[O] → CH 3 COOH + CH 3 CH 2 COOH (KMnO 4, H +, t 0).
3) ಬಂಧಗಳು C sp 3 -H (ಅಲಿಲಿಕ್ ಸ್ಥಾನದಲ್ಲಿ)
CH 2 =CH 2 + Cl 2 → CH 2 =CH-Cl + HCl (t 0 =400).
4) ಎಲ್ಲಾ ಸಂಬಂಧಗಳನ್ನು ಮುರಿಯುವುದು
C 2 H 4 + 2O 2 → 2CO 2 + 2H 2 O;
C n H 2n + 3n/2 O 2 → nCO 2 + nH 2 O.
ಆಲ್ಕೀನ್ಗಳ ಅನ್ವಯಗಳು
ಆಲ್ಕೀನ್ಗಳು ಬಳಕೆಯನ್ನು ಕಂಡುಕೊಂಡಿವೆ ವಿವಿಧ ಕೈಗಾರಿಕೆಗಳು ರಾಷ್ಟ್ರೀಯ ಆರ್ಥಿಕತೆ. ವೈಯಕ್ತಿಕ ಪ್ರತಿನಿಧಿಗಳ ಉದಾಹರಣೆಯನ್ನು ನೋಡೋಣ.
ಇಥಿಲೀನ್ ಅನ್ನು ಕೈಗಾರಿಕಾ ಸಾವಯವ ಸಂಶ್ಲೇಷಣೆಯಲ್ಲಿ ವಿವಿಧವನ್ನು ಉತ್ಪಾದಿಸಲು ವ್ಯಾಪಕವಾಗಿ ಬಳಸಲಾಗುತ್ತದೆ ಸಾವಯವ ಸಂಯುಕ್ತಗಳು, ಹ್ಯಾಲೊಜೆನ್ ಉತ್ಪನ್ನಗಳು, ಆಲ್ಕೋಹಾಲ್ಗಳು (ಎಥೆನಾಲ್, ಎಥಿಲೀನ್ ಗ್ಲೈಕಾಲ್), ಅಸಿಟಾಲ್ಡಿಹೈಡ್, ಅಸಿಟಿಕ್ ಆಮ್ಲಇತ್ಯಾದಿ ಬಿ ದೊಡ್ಡ ಪ್ರಮಾಣದಲ್ಲಿಪಾಲಿಮರ್ಗಳನ್ನು ಉತ್ಪಾದಿಸಲು ಎಥಿಲೀನ್ ಅನ್ನು ಬಳಸಲಾಗುತ್ತದೆ.
ಪ್ರೋಪಿಲೀನ್ ಅನ್ನು ಕೆಲವು ಆಲ್ಕೋಹಾಲ್ಗಳ ಉತ್ಪಾದನೆಗೆ ಕಚ್ಚಾ ವಸ್ತುವಾಗಿ ಬಳಸಲಾಗುತ್ತದೆ (ಉದಾಹರಣೆಗೆ, 2-ಪ್ರೊಪನಾಲ್, ಗ್ಲಿಸರಿನ್), ಅಸಿಟೋನ್, ಇತ್ಯಾದಿ. ಪಾಲಿಪ್ರೊಪಿಲೀನ್ ಅನ್ನು ಪ್ರೊಪಿಲೀನ್ ಪಾಲಿಮರೀಕರಣದಿಂದ ಉತ್ಪಾದಿಸಲಾಗುತ್ತದೆ.
ಸಮಸ್ಯೆ ಪರಿಹಾರದ ಉದಾಹರಣೆಗಳು
ಉದಾಹರಣೆ 1
| ವ್ಯಾಯಾಮ | ಜಲವಿಚ್ಛೇದನದ ಸಮಯದಲ್ಲಿ ಜಲೀಯ ದ್ರಾವಣಸೋಡಿಯಂ ಹೈಡ್ರಾಕ್ಸೈಡ್ NaOH ಡೈಕ್ಲೋರೈಡ್, ಎಥಿಲೀನ್ ಹೈಡ್ರೋಕಾರ್ಬನ್ಗೆ 6.72 l ಕ್ಲೋರಿನ್ ಅನ್ನು ಸೇರಿಸುವ ಮೂಲಕ 22.8 ಗ್ರಾಂ ಅನ್ನು ರಚಿಸಲಾಗಿದೆ ಡೈಹೈಡ್ರಿಕ್ ಮದ್ಯ. ಪ್ರತಿಕ್ರಿಯೆಗಳು ಪರಿಮಾಣಾತ್ಮಕ ಇಳುವರಿಯಲ್ಲಿ (ನಷ್ಟವಿಲ್ಲದೆ) ಮುಂದುವರಿಯುತ್ತವೆ ಎಂದು ತಿಳಿದಿದ್ದರೆ ಆಲ್ಕೀನ್ನ ಸೂತ್ರವೇನು? |
| ಪರಿಹಾರ | ಆಲ್ಕೀನ್ ಕ್ಲೋರಿನೀಕರಣಕ್ಕೆ ಸಮೀಕರಣವನ್ನು ಬರೆಯೋಣ ಸಾಮಾನ್ಯ ನೋಟ, ಹಾಗೆಯೇ ಡೈಹೈಡ್ರಿಕ್ ಆಲ್ಕೋಹಾಲ್ ಉತ್ಪಾದಿಸುವ ಪ್ರತಿಕ್ರಿಯೆ: C n H 2 n + Cl 2 = C n H 2 n Cl 2 (1); C n H 2 n Cl 2 + 2NaOH = C n H 2 n (OH) 2 + 2HCl (2). ಕ್ಲೋರಿನ್ ಪ್ರಮಾಣವನ್ನು ಲೆಕ್ಕಾಚಾರ ಮಾಡೋಣ: n(Cl 2) = V(Cl 2) / V m; n(Cl 2) = 6.72 / 22.4 = 0.3 mol, ಆದ್ದರಿಂದ, ಎಥಿಲೀನ್ ಡೈಕ್ಲೋರೈಡ್ 0.3 ಮೋಲ್ (ಸಮೀಕರಣ 1), ಡೈಹೈಡ್ರಿಕ್ ಆಲ್ಕೋಹಾಲ್ ಸಹ 0.3 ಮೋಲ್ ಆಗಿರಬೇಕು ಮತ್ತು ಸಮಸ್ಯೆಯ ಪರಿಸ್ಥಿತಿಗಳ ಪ್ರಕಾರ ಇದು 22.8 ಗ್ರಾಂ ಮೋಲಾರ್ ದ್ರವ್ಯರಾಶಿಇದು ಸಮಾನವಾಗಿರುತ್ತದೆ: M(C n H 2 n (OH) 2) = m (C n H 2 n (OH) 2) / n (C n H 2 n (OH) 2); M(C n H 2 n (OH) 2) = 22.8 / 0.3 = 76 g/mol. ಆಲ್ಕೀನ್ನ ಮೋಲಾರ್ ದ್ರವ್ಯರಾಶಿಯನ್ನು ಕಂಡುಹಿಡಿಯೋಣ: M(C n H 2 n) = 76 - (2×17) = 42 g/mol, ಇದು C 3 H 6 ಸೂತ್ರಕ್ಕೆ ಅನುರೂಪವಾಗಿದೆ. |
| ಉತ್ತರ | ಆಲ್ಕೀನ್ ಸೂತ್ರC 3 H 6 |
ಉದಾಹರಣೆ 2
| ವ್ಯಾಯಾಮ | 16.8 ಗ್ರಾಂ ಆಲ್ಕೀನ್ ಅನ್ನು ಬ್ರೋಮಿನೇಟ್ ಮಾಡಲು ಎಷ್ಟು ಗ್ರಾಂ ಅಗತ್ಯವಿದೆ, ಅದೇ ಪ್ರಮಾಣದ ಆಲ್ಕೀನ್ನ ವೇಗವರ್ಧಕ ಹೈಡ್ರೋಜನೀಕರಣದ ಸಮಯದಲ್ಲಿ, 6.72 ಲೀಟರ್ ಹೈಡ್ರೋಜನ್ ಅನ್ನು ಸೇರಿಸಲಾಯಿತು ಎಂದು ತಿಳಿದಿದ್ದರೆ? ಮೂಲ ಹೈಡ್ರೋಕಾರ್ಬನ್ನ ಸಂಯೋಜನೆ ಮತ್ತು ಸಂಭವನೀಯ ರಚನೆ ಏನು? |
| ಪರಿಹಾರ | ಆಲ್ಕೀನ್ನ ಬ್ರೋಮಿನೇಷನ್ ಮತ್ತು ಹೈಡ್ರೋಜನೀಕರಣದ ಸಮೀಕರಣಗಳನ್ನು ನಾವು ಸಾಮಾನ್ಯ ರೂಪದಲ್ಲಿ ಬರೆಯೋಣ: C n H 2 n + Br 2 = C n H 2 n Br 2 (1); C n H 2 n + H 2 = C n H 2 n +2 (2). ಹೈಡ್ರೋಜನ್ ವಸ್ತುವಿನ ಪ್ರಮಾಣವನ್ನು ಲೆಕ್ಕಾಚಾರ ಮಾಡೋಣ: n(H 2) = V(H 2) / V m; n(H 2) = 6.72 / 22.4 = 0.3 mol, ಆದ್ದರಿಂದ, ಆಲ್ಕೀನ್ 0.3 ಮೋಲ್ (ಸಮೀಕರಣ 2) ಆಗಿರುತ್ತದೆ ಮತ್ತು ಸಮಸ್ಯೆಯ ಪರಿಸ್ಥಿತಿಗಳ ಪ್ರಕಾರ ಇದು 16.8 ಗ್ರಾಂ ಆಗಿರುತ್ತದೆ ಇದರರ್ಥ ಅದರ ಮೋಲಾರ್ ದ್ರವ್ಯರಾಶಿಯು ಸಮಾನವಾಗಿರುತ್ತದೆ: M(C n H 2n) = m(C n H 2n) / n(C n H 2n); M(C n H 2 n) = 16.8 / 0.3 = 56 g/mol, ಇದು C 4 H 8 ಸೂತ್ರಕ್ಕೆ ಅನುರೂಪವಾಗಿದೆ. ಸಮೀಕರಣದ ಪ್ರಕಾರ (1) n (C n H 2 n) : n (Br 2) = 1:1, ಅಂದರೆ. n(Br 2) = n(C n H 2 n) = 0.3 mol. ಬ್ರೋಮಿನ್ ದ್ರವ್ಯರಾಶಿಯನ್ನು ಕಂಡುಹಿಡಿಯೋಣ: m(Br 2) = n(Br 2) × M(Br 2); M(Br 2) = 2×Ar(Br) = 2×80 = 160 g/mol; m(MnO 2) = 0.3 × 160 = 48 ಗ್ರಾಂ. ಐಸೋಮರ್ಗಳ ರಚನಾತ್ಮಕ ಸೂತ್ರಗಳನ್ನು ರಚಿಸೋಣ: ಬ್ಯೂಟಿನ್ -1 (1), ಬ್ಯೂಟಿನ್ -2 (2), 2-ಮೀಥೈಲ್ಪ್ರೊಪೀನ್ (3), ಸೈಕ್ಲೋಬುಟೇನ್ (4). CH 2 =CH-CH 2 -CH 3 (1); CH 3 -CH=CH-CH 3 (2); CH 2 =C(CH 3)-CH 3 (3); |
| ಉತ್ತರ | ಬ್ರೋಮಿನ್ ದ್ರವ್ಯರಾಶಿ 48 ಗ್ರಾಂ |
ಆಲ್ಕೀನ್ಗಳ ಭೌತಿಕ ಗುಣಲಕ್ಷಣಗಳು ಆಲ್ಕೇನ್ಗಳಂತೆಯೇ ಇರುತ್ತವೆ, ಆದರೂ ಅವೆಲ್ಲವೂ ಸ್ವಲ್ಪ ಹೆಚ್ಚು ಕಡಿಮೆ ತಾಪಮಾನಅನುಗುಣವಾದ ಆಲ್ಕೇನ್ಗಳಿಗಿಂತ ಕರಗುವಿಕೆ ಮತ್ತು ಕುದಿಯುತ್ತವೆ. ಉದಾಹರಣೆಗೆ, ಪೆಂಟೇನ್ 36 °C ಮತ್ತು ಪೆಂಟೆನ್-1 - 30 °C ಕುದಿಯುವ ಬಿಂದುವನ್ನು ಹೊಂದಿರುತ್ತದೆ. ಸಾಮಾನ್ಯ ಪರಿಸ್ಥಿತಿಗಳಲ್ಲಿ, ಆಲ್ಕೀನ್ಗಳು C 2 - C 4 ಅನಿಲಗಳು. C 5 - C 15 ದ್ರವಗಳು, C 16 ರಿಂದ ಪ್ರಾರಂಭವಾಗುವ ಘನಗಳು. ಆಲ್ಕೀನ್ಗಳು ನೀರಿನಲ್ಲಿ ಕರಗುವುದಿಲ್ಲ ಆದರೆ ಸಾವಯವ ದ್ರಾವಕಗಳಲ್ಲಿ ಹೆಚ್ಚು ಕರಗುತ್ತವೆ.
ಆಲ್ಕೀನ್ಗಳು ಪ್ರಕೃತಿಯಲ್ಲಿ ಅಪರೂಪ. ಆಲ್ಕೀನ್ಗಳು ಕೈಗಾರಿಕೆಗಳಿಗೆ ಬೆಲೆಬಾಳುವ ಕಚ್ಚಾ ವಸ್ತುಗಳಾಗಿರುವುದರಿಂದ ಸಾವಯವ ಸಂಶ್ಲೇಷಣೆ, ಅವುಗಳನ್ನು ಪಡೆಯಲು ಹಲವು ಮಾರ್ಗಗಳನ್ನು ಅಭಿವೃದ್ಧಿಪಡಿಸಲಾಗಿದೆ.
1. ಆಲ್ಕೀನ್ಗಳ ಮುಖ್ಯ ಕೈಗಾರಿಕಾ ಮೂಲವೆಂದರೆ ತೈಲದ ಭಾಗವಾಗಿರುವ ಆಲ್ಕೇನ್ಗಳ ಬಿರುಕುಗಳು:
3. ಬಿ ಪ್ರಯೋಗಾಲಯದ ಪರಿಸ್ಥಿತಿಗಳುಆಲ್ಕೀನ್ಗಳನ್ನು ಎಲಿಮಿನೇಷನ್ ಕ್ರಿಯೆಗಳಿಂದ ಪಡೆಯಲಾಗುತ್ತದೆ, ಇದರಲ್ಲಿ ಎರಡು ಪರಮಾಣುಗಳು ಅಥವಾ ಎರಡು ಗುಂಪುಗಳ ಪರಮಾಣುಗಳು ನೆರೆಯ ಇಂಗಾಲದ ಪರಮಾಣುಗಳಿಂದ ಹೊರಹಾಕಲ್ಪಡುತ್ತವೆ ಮತ್ತು ಹೆಚ್ಚುವರಿ p-ಬಂಧವು ರೂಪುಗೊಳ್ಳುತ್ತದೆ. ಅಂತಹ ಪ್ರತಿಕ್ರಿಯೆಗಳು ಈ ಕೆಳಗಿನವುಗಳನ್ನು ಒಳಗೊಂಡಿವೆ.
1) ಆಲ್ಕೋಹಾಲ್ಗಳ ನಿರ್ಜಲೀಕರಣವು ನೀರನ್ನು ತೆಗೆಯುವ ಏಜೆಂಟ್ಗಳೊಂದಿಗೆ ಬಿಸಿ ಮಾಡಿದಾಗ ಸಂಭವಿಸುತ್ತದೆ, ಉದಾಹರಣೆಗೆ 150 ° C ಗಿಂತ ಹೆಚ್ಚಿನ ತಾಪಮಾನದಲ್ಲಿ ಸಲ್ಫ್ಯೂರಿಕ್ ಆಮ್ಲದೊಂದಿಗೆ:
ಆಲ್ಕೋಹಾಲ್ಗಳಿಂದ H 2 O, ಆಲ್ಕೈಲ್ ಹಾಲೈಡ್ಗಳಿಂದ HBr ಮತ್ತು HCl ಗಳನ್ನು ಹೊರಹಾಕಿದಾಗ, ಹೈಡ್ರೋಜನ್ ಪರಮಾಣುಗಳನ್ನು ಬಂಧಿತವಾಗಿರುವ ನೆರೆಯ ಇಂಗಾಲದ ಪರಮಾಣುಗಳಿಂದ ಆದ್ಯತೆಯಿಂದ ಹೊರಹಾಕಲಾಗುತ್ತದೆ. ಚಿಕ್ಕ ಸಂಖ್ಯೆಹೈಡ್ರೋಜನ್ ಪರಮಾಣುಗಳು (ಕನಿಷ್ಠ ಹೈಡ್ರೋಜನೀಕರಿಸಿದ ಇಂಗಾಲದ ಪರಮಾಣುವಿನಿಂದ). ಈ ಮಾದರಿಯನ್ನು ಜೈಟ್ಸೆವ್ ನಿಯಮ ಎಂದು ಕರೆಯಲಾಗುತ್ತದೆ.
3) ಪಕ್ಕದ ಕಾರ್ಬನ್ ಪರಮಾಣುಗಳಲ್ಲಿ ಹ್ಯಾಲೊಜೆನ್ ಪರಮಾಣುಗಳನ್ನು ಹೊಂದಿರುವ ಡೈಹಲೈಡ್ಗಳನ್ನು ಸಕ್ರಿಯ ಲೋಹಗಳೊಂದಿಗೆ ಬಿಸಿ ಮಾಡಿದಾಗ ಡಿಹಲೋಜೆನೇಶನ್ ಸಂಭವಿಸುತ್ತದೆ:
CH 2 Br -CHBr -CH 3 + Mg → CH 2 =CH-CH 3 + Mg Br 2.
ಆಲ್ಕೀನ್ಗಳ ರಾಸಾಯನಿಕ ಗುಣಲಕ್ಷಣಗಳನ್ನು ಅವುಗಳ ಅಣುಗಳಲ್ಲಿ ಎರಡು ಬಂಧದ ಉಪಸ್ಥಿತಿಯಿಂದ ನಿರ್ಧರಿಸಲಾಗುತ್ತದೆ. ಎಲೆಕ್ಟ್ರಾನ್ ಸಾಂದ್ರತೆ p-ಬಂಧಗಳು ಸಾಕಷ್ಟು ಮೊಬೈಲ್ ಆಗಿರುತ್ತವೆ ಮತ್ತು ಎಲೆಕ್ಟ್ರೋಫಿಲಿಕ್ ಕಣಗಳೊಂದಿಗೆ ಸುಲಭವಾಗಿ ಪ್ರತಿಕ್ರಿಯಿಸುತ್ತವೆ. ಆದ್ದರಿಂದ, ಆಲ್ಕೀನ್ಗಳ ಅನೇಕ ಪ್ರತಿಕ್ರಿಯೆಗಳು ಕಾರ್ಯವಿಧಾನದ ಪ್ರಕಾರ ಮುಂದುವರಿಯುತ್ತವೆ ಎಲೆಕ್ಟ್ರೋಫಿಲಿಕ್ ಸೇರ್ಪಡೆ, ಎ ಇ ಚಿಹ್ನೆಯಿಂದ ಗೊತ್ತುಪಡಿಸಲಾಗಿದೆ (ಇಂಗ್ಲಿಷ್ನಿಂದ, ಸೇರ್ಪಡೆ ಎಲೆಕ್ಟ್ರೋಫಿಲಿಕ್). ಎಲೆಕ್ಟ್ರೋಫಿಲಿಕ್ ಸೇರ್ಪಡೆ ಪ್ರತಿಕ್ರಿಯೆಗಳು ಹಲವಾರು ಹಂತಗಳಲ್ಲಿ ಸಂಭವಿಸುವ ಅಯಾನಿಕ್ ಪ್ರಕ್ರಿಯೆಗಳಾಗಿವೆ.
ಮೊದಲ ಹಂತದಲ್ಲಿ, ಎಲೆಕ್ಟ್ರೋಫಿಲಿಕ್ ಕಣ (ಹೆಚ್ಚಾಗಿ ಇದು H + ಪ್ರೋಟಾನ್) ಡಬಲ್ ಬಾಂಡ್ನ p-ಎಲೆಕ್ಟ್ರಾನ್ಗಳೊಂದಿಗೆ ಸಂವಹಿಸುತ್ತದೆ ಮತ್ತು p-ಸಂಕೀರ್ಣವನ್ನು ರೂಪಿಸುತ್ತದೆ, ನಂತರ ಇದು ನಡುವೆ ಕೋವೆಲನ್ಸಿಯ s-ಬಂಧವನ್ನು ರೂಪಿಸುವ ಮೂಲಕ ಕಾರ್ಬೋಕೇಶನ್ ಆಗಿ ಪರಿವರ್ತಿಸಲಾಗುತ್ತದೆ. ಎಲೆಕ್ಟ್ರೋಫಿಲಿಕ್ ಕಣ ಮತ್ತು ಇಂಗಾಲದ ಪರಮಾಣುಗಳಲ್ಲಿ ಒಂದಾಗಿದೆ:
ಆಲ್ಕೀನ್ ಪಿ-ಕಾಂಪ್ಲೆಕ್ಸ್ ಕಾರ್ಬೋಕೇಶನ್
ಎರಡನೇ ಹಂತದಲ್ಲಿ, ಕಾರ್ಬೋಕೇಶನ್ X - anion ನೊಂದಿಗೆ ಪ್ರತಿಕ್ರಿಯಿಸುತ್ತದೆ, ಅಯಾನಿನ ಎಲೆಕ್ಟ್ರಾನ್ ಜೋಡಿಯಿಂದಾಗಿ ಎರಡನೇ s-ಬಂಧವನ್ನು ರೂಪಿಸುತ್ತದೆ:

ಎಲೆಕ್ಟ್ರೋಫಿಲಿಕ್ ಸೇರ್ಪಡೆಯ ಪ್ರತಿಕ್ರಿಯೆಗಳಲ್ಲಿ, ಹೈಡ್ರೋಜನ್ ಅಯಾನು ಇಂಗಾಲದ ಪರಮಾಣುವಿಗೆ ಡಬಲ್ ಬಾಂಡ್ನಲ್ಲಿ ಅಂಟಿಕೊಳ್ಳುತ್ತದೆ, ಅದು ದೊಡ್ಡ ಸಂಖ್ಯೆಯ ಕಾರ್ಬನ್ ಪರಮಾಣುಗಳನ್ನು ಹೊಂದಿರುತ್ತದೆ. ಋಣಾತ್ಮಕ ಶುಲ್ಕ. ಬದಲಿಗಳ ಪ್ರಭಾವದ ಅಡಿಯಲ್ಲಿ p-ಎಲೆಕ್ಟ್ರಾನ್ ಸಾಂದ್ರತೆಯ ಬದಲಾವಣೆಯಿಂದ ಚಾರ್ಜ್ ವಿತರಣೆಯನ್ನು ನಿರ್ಧರಿಸಲಾಗುತ್ತದೆ:  .
.
+I ಪರಿಣಾಮವನ್ನು ಪ್ರದರ್ಶಿಸುವ ಎಲೆಕ್ಟ್ರಾನ್-ದಾನದ ಬದಲಿಗಳು p-ಎಲೆಕ್ಟ್ರಾನ್ ಸಾಂದ್ರತೆಯನ್ನು ಹೆಚ್ಚು ಹೈಡ್ರೋಜನೀಕರಿಸಿದ ಇಂಗಾಲದ ಪರಮಾಣುವಿಗೆ ಬದಲಾಯಿಸುತ್ತವೆ ಮತ್ತು ಅದರ ಮೇಲೆ ಭಾಗಶಃ ಋಣಾತ್ಮಕ ಚಾರ್ಜ್ ಅನ್ನು ರಚಿಸುತ್ತವೆ. ಇದು ವಿವರಿಸುತ್ತದೆ ಮಾರ್ಕೊವ್ನಿಕೋವ್ ಅವರ ನಿಯಮ: HX (X = Hal, OH, CN, ಇತ್ಯಾದಿ) ನಂತಹ ಧ್ರುವೀಯ ಅಣುಗಳನ್ನು ಅಸಮಪಾರ್ಶ್ವದ ಆಲ್ಕೀನ್ಗಳಿಗೆ ಸೇರಿಸಿದಾಗ, ಹೈಡ್ರೋಜನ್ ಆದ್ಯತೆಯಾಗಿ ಡಬಲ್ ಬಾಂಡ್ನಲ್ಲಿ ಹೆಚ್ಚು ಹೈಡ್ರೋಜನೀಕರಿಸಿದ ಇಂಗಾಲದ ಪರಮಾಣುವಿಗೆ ಅಂಟಿಕೊಳ್ಳುತ್ತದೆ.
ಪರಿಗಣಿಸೋಣ ನಿರ್ದಿಷ್ಟ ಉದಾಹರಣೆಗಳುಸೇರ್ಪಡೆ ಪ್ರತಿಕ್ರಿಯೆಗಳು.
1) ಹೈಡ್ರೋಹಲೋಜೆನೇಷನ್. ಆಲ್ಕೀನ್ಗಳು ಹೈಡ್ರೋಜನ್ ಹಾಲೈಡ್ಗಳೊಂದಿಗೆ (HCl, HBr) ಸಂವಹನ ನಡೆಸಿದಾಗ, ಆಲ್ಕೈಲ್ ಹಾಲೈಡ್ಗಳು ರೂಪುಗೊಳ್ಳುತ್ತವೆ:
CH 3 -CH = CH 2 + HBr ® CH 3 -CHBr-CH 3 .
ಪ್ರತಿಕ್ರಿಯೆ ಉತ್ಪನ್ನಗಳನ್ನು ಮಾರ್ಕೊವ್ನಿಕೋವ್ ನಿಯಮದಿಂದ ನಿರ್ಧರಿಸಲಾಗುತ್ತದೆ.
ಆದಾಗ್ಯೂ, ಯಾವುದೇ ಉಪಸ್ಥಿತಿಯಲ್ಲಿ ಅದನ್ನು ಒತ್ತಿಹೇಳಬೇಕು ಸಾವಯವ ಪೆರಾಕ್ಸೈಡ್ಧ್ರುವೀಯ HX ಅಣುಗಳು ಮಾರ್ಕೊವ್ನಿಕೋವ್ ನಿಯಮದ ಪ್ರಕಾರ ಆಲ್ಕೀನ್ಗಳೊಂದಿಗೆ ಪ್ರತಿಕ್ರಿಯಿಸುತ್ತವೆ:
| ಆರ್-ಒ-ಆರ್ | ||
| CH 3 -CH = CH 2 + HBr | CH 3 -CH 2 -CH 2 Br |
ಪೆರಾಕ್ಸೈಡ್ ಇರುವಿಕೆಯು ಆಮೂಲಾಗ್ರವನ್ನು ಉಂಟುಮಾಡುತ್ತದೆ ಎಂಬ ಅಂಶದಿಂದಾಗಿ ಇದು ಸಂಭವಿಸುತ್ತದೆ ಅಯಾನು ಯಾಂತ್ರಿಕತೆಪ್ರತಿಕ್ರಿಯೆಗಳು.
2) ಜಲಸಂಚಯನ. ಖನಿಜ ಆಮ್ಲಗಳ (ಸಲ್ಫ್ಯೂರಿಕ್, ಫಾಸ್ಪರಿಕ್) ಉಪಸ್ಥಿತಿಯಲ್ಲಿ ಆಲ್ಕೀನ್ಗಳು ನೀರಿನೊಂದಿಗೆ ಪ್ರತಿಕ್ರಿಯಿಸಿದಾಗ, ಆಲ್ಕೋಹಾಲ್ಗಳು ರೂಪುಗೊಳ್ಳುತ್ತವೆ. ಖನಿಜ ಆಮ್ಲಗಳುವೇಗವರ್ಧಕಗಳಾಗಿ ಕಾರ್ಯನಿರ್ವಹಿಸುತ್ತವೆ ಮತ್ತು ಪ್ರೋಟಾನ್ಗಳ ಮೂಲಗಳಾಗಿವೆ. ನೀರಿನ ಸೇರ್ಪಡೆಯು ಮಾರ್ಕೊವ್ನಿಕೋವ್ ಅವರ ನಿಯಮವನ್ನು ಅನುಸರಿಸುತ್ತದೆ:
CH 3 -CH = CH 2 + HON ® CH 3 -CH (OH) -CH 3 .
3) ಹ್ಯಾಲೊಜೆನೇಶನ್. ಆಲ್ಕೀನ್ಗಳು ಬ್ರೋಮಿನ್ ನೀರಿನ ಬಣ್ಣವನ್ನು ಬದಲಾಯಿಸುತ್ತವೆ:
CH 2 = CH 2 + Br 2 ® B-CH 2 -CH 2 Br.
ಈ ಪ್ರತಿಕ್ರಿಯೆಯು ಡಬಲ್ ಬಾಂಡ್ಗೆ ಗುಣಾತ್ಮಕವಾಗಿದೆ.
4) ಹೈಡ್ರೋಜನೀಕರಣ. ಲೋಹದ ವೇಗವರ್ಧಕಗಳ ಕ್ರಿಯೆಯ ಅಡಿಯಲ್ಲಿ ಹೈಡ್ರೋಜನ್ ಸೇರ್ಪಡೆ ಸಂಭವಿಸುತ್ತದೆ:
ಅಲ್ಲಿ R = H, CH 3, Cl, C 6 H 5, ಇತ್ಯಾದಿ. CH 2 =CHR ಅಣುವನ್ನು ಮೊನೊಮರ್ ಎಂದು ಕರೆಯಲಾಗುತ್ತದೆ, ಪರಿಣಾಮವಾಗಿ ಸಂಯುಕ್ತವನ್ನು ಪಾಲಿಮರ್ ಎಂದು ಕರೆಯಲಾಗುತ್ತದೆ, ಸಂಖ್ಯೆ n ಪಾಲಿಮರೀಕರಣದ ಮಟ್ಟವಾಗಿದೆ.
ವಿವಿಧ ಆಲ್ಕೀನ್ ಉತ್ಪನ್ನಗಳ ಪಾಲಿಮರೀಕರಣವು ಮೌಲ್ಯಯುತವಾಗಿದೆ ಕೈಗಾರಿಕಾ ಉತ್ಪನ್ನಗಳು: ಪಾಲಿಥಿಲೀನ್, ಪಾಲಿಪ್ರೊಪಿಲೀನ್, ಪಾಲಿವಿನೈಲ್ ಕ್ಲೋರೈಡ್ ಮತ್ತು ಇತರರು.
ಜೊತೆಗೆ, ಆಲ್ಕೀನ್ಗಳು ಆಕ್ಸಿಡೀಕರಣ ಕ್ರಿಯೆಗಳಿಗೆ ಒಳಗಾಗುತ್ತವೆ. ಪೊಟ್ಯಾಸಿಯಮ್ ಪರ್ಮಾಂಗನೇಟ್ (ವ್ಯಾಗ್ನರ್ ಪ್ರತಿಕ್ರಿಯೆ) ನ ಜಲೀಯ ದ್ರಾವಣದೊಂದಿಗೆ ಆಲ್ಕೀನ್ಗಳ ಸೌಮ್ಯ ಆಕ್ಸಿಡೀಕರಣದ ಸಮಯದಲ್ಲಿ, ಡೈಹೈಡ್ರಿಕ್ ಆಲ್ಕೋಹಾಲ್ಗಳು ರೂಪುಗೊಳ್ಳುತ್ತವೆ:
ZSN 2 =CH 2 + 2KMn O 4 + 4H 2 O ® ZNOSN 2 -CH 2 OH + 2MnO 2 ↓ + 2KOH.
ಈ ಪ್ರತಿಕ್ರಿಯೆಯ ಪರಿಣಾಮವಾಗಿ, ಪೊಟ್ಯಾಸಿಯಮ್ ಪರ್ಮಾಂಗನೇಟ್ನ ನೇರಳೆ ದ್ರಾವಣವು ತ್ವರಿತವಾಗಿ ಬಣ್ಣಕ್ಕೆ ತಿರುಗುತ್ತದೆ ಮತ್ತು ಮ್ಯಾಂಗನೀಸ್ (IV) ಆಕ್ಸೈಡ್ನ ಕಂದು ಅವಕ್ಷೇಪವು ಅವಕ್ಷೇಪಿಸುತ್ತದೆ. ಈ ಪ್ರತಿಕ್ರಿಯೆಯು, ಬ್ರೋಮಿನ್ ನೀರಿನ ಡಿಕಲರ್ಟೈಸೇಶನ್ ಪ್ರತಿಕ್ರಿಯೆಯಂತೆ, ಡಬಲ್ ಬಾಂಡ್ಗೆ ಗುಣಾತ್ಮಕವಾಗಿದೆ. ಆಮ್ಲೀಯ ವಾತಾವರಣದಲ್ಲಿ ಪೊಟ್ಯಾಸಿಯಮ್ ಪರ್ಮಾಂಗನೇಟ್ನ ಕುದಿಯುವ ದ್ರಾವಣದೊಂದಿಗೆ ಆಲ್ಕೆನ್ಗಳ ತೀವ್ರ ಆಕ್ಸಿಡೀಕರಣದ ಸಮಯದಲ್ಲಿ, ಎರಡು ಬಂಧದ ಸಂಪೂರ್ಣ ಸೀಳುವಿಕೆಯು ಕೀಟೋನ್ಗಳ ರಚನೆಯೊಂದಿಗೆ ಸಂಭವಿಸುತ್ತದೆ, ಕಾರ್ಬಾಕ್ಸಿಲಿಕ್ ಆಮ್ಲಗಳುಅಥವಾ CO 2, ಉದಾಹರಣೆಗೆ:
| [ಸುಮಾರು] | ||
| CH 3 -CH=CH-CH 3 | 2CH 3 -COOH |
ಆಕ್ಸಿಡೀಕರಣ ಉತ್ಪನ್ನಗಳ ಆಧಾರದ ಮೇಲೆ, ಮೂಲ ಆಲ್ಕೀನ್ನಲ್ಲಿ ಡಬಲ್ ಬಾಂಡ್ನ ಸ್ಥಾನವನ್ನು ನಿರ್ಧರಿಸಬಹುದು.
ಎಲ್ಲಾ ಇತರ ಹೈಡ್ರೋಕಾರ್ಬನ್ಗಳಂತೆ, ಆಲ್ಕೀನ್ಗಳು ಉರಿಯುತ್ತವೆ ಮತ್ತು ಸಾಕಷ್ಟು ಗಾಳಿಯೊಂದಿಗೆ ಇಂಗಾಲದ ಡೈಆಕ್ಸೈಡ್ ಮತ್ತು ನೀರನ್ನು ರೂಪಿಸುತ್ತವೆ:
C n H 2 n + Zn /2O 2 ® n CO 2 + n H 2 O.
ಗಾಳಿಯು ಸೀಮಿತವಾದಾಗ, ಆಲ್ಕೀನ್ಗಳ ದಹನವು ಇಂಗಾಲದ ಮಾನಾಕ್ಸೈಡ್ ಮತ್ತು ನೀರಿನ ರಚನೆಗೆ ಕಾರಣವಾಗಬಹುದು:
C n H 2n + nO 2 ® nCO + nH 2 O .
ನೀವು ಆಲ್ಕೀನ್ ಅನ್ನು ಆಮ್ಲಜನಕದೊಂದಿಗೆ ಬೆರೆಸಿದರೆ ಮತ್ತು ಈ ಮಿಶ್ರಣವನ್ನು ಬೆಳ್ಳಿ ವೇಗವರ್ಧಕದ ಮೇಲೆ 200 ° C ಗೆ ಬಿಸಿಮಾಡಿದರೆ, ಆಲ್ಕೀನ್ ಆಕ್ಸೈಡ್ (ಎಪಾಕ್ಸಿಯಾಲ್ಕೇನ್) ರೂಪುಗೊಳ್ಳುತ್ತದೆ, ಉದಾಹರಣೆಗೆ:

ಯಾವುದೇ ತಾಪಮಾನದಲ್ಲಿ, ಆಲ್ಕೀನ್ಗಳು ಓಝೋನ್ನಿಂದ ಆಕ್ಸಿಡೀಕರಣಗೊಳ್ಳುತ್ತವೆ (ಓಝೋನ್ ಆಮ್ಲಜನಕಕ್ಕಿಂತ ಪ್ರಬಲವಾದ ಆಕ್ಸಿಡೈಸಿಂಗ್ ಏಜೆಂಟ್). ಕೋಣೆಯ ಉಷ್ಣಾಂಶಕ್ಕಿಂತ ಕಡಿಮೆ ತಾಪಮಾನದಲ್ಲಿ ಓಝೋನ್ ಅನಿಲವನ್ನು ಮೀಥೇನ್ ಟೆಟ್ರಾಕ್ಲೋರೈಡ್ನಲ್ಲಿರುವ ಆಲ್ಕೀನ್ ದ್ರಾವಣದ ಮೂಲಕ ಹಾದು ಹೋದರೆ, ಒಂದು ಸಂಕಲನ ಕ್ರಿಯೆಯು ಸಂಭವಿಸುತ್ತದೆ ಮತ್ತು ಅನುಗುಣವಾದ ಓಝೋನೈಡ್ಗಳು (ಸೈಕ್ಲಿಕ್ ಪೆರಾಕ್ಸೈಡ್ಗಳು) ರೂಪುಗೊಳ್ಳುತ್ತವೆ. ಓಝೋನೈಡ್ಗಳು ತುಂಬಾ ಅಸ್ಥಿರವಾಗಿರುತ್ತವೆ ಮತ್ತು ಸುಲಭವಾಗಿ ಸ್ಫೋಟಿಸಬಹುದು. ಆದ್ದರಿಂದ, ಅವು ಸಾಮಾನ್ಯವಾಗಿ ಪ್ರತ್ಯೇಕವಾಗಿರುವುದಿಲ್ಲ, ಆದರೆ ಉತ್ಪಾದನೆಯ ನಂತರ ತಕ್ಷಣವೇ ಅವು ನೀರಿನಿಂದ ಕೊಳೆಯುತ್ತವೆ - ಇದು ಉತ್ಪಾದಿಸುತ್ತದೆ ಕಾರ್ಬೊನಿಲ್ ಸಂಯುಕ್ತಗಳು(ಆಲ್ಡಿಹೈಡ್ಗಳು ಅಥವಾ ಕೀಟೋನ್ಗಳು), ಇದರ ರಚನೆಯು ಓಝೋನೇಷನ್ಗೆ ಒಳಪಟ್ಟ ಆಲ್ಕೀನ್ನ ರಚನೆಯನ್ನು ಸೂಚಿಸುತ್ತದೆ.
ಲೋವರ್ ಆಲ್ಕೀನ್ಗಳು ಕೈಗಾರಿಕಾ ಸಾವಯವ ಸಂಶ್ಲೇಷಣೆಗೆ ಪ್ರಮುಖ ಆರಂಭಿಕ ವಸ್ತುಗಳಾಗಿವೆ. ಎಥಿಲೀನ್ ನಿಂದ ಇದನ್ನು ಪಡೆಯಲಾಗುತ್ತದೆ ಎಥೆನಾಲ್, ಪಾಲಿಥಿಲೀನ್, ಪಾಲಿಸ್ಟೈರೀನ್. ಪಾಲಿಪ್ರೊಪಿಲೀನ್, ಫೀನಾಲ್, ಅಸಿಟೋನ್ ಮತ್ತು ಗ್ಲಿಸರಾಲ್ ಸಂಶ್ಲೇಷಣೆಗಾಗಿ ಪ್ರೊಪೀನ್ ಅನ್ನು ಬಳಸಲಾಗುತ್ತದೆ.
