НЕПРЕДЕЛЬНЫЕ, ИЛИ НЕНАСЫЩЕННЫЕ, УГЛЕВОДОРОДЫ РЯДА ЭТИЛЕНА
(АЛКЕНЫ, ИЛИ ОЛЕФИНЫ)
Алкены , или олефины (от лат. olefiant - масло - старое название, но широко используемое в химической литературе. Поводом к такому названию послужил хлористый этилен, полученный в XVIII столетии, - жидкое маслянист вещество.) - алифатические непредельные углеводороды, в молекулах которых между углеродными атомами имеется одна двойная связь.
Алкены содержат в своей молекуле меньшее число водородных атомов, чем соответствующие им алканы (с тем же числом углеродных атомов), поэтому такие углеводороды называют непредельными или ненасыщенными.
Алкены образуют гомологический ряд с общей формулой C n H 2n
1. Гомологический ряд алкенов
|
С n H 2 n алкен |
Названия, суффикс ЕН, ИЛЕН |
|
C 2 Н 4 |
этен , этилен |
|
C 3 H 6 |
пропен |
|
C 4 H 8 |
бутен |
|
C 5 H 10 |
пентен |
|
C 6 H 12 |
гексен |
Гомологи:
С H 2 = CH 2 этен
С H 2 = CH - CH 3 пропен
С H 2 =CH-CH 2 -CH 3 бутен -1
С H 2 =CH-CH 2 -CH 2 - СН 3 пентен -1
2. Физические свойства
Этилен (этен) – бесцветный газ с очень слабым сладковатым запахом, немного легче воздуха, малорастворим в воде.
С 2 – С 4 (газы)
С 5 – С 17 (жидкости)
С 18 – (твёрдые)
· Алкены не растворяются в воде, растворимы в органических растворителях (бензин, бензол и др.)
· Легче воды
· С увеличением Mr температуры плавления и кипения увеличиваются
3. Простейшим алкеном является этилен - C 2 H 4
Структурная
и электронная формулы этилена имеют вид:
В молекуле этилена подвергаются
гибридизации одна s
- и две p
-орбитали атомов C (sp
2 -гибридизация).
Таким образом, каждый атом C имеет по три гибридных орбитали и по одной негибридной p -орбитали. Две из гибридных орбиталей атомов C взаимно перекрываются и образуют между атомами C
σ - связь. Остальные четыре гибридных орбитали атомов C перекрываются в той же плоскости с четырьмя s -орбиталями атомов H и также образуют четыре σ - связь. Две негибридные p -орбитали атомов C взаимно перекрываются в плоскости, которая расположена перпендикулярно плоскости σ - связь, т.е. образуется одна П - связь.

По своей природе П - связь резко отличается от σ - связь; П - связь менее прочная вследствие перекрывания электронных облаков вне плоскости молекулы. Под действием реагентов П - связь легко разрывается.
Молекула этилена симметрична; ядра всех атомов расположены в одной плоскости и валентные углы близки к 120°; расстояние между центрами атомов C равно 0,134 нм.
Если атомы соединены двойной связью, то их вращение невозможно без того, чтобы электронные облака П - связь не разомкнулись.
4. Изомерия алкенов
Наряду со структурной изомерией углеродного скелета для алкенов характерны, во-первых, другие разновидности структурной изомерии - изомерия положения кратной связи и межклассовая изомерия .
Во-вторых, в ряду алкенов проявляется пространственная изомерия , связанная с различным положением заместителей относительно двойной связи, вокруг которой невозможно внутримолекулярное вращение.
Структурная изомерия алкенов
1. Изомерия углеродного скелета (начиная с С 4 Н 8):
2. Изомерия положения двойной связи (начиная с С 4 Н 8):
3. Межклассовая изомерия с циклоалканами, начиная с С 3 Н 6:
Пространственная изомерия алкенов
Вращение атомов вокруг двойной связи невозможно без ее разрыва. Это обусловлено особенностями строения p-связи (p-электронное облако сосредоточено над и под плоскостью молекулы). Вследствие жесткой закрепленности атомов поворотная изомерия относительно двойной связи не проявляется. Но становится возможной цис -транс -изомерия.
Алкены, имеющие у каждого из двух атомов углерода при двойной связи различные заместители, могут существовать в виде двух пространственных изомеров, отличающихся расположением заместителей относительно плоскости p-связи. Так, в молекуле бутена-2 СН 3 –СН=СН–СН 3 группы СН 3 могут находиться либо по одну сторону от двойной связи в цис -изомере, либо по разные стороны в транс -изомере.

ВНИМАНИЕ!
цис-транс
- Изомерия не проявляется, если хотя бы один из атомов С
при двойной связи имеет 2 одинаковых заместителя.
Например,
бутен-1 СН 2 =СН–СН 2 –СН 3 не имеет цис - и транс -изомеров, т.к. 1-й атом С связан с двумя одинаковыми атомами Н.
Изомеры цис - и транс - отличаются не только физическими
 ,
,
но и химическими свойствами, т.к. сближение или удаление частей молекулы друг от друга в пространстве способствует или препятствует химическому взаимодействию.
Иногда цис-транс -изомерию не совсем точно называют геометрической изомерией . Неточность состоит в том, что все пространственные изомеры различаются своей геометрией, а не только цис - и транс -.
5. Номенклатура
Алкены простого строения часто называют, заменяя суффикс -ан в алканах на -илен: этан - этилен, пропан - пропилен и т.д.
По систематической номенклатуре названия этиленовых углеводородов производят заменой суффикса -ан в соответствующих алканах на суффикс -ен (алкан - алкен, этан - этен, пропан - пропен и т.д.). Выбор главной цепи и порядок названия тот же, что и для алканов. Однако в состав цепи должна обязательно входить двойная связь. Нумерацию цепи начинают с того конца, к которому ближе расположена эта связь. Например:

Непредельные (алкеновые) радикалы называют тривиальными названиями или по систематической номенклатуре:
(Н 2 С=СН-)винил или этенил
(Н 2 С=CН-СН 2) аллил
Общая формула алкенов: C n H 2n (n 2)
Первые представители гомологического ряда алкенов:

Формулы алкенов можно составить из соответствующих формул алканов (предельных углеводородов). Названия алкенов образуют заменой суффикса -ан соответствующего алкана на -ен или –илен: бутан – бутилен, пентан –пентен и т.д. Номер атома углерода с двойной связью обозначается арабской цифрой после названия.
Атомы углерода, участвующие в образовании двойной связи находятся в состоянии sp-гибридизации. Три -связи, образованные гибридными орбиталям и, расположены в одной плоскости под углом 120° друг к другу. Дополнительная -связь образуется путем бокового перекрывания негибридных р-орбиталей:

Длина двойной связи С=С (0,133нм) меньше длины одинарной связи (0,154 нм). Энергия двойной связи меньше удвоенного значения энергии одинарной связи, поскольку энергия -связи меньше энергии -связи.
Изомеры алкенов
Все алкены кроме этилена имеют изомеры. Для алкенов характерна изомерия углеродного скелета, изомерия положения двойной связи, межклассовая и пространственная изомерии.
Межклассовым изомером пропена (C 3 H 6) является циклопропан. Начиная с бутена (C 4 H 8) появляется изомерия по положению двойной связи (бутен-1 и бутен-2), изомерия углеродного скелета (метилпропен или изобутилен), а также пространственная изомерия (цис-бутен-2 и транс-бутен-2). В цис- изомерах заместители расположены по одну сторону, а в транс- изомерах – по разные стороны от двойной связи.
Химические свойства и химическая активность алкенов определяются наличием в их молекулах двойной связи. Для алкенов наиболее характерны реакции электрофильного присоединения: гидрогалогенирование, гидратация, галогенирование, гидрирование, полимеризация.
Качественная реакция на двойную связь – обесцвечивание бромной воды:
Примеры решения задач по теме «формула алкенов»
ПРИМЕР 1
| Задание | Сколько изомеров, способных обесцвечивать бромную воду имеет вещество состава С 3 Н 5 Сl? Напишите структурные формулы этих изомеров |
| Решение | С 3 Н 5 Сl представляет собой монохлорпроизводное от углеводорода С 3 Н 6 . Этой формуле отвечает либо пропен –
углеводород с одной двойной связью, либо циклопропан (циклический углеводород). Данное вещество обесцвечивает бромную воду, значит, в его составе есть двойная связь. Три атома углерода могут образовать только такую структуру:
поскольку изомерия углеродного скелета и положения двойной связи при таком количестве атомов углерода невозможна. Структурная изомерия в данной молекуле возможна только за счет изменения положения атома хлора относительно двойной связи: Для 1-хлорпропена возможна цис-транс-изомерия: |
| Ответ | Условию задачи удовлетворяют 4 изомера |
ПРИМЕР 2
| Задание | Смесь изомерных углеводородов (газов с плотностью по водороду равной 21) объемом 11,2 л (н.у.) вступила в реакцию с бромной водой. В результате было получено 40,4 г соответствующего дибромпроизводного. Какое строение имеют эти углеводороды? Определите их объемное содержание в смеси (в %). |
| Решение | Общая формула углеводородов C х H у.
Рассчитаем молярную массу углеводородов: Следовательно, формула углеводородов – С 3 Н 6 . Такую формулу имеют только два вещества – пропен и циклопропан. С бромной водой реагирует только пропен: Рассчитаем количество вещества дибромпроизводного: По уравнению реакции: n(пропена) моль Суммарное количество углеводородов в смеси равно: |
4. Химические свойства алкенов
Энергия двойной углерод-углеродной связи в этилене (146 ккал/моль) оказывается значительно более низкой, чем удвоенная энергия одинарной С-С-связи в этане (2 88=176 ккал/моль). -Связь С-С в этилене прочнее -связи, поэтому реакции алкенов, сопровождающиеся разрывом -связи с образованием двух новых простых -связей, представляют собой термодинамически благоприятный процесс. Так, например, в газовой фазе согласно расчетным данным все приведенные ниже реакции являются экзотермическими со значительной отрицательной энтальпией, независимо от их реального механизма.
С точки зрения теории молекулярных орбиталей также можно сделать вывод о большей реакционной способности -связи по сравнению с -связью. Рассмотрим молекулярные орбитали этилена (рис. 2).

Действительно, связывающая -орбиталь этилена имеет более высокую энергию, чем связывающая -орбиталь, и наоборот, разрыхляющая *-орбиталь этилена лежит ниже разрыхляющей *-орбитали связи С=С. В обычных условиях *- и *-орбитали этилена вакантны. Следовательно, граничными орбиталями этилена и других алкенов, определяющими их реакционную способность будут -орбитали.
4.1. Каталитическое гидрирование алкенов
Несмотря на то, что гидрирование этилена и других алкенов до алканов, сопровождается выделением тепла, эта реакция с заметной скоростью идет только в присутствии определенных катализаторов. Катализатор, по определению, не влияет на тепловой эффект реакции, и его роль сводится к понижению энергии активации. Следует различать гетерогенное и гомогенное каталитическое гидрирование алкенов. В гетерогенном гидрировании используются тонкоизмельченные металлические катализаторы - платина, палладий, рутений, родий, осмий и никель либо в чистом виде, либо нанесенные на инертные носители - BaSO 4 , CaCO 3 , активированный уголь, Al 2 O 3 и т. д. Все они нерастворимы в органических средах и действуют как гетерогенные катализаторы. Наибольшую активность среди них проявляют рутений и родий, но наибольшее распространение получил платина и никель. Платину обычно применяют в виде черного диоксида PtO 2 , широко известного под названием "катализатора Адамса". Диоксид платины получают при сплавлении платинохлористоводородной кислоты H 2 PtCl 6 . 6H 2 O или гексахлорплатината аммония (NH 4) 2 PtCl 6 с нитратом натрия. Гидрирование алкенов с катализатором Адамса проводят обычно при нормальном давлении и температуре 20-50 0 С в спирте, уксусной кислоте, этилацетате. При пропускании водорода двуокись платины восстанавливается непосредственно в реакционном сосуде до платиновой черни, которая и катализирует гидрирование. Другие более активные металлы платиновой группы используют на инертных носителях, например, Pd/C или Pd/BaSO 4 , Ru/Al 2 O 3 ; Rh/C и др. Палладий, нанесенный на уголь, катализирует гидрирование алкенов до алканов в спиртовом растворе при 0-20 0 С и нормальном давлении. Никель обычно используется в виде так называемого "никеля Ренея". Для получения этого катализатора сплав никеля с алюминием обрабатывают горячей водной щелочью для удаления почти всего алюминия и далее водой до нейтральной реакции. Катализатор имеет пористую структуру, и поэтому называется также скелетным никелевым катализатором. Типичные условия гидрирования алкенов над никелем Ренея требуют применения давления порядка 5-10 атм и температуры 50-100 0 С, т. е. этот катализатор значительно менее активен, чем металлы платиновой группы, но он белее дешев. Ниже приведены некоторые типичные примеры гетерогенного каталитического гидрирования ациклических и циклических алкенов:

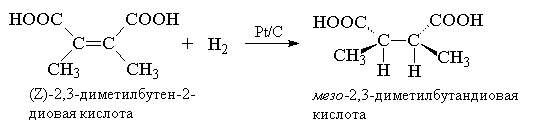
Так как оба атома водорода присоединяются к атомам углерода двойной связи с поверхности металла-катализатора, обычно присоединение происходит с одной стороны двойной связи. Этот тип присоединения называется син -присоединением. В тех случаях когда два фрагмента реагента присоединяются с различных сторон кратной связи (двойной или тройной) имеет место анти -присоединение. Термины син - и анти - по смыслу эквивалентны терминам цис - и транс -. Для того, чтобы избежать путаницы и недоразумений термины син - и анти - относятся к типу присоединения, а термины цис - и транс - к строению субстрата.
Двойная связь в алкенах гидрируется с большей скоростью по сравнению со многими другими функциональными группами (С=О, COOR, CN и др.) и поэтому гидрирование двойной связи С=С часто представляет собой селективный процесс, если гидрирование ведется в мягких условиях (0-20 0 С и при атмосферном давлении). Ниже приведены некоторые типичные примеры:


Бензольное кольцо не восстанавливается в этих условиях.
Большим и принципиально важным достижением в каталитическом гидрировании является открытие растворимых комплексов металлов, которые катализируют гидрирование в гомогенном растворе. Гетерогенное гидрирование на поверхности металлических катализаторов имеет ряд существенных недостатков, таких, как изомеризация алкенов и расщепление одинарных углерод-углеродных связей (гидрогенолиз). Гомогенное гидрирование лишено этих недостатков. За последние годы получена большая группа катализаторов гомогенного гидрирования - комплексов переходных металлов, содержащих различные лиганды. Лучшими катализаторами гомогенного гидрирования являются комплексы хлоридов родия (I) и рутения (III) с трифенилфосфином - трис(трифенилфосфин)родийхлорид (Ph 3 P) 3 RhCl (катализатор Уилкинсона) и гидрохлорид трис(трифенилфосфин)рутения (Ph 3 P) 3 RuHCl. Наиболее доступен родиевый комплекс, который получается при взаимодействии хлорида родия (III) с трифенилфосфином. Родиевый комплекс Уилкинсона используется для гидрирования двойной связи в обычных условиях.

Важное преимущество гомогенных катализаторов заключается в возможности селективного восстановления моно- или дизамещенной двойной связи в присутствии три- и тетразамещенной двойной связи из-за больших различий в скорости их гидрирования.

В случае гомогенных катализаторов присоединение водорода также происходит как син -присоединение. Так восстановление цис -бутена-2 дейтерием в этих условиях приводит к мезо -2,3-дидейтеробутану.

4.2. Восстановление двойной связи с помощью диимида
Восстановление алкенов до соответствующих алканов может быть с успехом осуществлено с помощью диимида NH=NH.
Диимид получают двумя основными методами: окислением гидразина пероксидом водорода в присутствии ионов Cu 2+ или взаимодействием гидразина с Ni-Ренея (дегидрирование гидразина). Если в реакционной смеси присутствует алкен, его двойная связь под действием очень нестабильного диимида подвергается гидрированию. Отличительной особенностью этого метода является строгая син -стереоспецифичность процесса восстановления. Полагают, что эта реакция протекает через циклический активированный комплекс со строгой ориентацией обеих реагирующих молекул в пространстве.

4.3. Реакции электрофильного присоединения по двойной связи алкенов
Граничными орбиталями ВЗМО и НСМО алкенов являются занятая - и пустая *-орбитали. Следовательно, в реакциях с электрофилами (Е +) будет участвовать -орбиталь, а в реакциях с нуклеофилами (Nu -) - *-орбиталь связи С=С (см. рис. 3). В большинстве случаев простые алкены легко вступают в реакции с электрофилами, а с нуклеофилами реагируют с большим трудом. Это объясняется тем, что обычно НСМО большинства электрофилов по энергии близки к энергии -ВЗМО алкенов, тогда как ВЗМО большинства нуклеофилов лежат значительно ниже *-НСМО.

Простые алкены реагируют лишь с очень сильными нуклеофильными агентами (карбанионы) в жестких условиях, однако введение электроноакцепторных групп в алкены, например, NO 2 , COR и др., приводит к понижению *-уровня, благодаря чему алкен приобретает способность реагировать с нуклеофилами средней силы (аммиак, RO - , Nє C - , енолят-анион и т. д.).
В результате взаимодействия электрофильного агента Е + с алкеном образуется карбокатион, обладающий высокой реакционной способностью. Карбокатион далее стабилизируется за счет быстрого присоединения нуклеофильного агента Nu - :


Поскольку медленной стадией является присоединение электрофила, то процесс присоединения любого полярного агента Е + Nu - следует рассматривать именно как электрофильное присоединение к кратной связи алкена. Известно большое число реакций этого типа, где роль электрофильного агента выполняют галогены, галогеноводороды, вода, соли двухвалентной ртути и другие полярные реагенты. Электрофильное присоединение к двойной связи в классификации механизмов органических реакций имеет символ Аd E (Addition Electrophilic ) и в зависимости от числа реагирующих молекул обозначается как Аd E 2 (бимолекулярная реакция) или Аd E 3 (тримолекулярная реакция).
4.3.а. Присоединение галогенов
Алкены реагируют с бромом и хлором с образованием продуктов присоединения по двойной связи одной молекулы галогена с выходом близким к количественному. Фтор слишком активен и вызывает деструкцию алкенов. Присоединение йода к алкенам в большинстве случаев представляет собой обратимую реакцию, равновесие которой смещено в сторону исходных реагентов.


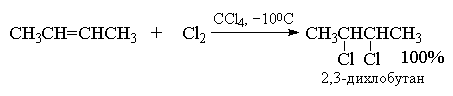
Быстрое обесцвечивание раствора брома в СCl 4 служит одним из простейших тестов на ненасыщенность, поскольку и алкены, и алкины, и диены быстро реагируют с бромом.
Присоединение брома и хлора к алкенам происходит по ионному, а не по радикальному механизму. Этот вывод следует из того, что скорость присоединения галогена не зависит от облучения, присутствия кислорода и других реагентов, инициирующих или ингибирующих радикальные процессы. На основании большого числа экспериментальных данных для этой реакции был предложен механизм, включающий несколько последовательных стадий. На первой стадии происходит поляризация молекулы галогена под действием электронов -связи. Атом галогена, приобретающий некоторый дробный положительный заряд, образует с электронами -связи нестабильный интермедиат, называемый -комплексом или комплексом с переносом заряда. Следует отметить, что в -комплексе галоген не образует направленной связи с каким-нибудь конкретным атомом углерода; в этом комплексе просто реализуется донорно-акцепторное взаимодействие электронной пары -связи как донора и галогена как акцептора.

Далее -комплекс превращается в циклический бромониевый ион. В процессе образования этого циклического катиона происходит гетеролитический разрыв связи Br-Br и пустая р -орбиталь sp 2 -гибридизованного атома углерода перекрывается с р -орбиталью "неподеленной пары" электронов атома галогена, образуя циклический ион бромония.

На последней, третьей стадии анион брома как нуклеофильный агент атакует один из атомов углерода бромониевого иона. Нуклеофильная атака бромид-иона приводит к раскрытию трехчленного цикла и образованию вицинального дибромида (vic -рядом). Эту стадию формально можно рассматривать как нуклеофильное замещение S N 2 у атома углерода, где уходящей группой является Br+ .
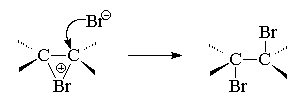
Присоединение галогенов к двойной связи алкенов представляет собой одну из формально простых модельных реакций, на примере которой можно рассмотреть влияние основных факторов, позволяющих сделать аргументированные выводы о детальном механизме процесса. Для обоснованных выводов о механизме любой реакции следует располагать данными по: 1) кинетике реакции; 2) стереохимии (стереохимический результат реакции); 3) наличию или отсутствию сопряженного, конкурирующего процесса; 4) влиянию заместителей в исходном субстрате на скорость реакции; 5) использованию меченых субстратов и (или) реагентов; 6) возможности перегруппировок в ходе реакции; 7) влиянию растворителя на скорость реакции.
Рассмотрим эти факторы на примере галогенирования алкенов. Кинетические данные дают возможность установить порядок реакции по каждому компоненту и на этом основании сделать вывод об общей молекулярности реакции, т. е. о числе реагирующих молекул.
Для бромирования алкенов скорость реакции как правило описывается следующим уравнением:
v = k`[алкен] + k``[алкен] 2 ,
которое в редких случаях упрощается до
v = k`[алкен].
На основании кинетических данных можно сделать вывод о том, что в определяющей скорость стадии принимает участие одна или две молекулы брома. Второй порядок по брому означает, что с бромониевым ионом реагирует не бромид-ион Br - , а трибромид-ион , образующийся при взаимодействии брома и бромид-иона:
![]()
Это равновесие сдвинуто вправо. Кинетические данные не позволяют сделать какие-либо другие выводы о структуре переходного состояния и природе электрофильной частицы в реакции присоединения галогена по двойной связи. Наиболее ценную информацию о механизме этой реакции представляют данные по стереохимии присоединения. Присоединение галогена к двойной связи представляет собой стереоспецифический процесс (процесс, в котором образуется только один из возможных стереоизомеров; в стереоселективном процессе наблюдается преимущественное образование одного стереомера) анти -присоединения для алкенов и циклоалкенов, у которых двойная связь не сопряжена с бензольным кольцом. Для цис - и транс -изомеров бутена-2, пентена-2, гексена-3, циклогексена, циклопентена и других алкенов присоединение брома происходит исключительно как анти -присоединение. При этом в случае циклогексена образуется исключительно транс -1,2-дибромциклогексан (смесь энантиомеров).

Транс-расположение атомов брома в 1,2-дибромциклогексане можно упрощенно изобразить относительно средней плоскости циклогексанового кольца (без учета конформаций ):
При присоединении брома к циклогексену первоначально образуется транс -1,2-дибромциклогексан в а,а -конформации, которая затем сразу же переходит в энергетически более выгодную е,е -конформацию. Анти -присоединение галогенов к двойной связи позволяет отвергнуть механизм одностадийного синхронного присоединения одной молекулы галогена к двойной связи, которое может осуществляться только как син -присоединение. Анти -присоединение галогена не согласуется также и с образованием открытого карбкатиона RCH + -CH 2 Hal в качестве интермедиата. В открытом карбокатионе возможно свободное вращение вокруг С-С-связи, что должно приводить после атаки аниона Br - к образованию смеси продуктов как анти -, так и син -присоединения. Стереоспецифическое анти -присоединение галогенов явилось главной причиной создания концепции бромониевого или хлорониевого ионов в качестве дискретных промежуточных частиц. Эта концепция идеально удовлетворяет правилу анти -присоединения, поскольку нуклеофильная атака галогенид-иона возможна с анти -стороны по любому из двух атомов углерода галогенониевого иона по S N 2 механизму.

В случае несимметрично замещенных алкенов это должно приводить к двум энантиомерам трео -формы при присоединении брома к цис -изомеру или к энантиомерам эритро -формы при галоидировании транс -изомера. Это действительно наблюдается при присоединении брома, например, к цис - и транс -изомерам пентена-2.
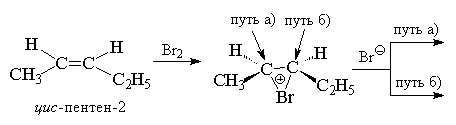



В случае бромирования симметричных алкенов, например, цис - или транс -гексенов-3 должны образоваться или рацемат (D,L -форма), или мезо -форма конечного дибромида, что и наблюдается в действительности.


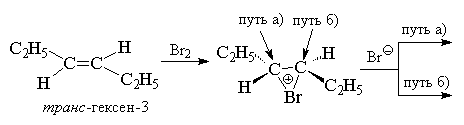

Имеется независимое, прямое доказательство существования галогенониевых ионов в ненуклеофильной, индифферентной среде при низкой температуре. С помощью ЯМР-спектроскопии было зарегистрировано образование бромониевых ионов при ионизации 3-бром-2-метил-2-фторбутана при действии очень сильной кислоты Льюиса пятифтористой сурьмы в растворе жидкой двуокиси серы при -80 0 С.

Этот катион достаточно стабилен при -80 0 С в ненуклеофильной среде, но мгновенно разрушается при действии любых нуклеофильных агентов или при нагревании.
Циклические ионы бромония иногда могут быть выделены в чистом виде, если пространственные препятствия мешают их раскрытию при действии нуклеофилов:

Понятно, что возможность существования довольно стабильных в специальных условиях бромониевых ионов не может служить прямым доказательством их образования в реакции присоединения брома к двойной связи алкена в спирте, уксусной кислоте и других электронодонорных растворителях. Такие данные следует рассматривать лишь как независимое подтверждение принципиальной возможности образования галогенониевых ионов в процессе электрофильного присоединения по двойной связи.
Концепция галогенониевых иона позволяет дать рациональное объяснение обратимости присоединения йода к двойной связи. В катионе галогенония есть три электрофильных центра, доступных нуклеофильной атаке галогенид-аниона: два атома углерода и атом галогена. В случае хлорониевых ионов, анион Cl - , по-видимому, преимущественно или даже исключительно атакует углеродные центры катиона. Для бромониевого катиона равно вероятны оба направления раскрытия галогенониевого иона как за счет атаки бромид-иона по обоим атомам углерода, так и по атому брома. Нуклеофильная атака по атому брома бромониевого иона приводит к исходным реагентам брому и алкену:

Иодониевый ион раскрывается преимущественно в результате атаки иодид-иона по атому йода, и поэтому равновесие между исходными реагентами и иодониевым ионом смещено влево.

Кроме того, конечный продукт присоединения - вицинальный дииодид может подвергаться нуклеофильной атаке по атому йода присутствующим в растворе трииодид-анионом , что также приводит к образованию исходных реагентов алкена и иода. Другими словами, в условиях реакции присоединения происходит деиодирование образующегося вицинального дииодида под действием трииодид-аниона. Вицинальные дихлориды и дибромиды не дегалогенируются в условиях реакции присоединения соответственно хлора или брома к алкенам.
Анти-присоединение хлора или брома характерно для алкенов, у которых двойная связь не сопряжена с -электронами бензольного кольца. Для стирола, стильбена и их производных наряду с анти -присоединением имеет место и син -присоединение галогена, которое в полярной среде может стать даже доминирующим.

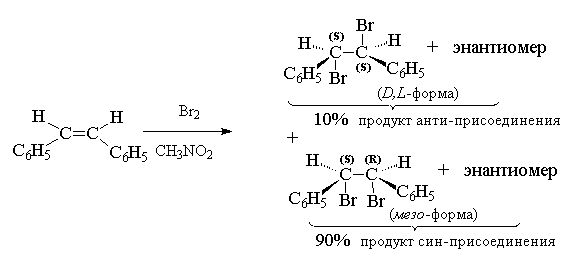
В тех случаях, когда присоединение галогена к двойной связи проводится в среде нуклеофильных растворителей, растворитель эффективно конкурирует с галогенид-ионом при раскрытии трехчленного цикла галогенониевого иона:

Образование продуктов присоединения с участием растворителя или какого-либо иного "внешнего" нуклеофильного агента носит название реакции сопряженного присоединения. При взаимодействии брома и стирола в метаноле образуется два продукта: вицинальный дибромид и бромэфир, соотношение которых зависит от концентрации брома в метаноле
В сильно разбавленном растворе доминирует продукт сопряженного присоединения, а в концентрированном растворе, напротив, преобладающий вицинальный дибромид. В водном растворе всегда преобладает галогенгидрин (спирт, содержащий галоген при -углеродном атоме) - продукт сопряженного присоединения.

ее-Конформер транс -2-хлорциклогексанола дополнительно стабилизирован водородной связью О-Н . . . Cl. В случае несимметричных алкенов в реакциях сопряженного присоединения галоген всегда присоединяется к атому углерода, содержащему наибольшее количество атомов водорода, а нуклеофильный агент к углероду с меньшим количеством атомов водорода. Изомерный продукт с иным расположением присоединяющихся групп не образуется. Это означает, что образующийся в качестве интермедиата циклический галогенониевый ион должен иметь несимметричную структуру с двумя различающимися по энергии и прочности связями С 1 -Hal и С 2 -Hal и большим положительным зарядом на внутреннем атоме углерода С 2 , что можно графически выразить двумя способами:

Поэтому нуклеофильной атаке растворителем подвергается атом углерода С 2 галогенониевого иона несмотря на то, что он более замещен и стерически менее доступен.


Один из лучших препаративных методов синтеза бромгидринов заключается в гидроксибромировании алкенов с помощью N-бромсукцинимида ( NBS ) в бинарной смеси диметилсульфоксида (ДМСО ) и воды.

Данную реакцию можно проводить в воде и без ДМСО , однако выходы бромгидринов в этом случае несколько ниже.



Образование продуктов сопряженного присоединения в реакции галогенирования алкенов также позволяет отвергнуть синхронный механизм присоединения одной молекулы галогена. Сопряженное присоединение к двойной связи находится в хорошем соответствии с двухстадийным механизмом с участием катиона галогенония в качестве интермедиата.
Для реакции электрофильного присоединения к двойной связи следует ожидать увеличения скорости реакции при наличии электронодонорных алкильных заместителей и ее уменьшения при наличии электроноакцепторных заместителей при двойной связи. Действительно, скорость присоединения хлора и брома к двойной связи резко возрастает при переходе от этилена к его метилзамещенным производным. Например, скорость присоединения брома к тетраметилэтилену в 10 5 раз выше, чем скорость его присоединения к бутену-1. Такое громадное ускорение определенно указывает на высокую полярность переходного состояния и высокую степень разделения зарядов в переходном состоянии и согласуется с элетрофильным механизмом присоединения.
В некоторых случаях присоединение хлора к алкенам, содержащим электронодонорные заместители, сопровождается отщеплением протона из промежуточного соединения вместо присоединения хлорид-иона. Отщепление протона приводит к образованию хлорзамещенного алкена, которое формально можно рассматривать как прямое замещение с миграцией двойной связи. Однако опыты с изотопной меткой указывают на более сложный характер происходящих здесь превращений. При хлорировании изобутилена при 0 0 С образуется 2-метил-3-хлорпропен (металлилхлорид) вместо ожидаемого дихлорида - продукта присоединения по двойной связи.

Формально как будто идет замещение, а не присоединение. Изучение этой реакции с использованием изобутилена меченного в положение 1 изотопом 14 С, показало, что прямое замещение водорода хлором не происходит, так как в образующемся металлилхлориде метка находится в группе 14 СН 2 Cl. Этот результат можно объяснить следующей последовательностью превращений:

В отдельных случаях может происходить также 1,2-миграция алкильной группы

В ССl 4 (неполярный растворитель) эта реакция дает практически 100% дихлорида Б - продукта обычного присоединения по двойной связи (без перегруппировки).
Скелетные перегруппировки подобного типа наиболее характерны для процессов с участием открытых карбокатионов в качестве промежуточных частиц. Не исключено, что присоединение хлора в этих случаях идет не через хлорониевый ион, а через катионную частицу, близкую к открытому карбокатиону. Вместе с тем следует отметить, что скелетные перегруппировки явление достаточно редкое в процессах присоединения галогенов и смешанных галогенов по двойной связи: они чаще наблюдаются при присоединении хлора и гораздо реже при присоединении брома. Вероятность таких перегруппировок увеличивается при переходе от неполярных растворителей (ССl 4) к полярным (нитрометан, ацетонитрил).
Суммируя приведенные данные по стереохимии, сопряженному присоединению, влияние заместителей в алкене, а также перегруппировкам в реакциях присоединения галогенов по двойной связи, следует отметить, что они находятся в хорошем соответствии с механизмом электрофильного присоединения с участием циклического галогенониевого иона. Таким же образом могут быть интерпретированы данные по присоединению к алкенам смешанных галогенов, для которых стадийность присоединения определяется полярностью связи двух атомов галогена.
ОПРЕДЕЛЕНИЕ
Алкенами называются ненасыщенные углеводороды, молекулы которых содержат одну двойную связь. Строение молекулы алкенов на примере этилена приведено на рис. 1.
Рис. 1. Строение молекулы этилена.
По физическим свойствам алкены мало отличаются от алканов с тем же числом атомов углерода в молекуле. Низшие гомологи С 2 - С 4 при нормальных условиях - газы; С 5 - С 17 - жидкости; высшие гомологи - твердые вещества. Алкены нерастворимы в воде. Хорошо растворимы в органических растворителях.
Получение алкенов
В промышленности алкены получают при переработке нефти: крекингом и дегидрированием алканов. Лабораторные способы получения алкенов мы разделили на две группы:
- Реакции элиминирования (отщепления)
— дегидратация спиртов
CH 3 -CH 2 -OH → CH 2 =CH 2 + H 2 O (H 2 SO 4 (conc) , t 0 = 170).
— дегидрогалогенированиемоногалогеналканов
CH 3 -CH(Br)-CH 2 -CH 3 + NaOH alcohol → CH 3 -CH=CH-CH 3 + NaBr + H 2 O (t 0).
— дегалогенированиедигалогеналканов
CH 3 -CH(Cl)-CH(Cl)-CH 2 -CH 3 + Zn(Mg) → CH 3 -CH=CH-CH 2 -CH 3 + ZnCl 2 (MgCl 2).
- Неполное гидрирование алкинов
CH≡CH + H 2 →CH 2 =CH 2 (Pd, t 0).
Химические свойства алкенов
Алкены - весьма реакционноспособоные органические соединения. Это объясняется их строением. Химия алкенов - это химия двойной связи. Типичные реакции для алкенов - реакции электрофильного присоединения.
Химические превращения алкенов протекают с расщеплением:
1) π-связи С-С (присоединение, полимеризация и окисление)
— гидрирование
CH 3 -CH=CH 2 + H 2 → CH 3 -CH 2 -CH 2 (kat = Pt).
— галогенирование
CH 3 -CH 2 -CH=CH 2 + Br 2 → CH 3 -CH 2 -CH(Br)-CH 2 Br.
— гидрогалогенирование (протекает по правилу Марковникова: атом водорода присоединяется преимущественно к более гидрированному атому углерода)
CH 3 -CH=CH 2 + H-Cl → CH 3 -CH(Cl)-CH 3 .
— гидратация
CH 2 =CH 2 + H-OH → CH 3 -CH 2 -OH (H + , t 0).
— полимеризация
nCH 2 =CH 2 → -[-CH 2 -CH 2 -]- n (kat, t 0).
— окисление
CH 2 =CH 2 + 2KMnO 4 + 2KOH → HO-CH 2 -CH 2 -OH + 2K 2 MnO 4 ;
2CH 2 =CH 2 + O 2 → 2C 2 OH 4 (эпоксид) (kat = Ag,t 0);
2CH 2 =CH 2 + O 2 → 2CH 3 -C(O)H (kat = PdCl 2 , CuCl).
2) σ- и π-связей С-С
CH 3 -CH=CH-CH 2 -CH 3 + 4[O] → CH 3 COOH + CH 3 CH 2 COOH (KMnO 4 , H +, t 0).
3) связей С sp 3 -Н (в аллильном положении)
CH 2 =CH 2 + Cl 2 → CH 2 =CH-Cl + HCl (t 0 =400).
4) Разрыв всех связей
C 2 H 4 + 2O 2 → 2CO 2 + 2H 2 O;
C n H 2n + 3n/2 O 2 → nCO 2 + nH 2 O.
Применение алкенов
Алкены нашли применение в различных отраслях народного хозяйства. Рассмотрим на примере отдельных представителей.
Этилен широко используется в промышленном органическом синтезе для получения разнообразных органических соединений, таких как галогенопроизводные, спирты (этанол, этиленгликоль), уксусный альдегид, уксусная кислота и др. В большом количестве этилен расходуется для производства полимеров.
Пропилен используется как сырье для получения некоторых спиртов (например, пропанола-2, глицерина), ацетона и др. Полимеризацией пропилена получают полипропилен.
Примеры решения задач
ПРИМЕР 1
| Задание | При гидролизе водным раствором гидроксида натрия NaOH дихлорида, полученного присоединением 6,72 л хлора к этиленовому углеводороду, образовалось 22,8 г двухатомного спирта. Какова формула алкена, если известно, что реакции протекают с количественными выходами (без потерь)? |
| Решение | Запишем уравнение хлорирования алкена в общем виде, а также реакцию получения двухатомного спирта:
C n H 2 n + Cl 2 = C n H 2 n Cl 2 (1); C n H 2 n Cl 2 + 2NaOH = C n H 2 n (OH) 2 + 2HCl (2). Рассчитаем количество вещества хлора: n(Cl 2) = V(Cl 2) / V m ; n(Cl 2) = 6,72 / 22,4 = 0,3 моль, следовательно, дихлорида этилена тоже будет 0,3 моль (уравнение 1), двухатомного спирта также должно получиться 0,3 моль, а по условию задачи это 22,8 г. Значит молярная масса его будет равна: M(C n H 2 n (OH) 2) = m(C n H 2 n (OH) 2) / n(C n H 2 n (OH) 2); M(C n H 2 n (OH) 2) = 22,8 / 0,3 = 76 г/моль. Найдем молярную массу алкена: M(C n H 2 n) = 76 - (2×17) = 42 г/моль, что соответствует формуле C 3 H 6 . |
| Ответ | Формула алкенаC 3 H 6 |
ПРИМЕР 2
| Задание | Сколько граммов потребуется для бромирования 16,8 г алкена, если известно, что при каталитическом гидрировании такого же количества алкена присоединилось 6,72 л водорода? Каков состав и возможное строение исходного углеводорода? |
| Решение | Запишем в общем виде уравнения бромирования и гидрирования алкена:
C n H 2 n + Br 2 = C n H 2 n Br 2 (1); C n H 2 n + H 2 = C n H 2 n +2 (2). Рассчитаем количество вещества водорода: n(H 2) = V(H 2) / V m ; n(H 2) = 6,72 / 22,4 = 0,3 моль, следовательно, алкена тоже будет 0,3 моль (уравнение 2), а по условию задачи это 16,8 г. Значит молярная масса его будет равна: M(C n H 2n) = m(C n H 2n) / n(C n H 2n); M(C n H 2 n) = 16,8 / 0,3 = 56 г/моль, что соответствует формуле C 4 H 8 . Согласно уравнению (1) n(C n H 2 n) :n(Br 2) = 1:1, т.е. n(Br 2) = n(C n H 2 n) = 0,3 моль. Найдем массу брома: m(Br 2) = n(Br 2) × M(Br 2); M(Br 2) = 2×Ar(Br) = 2×80 = 160 г/моль; m(MnO 2) = 0,3 × 160 = 48 г. Составим структурные формулы изомеров: бутен-1 (1), бутен-2 (2), 2-метилпропен (3), циклобутан (4). CH 2 =CH-CH 2 -CH 3 (1); CH 3 -CH=CH-CH 3 (2); CH 2 =C(CH 3)-CH 3 (3); |
| Ответ | Масса брома равна 48 г |
Физические свойства алкенов похожи на свойства алканов, хотя все они имеют несколько более низкие температуры плавления и кипения, чем соответствующие алканы. Например, пентан имеет температуру кипения 36 °С, а пентен-1 - 30 °С. При обычных условиях алкены С 2 — С 4 - газы. С 5 – С 15 - жидкости, начиная с C 16 - твердые вещества. Алкены не растворимы в воде, хорошо растворимы в органических растворителях.
В природе алкены встречаются редко. Поскольку алкены являются ценным сырьем для промышленного органического синтеза, разработаны многие способы их получения.
1. Основным промышленным источником алкенов служит крекинг алканов, входящих в состав нефти:
3. В лабораторных условиях алкены получают по реакциям отщепления (элиминирования), при которых от соседних атомов углерода отщепляются два атома или две группы атомов, и образуется дополнительная p -связь. К таким реакциям относятся следующие.
1) Дегидратация спиртов происходит при их нагревании с водоотнимающими средствами, например с серной кислотой при температуре выше 150 °С:
При отщеплении Н 2 O от спиртов, НВr и HCl от алкилгалогенидов атом водорода преимущественно отщепляется от того из соседних атомов углерода, который связан с наименьшим числом атомов водорода (от наименее гидрогенизированного атома углерода). Эта закономерность носит название правила Зайцева .
3) Дегалогенирование происходит при нагревании дигалогенидов, имеющих атомы галогена у соседних атомов углерода, с активными металлами:
CH 2 Br —CHBr —CH 3 + Mg → СН 2 =СН-СН 3 + Mg Вr 2 .
Химические свойства алкенов определяются наличием в их молекулах двойной связи. Электронная плотность p -связи достаточно подвижна и легко вступает в реакции с электрофильными частицами. Поэтому многие реакции алкенов протекают по механизму электрофильного присоединения , обозначаемому символом A E (от англ, addition electrophilic ). Реакции злектрофильного присоединения это ионные процессы, протекающие в несколько стадий.
На первой стадии электрофильная частица (чаще всего это бывает протон H +) взаимодействует с p -электронами двойной связи и образует p -комплекс, который затем превращается в карбокатион путем образования ковалентной s -связи между электрофильной частицей и одним из атомов углерода:
алкен p -комплекс карбокатион
На второй стадии карбокатион реагирует с анионом X — , образуя вторую s -связь за счет электронной пары аниона:

Ион водорода в реакциях электрофильного присоединения присоединяется к тому из атомов углерода при двойной связи, на котором больше отрицательный заряд. Распределение зарядов определяется смещением p
-электронной плотности под влиянием заместителей:  .
.
Электронодонорные заместители, проявляющие +I -эффект, смещают p -электронную плотность к более гидрогенизированному атому углерода и создают на нем частичный отрицательный заряд. Этим объясняется правило Марковникова : при присоединении полярных молекул типа НХ(X = Hal , ОН, CN и т.п.) к несимметричным алкенам водород преимущественно присоединяется к более гидрогенизированному атому углерода при двойной связи.
Рассмотрим конкретные примеры реакций присоединения.
1) Гидрогалогенирование . При взаимодействии алкенов с галогеноводородами (HCl , НВr ) образуются алкилгалогениды:
СН 3 -СН=СН 2 + НВr ® СН 3 -СНВr-СН 3 .
Продукты реакции определяются правилом Марковникова.
Следует, однако, подчеркнуть, что в присутствии какого-либо органического пероксида полярные молекулы НХ реагируют с алкенами не по правилу Марковникова:
| R-O-O-R | ||
| СН 3 -СН=СН 2 + НВr | СН 3 -СН 2 -СН 2 Вr |
Это связано с тем, что присутствие перекиси обусловливает радикальный, а не ионный механизм реакции.
2) Гидратация . При взаимодействии алкенов с водой в присутствии минеральных кислот (серной, фосфорной) образуются спирты. Минеральные кислоты выполняют роль катализаторов и являются источниками протонов. Присоединение воды также идет по правилу Марковникова:
СН 3 -СН=СН 2 + НОН ® СН 3 -СН(ОН)-СН 3 .
3) Галогенирование . Алкены обесцвечивают бромную воду:
СН 2 =СН 2 + Вr 2 ® ВrСН 2 -СН 2 Вr.
Эта реакция является качественной на двойную связь.
4) Гидрирование . Присоединение водорода происходит под действием металлических катализаторов:
где R = Н, СН 3 , Cl , С 6 Н 5 и т.д. Молекула CH 2 =CHR называется мономером, полученное соединение - полимером , число n-степень полимеризации.
Полимеризация различных производных алкенов дает ценные промышленные продукты: полиэтилен, полипропилен, поливинилхлорид и другие.
Кроме присоединения, для алкенов характерны также реакции окисления. При мягком окислении алкенов водным раствором перманганата калия (реакция Вагнера ) образуются двухатомные спирты:
ЗСН 2 =СН 2 + 2КМn О 4 + 4Н 2 О ® ЗНОСН 2 -СН 2 ОН + 2MnO 2 ↓ + 2KOH .
В результате протекания этой реакции фиолетовый раствор перманганата калия быстро обесцвечивается и выпадает коричневый осадок оксида марганца (IV ). Эта реакция, как и реакция обесцвечивания бромной воды, является качественной на двойную связь. При жестком окислении алкенов кипящим раствором перманганата калия в кислой среде происходит полный разрыв двойной связи с образованием кетонов, карбоновых кислот или СО 2 , например:
| [О] | ||
| СН 3 -СН=СН-СН 3 | 2СН 3 -СООН |
По продуктам окисления можно установить положение двойной связи в исходном алкене.
Как и все другие углеводороды, алкены горят, и при обильном доступе воздуха образуют диоксид углерода и воду:
С n Н 2 n + Зn /2О 2 ® n СО 2 + n Н 2 О.
При ограниченном доступе воздуха горение алкенов может приводить к образованию монооксида углерода и воды:
С n Н 2n + nО 2 ® nCO + nH 2 O .
Если смешать алкен с кислородом и пропустить эту смесь над нагретым до 200°С серебряным катализатором, то образуется оксид алкена (эпоксиалкан), например:

При любых температурах алкены окисляются озоном (озон более сильный окислитель, чем кислород). Если газообразный озон пропускают через раствор какого-либо алкена в тетрахлор-метане при температурах ниже комнатной, то происходит реакция присоединения, и образуются соответствующие озониды (циклические перекиси). Озониды очень неустойчивы и могут легко взрываться. Поэтому обычно их не выделяют, а сразу после получения разлагают водой - при этом образуются карбонильные соединения (альдегиды или кетоны), строение которых указывает на строение подвергавшегося озонированию алкена.
Низшие алкены - важные исходные вещества для промышленного органического синтеза. Из этилена получают этиловый спирт, полиэтилен, полистирол. Пропен используют для синтеза полипропилена, фенола, ацетона, глицерина.
