តំណពូជគឺជាការតភ្ជាប់រវាងសារធាតុដែលជាកម្មសិទ្ធិរបស់ថ្នាក់ផ្សេងៗ។
លក្ខណៈសំខាន់ៗនៃស៊េរីហ្សែន៖
1. សារធាតុទាំងអស់នៃស៊េរីដូចគ្នាត្រូវតែត្រូវបានបង្កើតឡើងដោយធាតុគីមីមួយ។
2. សារធាតុដែលបង្កើតឡើងដោយធាតុដូចគ្នាត្រូវតែជាកម្មសិទ្ធិរបស់ថ្នាក់ផ្សេងគ្នានៃសារធាតុគីមី។
3. សារធាតុដែលបង្កើតជាស៊េរីហ្សែននៃធាតុមួយត្រូវតែមានទំនាក់ទំនងគ្នាទៅវិញទៅមកដោយការបំប្លែងទៅវិញទៅមក។
ដូច្នេះ ហ្សែនដាក់ឈ្មោះសារធាតុមួយចំនួនដែលតំណាងឱ្យថ្នាក់ផ្សេងគ្នានៃសមាសធាតុអសរីរាង្គ គឺជាសមាសធាតុនៃធាតុគីមីដូចគ្នា ត្រូវបានទាក់ទងដោយការបំប្លែងទៅវិញទៅមក និងឆ្លុះបញ្ចាំងពីប្រភពដើមទូទៅនៃសារធាតុទាំងនេះ។
សម្រាប់លោហធាតុ សារធាតុដែលទាក់ទងនឹងហ្សែនចំនួនបីជួរត្រូវបានសម្គាល់ សម្រាប់មិនមែនលោហធាតុ - មួយជួរ។
1. ស៊េរីហ្សែននៃលោហធាតុដែលអ៊ីដ្រូអុកស៊ីតជាមូលដ្ឋាន (អាល់កាឡាំង)៖
លោហៈ→អុកស៊ីដមូលដ្ឋាន→មូលដ្ឋាន (lye)→អំបិល។
ឧទាហរណ៍ ស៊េរីហ្សែននៃជាតិកាល់ស្យូម៖
Ca → CaO → Ca(OH) 2 → CaCl 2
2. ស៊េរីហ្សែននៃលោហធាតុដែលបង្កើតជា amphoteric hydroxides:
អំបិល
លោហៈ→អុកស៊ីដ amphoteric→(អំបិល)→amphoteric hydroxide
ឧទាហរណ៍៖ ZnCl ២
Zn → ZnO → ZnSO 4 → Zn(OH) ២
(H2ZnO2) ↓
Na 2 ZnO ២
អុកស៊ីដស័ង្កសីមិនមានប្រតិកម្មជាមួយទឹកទេ ដូច្នេះអំបិលត្រូវបានទទួលពីវាដំបូង ហើយបន្ទាប់មកស័ង្កសីអ៊ីដ្រូសែន។ ដូចគ្នានេះដែរត្រូវបានធ្វើប្រសិនបើលោហៈត្រូវគ្នាទៅនឹងមូលដ្ឋានដែលមិនអាចរលាយបាន។
3. ស៊េរីហ្សែននៃមិនមែនលោហធាតុ (មិនមែនលោហធាតុបង្កើតបានតែអាស៊ីតអុកស៊ីត)៖
មិនមែនលោហធាតុ→អុកស៊ីដអាស៊ីត→អាស៊ីត→អំបិល
ឧទាហរណ៍ ស៊េរីហ្សែននៃផូស្វ័រ៖
P → P 2 O 5 → H 3 PO 4 → K 3 PO 4
ការផ្លាស់ប្តូរពីសារធាតុមួយទៅសារធាតុមួយទៀតត្រូវបានអនុវត្តដោយប្រើប្រតិកម្មគីមី។
ថ្នាក់ទី 9 មេរៀនទី 47 ប្រធានបទ៖ « តំណពូជនៃខ្ញុំ នេមេ និងសមាសធាតុផ្សំរបស់ពួកវា។
គោលដៅ និងគោលបំណងនៃមេរៀន:
ស្វែងយល់ពីគំនិតនៃ "ទំនាក់ទំនងហ្សែន" ។
រៀនបង្កើតស៊េរីហ្សែននៃលោហធាតុ និងមិនមែនលោហធាតុ។
ដោយផ្អែកលើចំណេះដឹងរបស់សិស្សអំពីថ្នាក់ចម្បងនៃសារធាតុអសរីរាង្គ នាំពួកគេទៅកាន់គំនិតនៃ "ការភ្ជាប់ហ្សែន" និងស៊េរីហ្សែននៃលោហៈ និងមិនមែនលោហៈ។
ដើម្បីបង្រួបបង្រួមចំណេះដឹងអំពីនាមនាម និងលក្ខណៈសម្បត្តិនៃសារធាតុដែលជាកម្មសិទ្ធិរបស់ថ្នាក់ផ្សេងៗ។
អភិវឌ្ឍសមត្ថភាពដើម្បីបន្លិចរឿងសំខាន់ ប្រៀបធៀប និងទូទៅ; កំណត់អត្តសញ្ញាណនិងបង្កើតទំនាក់ទំនង;
បង្កើតគំនិតអំពីទំនាក់ទំនងបុព្វហេតុ និងឥទ្ធិពលនៃបាតុភូត។
ស្តារឡើងវិញក្នុងការចងចាំ គំនិតនៃសារធាតុសាមញ្ញ និងស្មុគ្រស្មាញ លោហធាតុ និងមិនមែនលោហធាតុ ថ្នាក់សំខាន់នៃសមាសធាតុអសរីរាង្គ;
ដើម្បីអភិវឌ្ឍចំណេះដឹងអំពីការភ្ជាប់ហ្សែន និងស៊េរីហ្សែន សូមរៀនបង្កើតស៊េរីហ្សែននៃលោហធាតុ និងមិនមែនលោហធាតុ។
អភិវឌ្ឍសមត្ថភាពក្នុងការធ្វើឱ្យការពិតទូទៅ បង្កើតភាពស្រដៀងគ្នា និងទាញការសន្និដ្ឋាន;
បន្តអភិវឌ្ឍវប្បធម៌ទំនាក់ទំនង សមត្ថភាពក្នុងការបញ្ចេញទស្សនៈ និងការវិនិច្ឆ័យ។
ពង្រឹងស្មារតីទទួលខុសត្រូវចំពោះចំណេះដឹងដែលទទួលបាន។
លទ្ធផលដែលបានគ្រោងទុក៖
ដឹង និយមន័យ និងការចាត់ថ្នាក់នៃសារធាតុអសរីរាង្គ។
អាច ចាត់ថ្នាក់សារធាតុអសរីរាង្គដោយសមាសភាពនិងលក្ខណៈសម្បត្តិ; បង្កើតស៊េរីហ្សែននៃលោហៈនិងមិនមែនលោហធាតុ;
ប្រើសមីការនៃប្រតិកម្មគីមីដើម្បីបង្ហាញពីទំនាក់ទំនងហ្សែនរវាងថ្នាក់សំខាន់ៗនៃសមាសធាតុអសរីរាង្គ។
សមត្ថភាព៖
ជំនាញការយល់ដឹង ៖ រៀបចំ និងចាត់ថ្នាក់ព័ត៌មានពីប្រភពជាលាយលក្ខណ៍អក្សរ និងផ្ទាល់មាត់។
ជំនាញសកម្មភាព ៖ ឆ្លុះបញ្ចាំងពីសកម្មភាពរបស់ខ្លួន, ធ្វើតាមក្បួនដោះស្រាយមួយ, អាចបង្កើតក្បួនដោះស្រាយសម្រាប់សកម្មភាពថ្មីមួយដែលអាចត្រូវបានកំណត់ជាក្បួនដោះស្រាយមួយ។ យល់ពីភាសានៃដ្យាក្រាម។
ជំនាញទំនាក់ទំនង ៖ បង្កើតទំនាក់ទំនងជាមួយមនុស្សផ្សេងទៀត - ធ្វើការសន្ទនាជាគូ គិតគូរពីភាពស្រដៀងគ្នា និងភាពខុសគ្នានៃមុខតំណែង ធ្វើអន្តរកម្មជាមួយដៃគូដើម្បីទទួលបានផលិតផលរួម និងលទ្ធផល។
ប្រភេទមេរៀន:
សម្រាប់គោលបំណង didactic: មេរៀនក្នុងការធ្វើឱ្យទាន់សម័យចំណេះដឹង;
ដោយវិធីសាស្រ្តនៃការរៀបចំ: ទូទៅជាមួយនឹងការទទួលបានចំណេះដឹងថ្មី (មេរៀនរួមបញ្ចូលគ្នា) ។
វឌ្ឍនភាពមេរៀន
I. ពេលរៀបចំ។
II. ការធ្វើបច្ចុប្បន្នភាពចំណេះដឹងជាមូលដ្ឋានរបស់សិស្ស និងវិធីសាស្រ្តនៃសកម្មភាព។
បាវចនានៃមេរៀន៖“វិធីតែមួយគត់
នាំទៅរកចំណេះដឹងគឺជាសកម្មភាព” (B. Shaw) ។ ស្លាយ 1
នៅដំណាក់កាលដំបូងនៃមេរៀន ខ្ញុំធ្វើបច្ចុប្បន្នភាពចំណេះដឹងផ្ទៃខាងក្រោយដែលចាំបាច់ដើម្បីដោះស្រាយបញ្ហា។ នេះរៀបចំសិស្សឱ្យទទួលយកបញ្ហា។ ខ្ញុំអនុវត្តការងារតាមរបៀបកម្សាន្ត ខ្ញុំធ្វើវគ្គបំផុសគំនិតលើប្រធានបទ៖ “ថ្នាក់សំខាន់ៗនៃសមាសធាតុអសរីរាង្គ” ធ្វើការដោយប្រើកាត
កិច្ចការ 1. "កង់ទីបី" ស្លាយ 2
សិស្សត្រូវបានផ្តល់កាតដែលរូបមន្តបីត្រូវបានសរសេរ ដែលមួយក្នុងចំណោមនោះគឺមិនលើសលប់។
សិស្សកំណត់រូបមន្តបន្ថែម ហើយពន្យល់ពីមូលហេតុដែលវាបន្ថែម
ចំលើយ៖ MgO, Na 2 SO 4, H 2 S slide 3
កិច្ចការ 2. “ដាក់ឈ្មោះ និងជ្រើសរើសយើង” (“ដាក់ឈ្មោះយើង”)ស្លាយ 4
| មិនមែនលោហធាតុ | អ៊ីដ្រូសែន | អាស៊ីតអាណូស៊ីក |
ដាក់ឈ្មោះទៅសារធាតុដែលបានជ្រើសរើស (“៤-៥” សរសេរចម្លើយក្នុងរូបមន្ត “៣” ជាពាក្យ)។
( សិស្សធ្វើការជាគូនៅក្ដារខៀន។ ( “៤-៥” សរសេរចម្លើយក្នុងរូបមន្ត “៣” ជាពាក្យ)។
ចម្លើយ៖ ស្លាយ ៥
1. ទង់ដែង ម៉ាញេស្យូម;
4. ផូស្វ័រ;
5. ម៉ាញ៉េស្យូមកាបូណាតសូដ្យូមស៊ុលហ្វាត
7. អំបិល
III. រៀនសម្ភារៈថ្មី។
1. កំណត់ប្រធានបទនៃមេរៀនរួមគ្នាជាមួយសិស្ស។
ជាលទ្ធផលនៃការផ្លាស់ប្តូរគីមី សារធាតុនៃថ្នាក់មួយត្រូវបានបំប្លែងទៅជាសារធាតុមួយទៀត៖ អុកស៊ីដមួយត្រូវបានបង្កើតឡើងពីសារធាតុសាមញ្ញ អាស៊ីតមួយត្រូវបានបង្កើតឡើងពីអុកស៊ីដ ហើយអំបិលត្រូវបានបង្កើតឡើងពីអាស៊ីត។ ម្យ៉ាងវិញទៀត ថ្នាក់នៃសមាសធាតុដែលអ្នកបានសិក្សាគឺទាក់ទងគ្នាទៅវិញទៅមក។ ចូរយើងចែកចាយសារធាតុចូលទៅក្នុងថ្នាក់ដោយយោងទៅតាមភាពស្មុគស្មាញនៃសមាសភាពរបស់វាដោយចាប់ផ្តើមពីសារធាតុសាមញ្ញយោងទៅតាមគ្រោងការណ៍របស់យើង។
សិស្សបង្ហាញពីកំណែរបស់ពួកគេ អរគុណដែលយើងគូរដ្យាក្រាមសាមញ្ញនៃ 2 ជួរ៖ លោហៈ និងមិនមែនលោហធាតុ។ គ្រោងការណ៍នៃស៊េរីហ្សែន។
ខ្ញុំទាក់ទាញការយកចិត្តទុកដាក់របស់សិស្សចំពោះការពិតដែលថាខ្សែសង្វាក់នីមួយៗមានអ្វីមួយដូចគ្នា - ទាំងនេះគឺជាធាតុគីមីនៃលោហៈនិងមិនមែនលោហធាតុដែលឆ្លងកាត់ពីសារធាតុមួយទៅសារធាតុមួយទៀត (ដូចជាតាមរយៈមរតក) ។
(សម្រាប់សិស្សខ្លាំង) CaO, P 2 O 5, MgO, P, H 3 PO 4, Ca, Na 3 PO 4, Ca(OH) 2, NaOH, CaCO 3, H 2 SO 4
(សម្រាប់សិស្សខ្សោយ) CaO, CO 2, C, H 2 CO 3, Ca, Ca(OH) 2, CaCO 3 ស្លាយ 6
ចម្លើយ៖ ស្លាយ ៧
P P2O5 H3PO4 Na3 PO4
Ca CaO Ca(OH)2 CaCO3
អ្វីទៅជាព័ត៌មានតំណពូជដែលហៅថាក្នុងជីវវិទ្យា?
តើអ្នកគិតថាធាតុមួយណានឹងក្លាយជា "ហ្សែន" សម្រាប់ខ្សែសង្វាក់នីមួយៗ? (លោហៈ និងមិនមែនលោហធាតុ)។
ដូច្នេះខ្សែសង្វាក់ឬស៊េរីបែបនេះត្រូវបានគេហៅថាហ្សែន។ ប្រធានបទនៃមេរៀនរបស់យើងគឺ "ទំនាក់ទំនងហ្សែនរវាងខ្ញុំ និង នេមេ" ស្លាយ ៨. បើកសៀវភៅកត់ត្រារបស់អ្នក ហើយសរសេរកាលបរិច្ឆេទ និងប្រធានបទនៃមេរៀន។ តើអ្នកគិតថាអ្វីជាគោលដៅនៃមេរៀនរបស់យើង? ស្វែងយល់ពីគំនិតនៃ "ការភ្ជាប់ហ្សែន" រៀនបង្កើតស៊េរីហ្សែននៃលោហធាតុ និងមិនមែនលោហធាតុ។
2. ចូរកំណត់ទំនាក់ទំនងហ្សែន។
តំណពូជ -គឺជាការផ្សារភ្ជាប់គ្នារវាងសារធាតុនៃថ្នាក់ផ្សេងៗគ្នា ដោយផ្អែកលើការផ្លាស់ប្តូរគ្នាទៅវិញទៅមក និងឆ្លុះបញ្ចាំងពីឯកភាពនៃប្រភពដើមរបស់វា។ ស្លាយ 9.10
សញ្ញាដែលកំណត់លក្ខណៈនៃស៊េរីហ្សែន៖ ស្លាយ ១១
1. សារធាតុនៃថ្នាក់ផ្សេងគ្នា;
2. សារធាតុផ្សេងគ្នាដែលបង្កើតឡើងដោយធាតុគីមីមួយ, i.e. តំណាងឱ្យទម្រង់ផ្សេងគ្នានៃអត្ថិភាពនៃធាតុមួយ;
3. សារធាតុផ្សេងគ្នានៃធាតុគីមីដូចគ្នាត្រូវបានតភ្ជាប់ដោយការបំប្លែងទៅវិញទៅមក។
3. ពិចារណាឧទាហរណ៍នៃទំនាក់ទំនងហ្សែនរបស់ Me ។
2. ស៊េរីហ្សែន ដែលមូលដ្ឋានគឺជាមូលដ្ឋានដែលមិនអាចរលាយបាន នោះស៊េរីអាចត្រូវបានតំណាងដោយខ្សែសង្វាក់នៃការផ្លាស់ប្តូរ៖ ស្លាយ 12
លោហៈ → អុកស៊ីដមូលដ្ឋាន → អំបិល → មូលដ្ឋានមិនរលាយ → អុកស៊ីដមូលដ្ឋាន → លោហៈ
ឧទាហរណ៍ Cu → CuO → CuCl2 → Cu (OH) 2 → CuO
1. 2 Cu+O 2 → 2 CuO 2. CuO+ 2HCI → CuCI 2 3. CuCI 2 +2NaOH → Cu(OH) 2 +2NaCI
4.Cu(OH) 2 CuO + H 2 O
4. ពិចារណាឧទាហរណ៍នៃការភ្ជាប់ហ្សែនរបស់ NeMe ។
ក្នុងចំណោមមិនមែនលោហធាតុ ស៊េរីពីរប្រភេទក៏អាចសម្គាល់បានដែរ៖ ស្លាយ ១៣
2. ស៊េរីហ្សែននៃមិនមែនលោហធាតុ ដែលអាស៊ីតរលាយដើរតួនាទីជាតំណភ្ជាប់ក្នុងស៊េរី។ ខ្សែសង្វាក់នៃការផ្លាស់ប្តូរអាចត្រូវបានតំណាងដូចខាងក្រោមៈ មិនមែនលោហៈ → អុកស៊ីដអាស៊ីត → អាស៊ីតរលាយ → អំបិល ឧទាហរណ៍ P → P 2 O 5 → H 3 PO 4 → Ca 3 (PO 4) 2
1. 4P + 5O 2 → 2P 2 O 5 2. P 2 O 5 + H 2 O → 2H 3 PO 4 3. 2H 3 PO 4 +3 Ca(OH) 2 → Ca 3 (PO 4) 2 +6 H 2 ឱ
5. ការចងក្រងនៃស៊េរីហ្សែន។ ស្លាយ ១៤
1. ស៊េរីហ្សែនដែលអាល់កាឡាំងដើរតួជាមូលដ្ឋាន។ ស៊េរីនេះអាចត្រូវបានតំណាងដោយប្រើបំលែងដូចខាងក្រោមៈ លោហៈ → អុកស៊ីដមូលដ្ឋាន → អាល់កាឡាំង → អំបិល
O 2 , + H 2 O , + HCI
4K + O 2 = 2K 2 O K 2 O + H 2 O = 2KOH KOH + HCI = KCl ស្លាយ 15
2. ស៊េរីហ្សែននៃមិនមែនលោហធាតុ ដែលអាស៊ីតមិនអាចរលាយបានដើរតួជាតំណភ្ជាប់ក្នុងស៊េរី៖
nonmetal → អាស៊ីតអុកស៊ីត → អំបិល → អាស៊ីត → អុកស៊ីដអាស៊ីត → មិនមែនលោហៈ
ឧទាហរណ៍ Si → SiO 2 → Na 2 SiO 3 → H 2 SiO 3 → SiO 2 → Si (បង្កើតសមីការដោយខ្លួនឯងដែលធ្វើការ "4-5") ។ តេស្តខ្លួនឯង។ សមីការទាំងអស់គឺត្រឹមត្រូវ "5" កំហុសមួយគឺ "4" កំហុសពីរគឺ "3" ។
5. អនុវត្តលំហាត់ឌីផេរ៉ង់ស្យែល (ការធ្វើតេស្តដោយខ្លួនឯង) ។ ស្លាយ ១៥
Si + O 2 = SiO 2 SiO 2 +2 NaOH = Na 2 SiO 3 + H 2 O Na 2 SiO 3 + 2НCI = H 2 SiO 3 +2NaCI H 2 SiO 3 = SiO 2 + H 2 O
SiO 2 +2Mg = Si + 2MgO
1. អនុវត្តការបំប្លែងតាមគ្រោងការណ៍ (ភារកិច្ច "4-5") ។
កិច្ចការ 1. នៅក្នុងរូប ចូរភ្ជាប់រូបមន្តនៃសារធាតុជាមួយនឹងបន្ទាត់ស្របតាមទីតាំងរបស់វានៅក្នុងស៊េរីហ្សែននៃអាលុយមីញ៉ូម។ សរសេរសមីការប្រតិកម្ម។ ស្លាយ ១៦
តេស្តខ្លួនឯង។
4AI+ 3O 2 = 2AI 2 O 3 AI 2 O 3 + 6НCI = 2AICI 3 + 3Н 2 О AICI 3 + 3NaOH = AI(OH) 3 +3NaCI
AI(OH) 3 = AI 2 O 3 + H 2 O ស្លាយ ១៧
កិច្ចការទី 2. "វាយគោលដៅ" ។ ជ្រើសរើសរូបមន្តនៃសារធាតុដែលបង្កើតជាស៊េរីហ្សែននៃជាតិកាល់ស្យូម។ សរសេរសមីការប្រតិកម្មសម្រាប់ការបំប្លែងទាំងនេះ។ ស្លាយ 18

តេស្តខ្លួនឯង។
2Ca+O 2 =2CaO CaO+H 2 O = Ca(OH) 2 Ca(OH) 2 +2 HCI = CaCI 2 + 2 H 2 O CaCI 2 +2AgNO 3 = Ca(NO 3) 2 +2AgCI ស្លាយ 19
2. អនុវត្តការងារតាមគ្រោងការណ៍។ សរសេរសមីការប្រតិកម្មសម្រាប់ការបំប្លែងទាំងនេះ។
O 2 + H 2 O + NaOH
S SO 2 H 2 SO 3 Na 2 SO 3 ឬកំណែស្រាលជាង
S + O 2 = SO 2 + H 2 O = H 2 SO 3 + NaOH =
SO 2 + H 2 O = H 2 SO 3
H 2 SO 3 +2NaOH = Na 2 SO 3 +2H 2 O
IV. ការបង្រួបបង្រួមហ្សុន
ជម្រើសទី 1 ។
ផ្នែក A
1. ស៊េរីហ្សែននៃលោហៈគឺ៖ ក) សារធាតុបង្កើតជាស៊េរីដោយផ្អែកលើលោហៈមួយ។
ក)CO 2 ខ) CO គ) CaO ឃ) O ២
៣.កំណត់អត្តសញ្ញាណសារធាតុ “Y” ពីគ្រោងការណ៍បំប្លែង៖ Na → Y → NaOH ក)ណា 2 អូខ) Na 2 O 2 គ) H 2 O d) Na
4. នៅក្នុងគ្រោងការណ៍បំប្លែង៖ CuCl 2 → A → B → Cu រូបមន្តនៃផលិតផលកម្រិតមធ្យម A និង B គឺ: ក) CuO និង Cu (OH) 2 ខ) CuSO 4 និង Cu (OH) 2 គ) CuCO 3 និង Cu(OH) ២ ឆ)គ(អូ) 2 និងCuO
5. ផលិតផលចុងក្រោយនៅក្នុងខ្សែសង្វាក់នៃការផ្លាស់ប្តូរដោយផ្អែកលើសមាសធាតុកាបូន CO 2 → X 1 → X 2 → NaOH ក) សូដ្យូមកាបូនខ) សូដ្យូមប៊ីកាបូណាត គ) សូដ្យូម កាបូអ៊ីដ ឃ) អាសេតាត សូដ្យូម
E → E 2 O 5 → N 3 EO 4 → Na 3 EO 4 ក) N ខ) Mn វី)ទំឃ) Cl
ផ្នែកខ។
Fe + Cl 2 A) FeCl ២
Fe + HCl B) FeCl ៣
FeO + HCl B) FeCl 2 + H 2
Fe 2 O 3 + HCl D) FeCl 3 + H 2
ឃ) FeCl 2 + H 2 O
ង) FeCl 3 + H 2 O
1 B, 2 A, 3D, 4E
ក) ប៉ូតាស្យូមអ៊ីដ្រូសែន (ដំណោះស្រាយ) ខ) ជាតិដែក គ) បារីយ៉ូមនីត្រាត (ដំណោះស្រាយ)ឃ) អុកស៊ីដអាលុយមីញ៉ូម
ង) កាបូនម៉ូណូអុកស៊ីត (II) ង) សូដ្យូមផូស្វាត (ដំណោះស្រាយ)
ផ្នែក C
1. អនុវត្តគ្រោងការណ៍បំប្លែងសារធាតុ៖ Fe → FeO → FeCI 2 → Fe (OH) 2 → FeSO 4
2Fe + O 2 = 2FeO FeO + 2HCI = FeCI 2 + H 2 O FeCI 2 + 2NaOH = Fe(OH) 2 +2NaCI
Fe(OH) 2 + H 2 SO 4 = FeSO 4 +2 H 2 O
ជម្រើស 2.
ផ្នែក A (ភារកិច្ចដែលមានចម្លើយត្រឹមត្រូវមួយ)
ខ) សារធាតុដែលបង្កើតជាស៊េរីដោយផ្អែកលើមួយមិនមែនលោហធាតុ គ) សារធាតុដែលបង្កើតជាស៊េរីដោយផ្អែកលើលោហៈ ឬមិនមែនលោហធាតុ ឃ) សារធាតុពីថ្នាក់ផ្សេងៗនៃសារធាតុដែលទាក់ទងនឹងការបំប្លែង
2. កំណត់អត្តសញ្ញាណសារធាតុ “X” ពីគ្រោងការណ៍បំប្លែង៖ P → X → Ca 3 (PO 4) 2 ក)ទំ 2 អូ 5 ខ) P 2 O 3 គ) CaO ឃ) O 2
ក) កា ខ)CaOគ) CO 2 ឃ) H 2 O
4. នៅក្នុងគ្រោងការណ៍បំប្លែង៖ MgCl 2 → A → B → Mg រូបមន្តនៃផលិតផលកម្រិតមធ្យម A និង B គឺ៖ ក) MgO និង Mg(OH) 2 ខ) MgSO 4 និង Mg(OH) 2 គ) MgCO 3 និង Mg(OH) ២ ឆ)Mg(អូ) 2 និងMgO
CO 2 → X 1 → X 2 → NaOH ក) សូដ្យូមកាបូនខ) សូដ្យូមប៊ីកាបូណាត
6. ធាតុ "E" ដែលចូលរួមក្នុងខ្សែសង្វាក់នៃការផ្លាស់ប្តូរ៖
ផ្នែកខ។ (កិច្ចការដែលមានជម្រើសចម្លើយត្រឹមត្រូវ 2 ឬច្រើន)
1. បង្កើតការឆ្លើយឆ្លងគ្នារវាងរូបមន្តនៃសារធាតុចាប់ផ្តើម និងផលិតផលប្រតិកម្ម៖
រូបមន្តនៃសារធាតុចាប់ផ្តើម រូបមន្តនៃផលិតផល
NaOH+ CO 2 A) NaOH + H ២
Na + H 2 O B) NaHCO ៣
NaOH + HCl ឃ) NaCl + H 2 O
1B, 2B, 3 A, 4G
ក) សូដ្យូមអ៊ីដ្រូសែន (ដំណោះស្រាយ) ខ) អុកស៊ីសែន គ) សូដ្យូមក្លរួ (ដំណោះស្រាយ)ឃ) កាល់ស្យូមអុកស៊ីដ
ង) ប៉ូតាស្យូម permanganate (គ្រីស្តាល់) ង) អាស៊ីតស៊ុលហ្វួរីក
ផ្នែក C (ជាមួយជម្រើសចម្លើយលម្អិត)
S + O 2 = SO 2 2SO 2 + O 2 = 2 SO 3 SO 3 + H 2 O = H 2 SO 4 H 2 SO 4 + Ca(OH) 2 = CaSO 4 +2 H 2 O
CaSO 4 + BaCI 2 = BaSO 4 + CaCI ២
វ.លទ្ធផលមេរៀន. ការចាត់ថ្នាក់។
VI.D/Zទំព័រ 215-216 រៀបចំសម្រាប់លំហាត់លេខ 3 ជម្រើសទី 1 កិច្ចការលេខ 2,4, 6, ជម្រើសទី 2 កិច្ចការលេខ 2,3, 6. ស្លាយ 20
VII. ការឆ្លុះបញ្ចាំង។
សិស្សសរសេរនៅលើក្រដាសនូវអ្វីដែលពួកគេធ្វើបានល្អនៅក្នុងមេរៀន និងអ្វីដែលពួកគេធ្វើមិនបាន។ តើមានការលំបាកអ្វីខ្លះ? និងជូនពរលោកគ្រូ។
មេរៀនបានបញ្ចប់ហើយ។ អរគុណអ្នកទាំងអស់គ្នា ហើយមានថ្ងៃល្អ ស្លាយ 21
ប្រសិនបើមានពេលវេលានៅសល់។
កិច្ចការ
Yuh ធ្លាប់ធ្វើការពិសោធន៍ដើម្បីវាស់ចរន្តអគ្គិសនីនៃដំណោះស្រាយនៃអំបិលផ្សេងៗ។ នៅលើតុមន្ទីរពិសោធន៍របស់គាត់មាន beakers ជាមួយនឹងដំណោះស្រាយ KCl, BaCl
2
, ខេ
2
CO
3
, ណា
2
ដូច្នេះ
4
និង AgNO
3
. កញ្ចក់នីមួយៗមានស្លាកសញ្ញាបិទជាប់យ៉ាងប្រុងប្រយ័ត្ន។ នៅក្នុងមន្ទីរពិសោធន៍ មានសេកមួយក្បាលដែលទ្រុងមិនចាក់សោបានល្អ។ នៅពេលដែល Yukh ស្រូបនៅក្នុងការពិសោធន៍ ក្រឡេកមើលទៅក្រឡេកមើលច្រែះដែលគួរឱ្យសង្ស័យ គាត់ពិតជារន្ធត់ណាស់ដែលបានរកឃើញថាសេកដែលបំពានលើបទប្បញ្ញត្តិសុវត្ថិភាពទាំងស្រុង កំពុងព្យាយាមផឹកពីកែវជាមួយនឹងដំណោះស្រាយ BaCl 2។ ដោយដឹងថាអំបិលបារីយ៉ូមដែលរលាយទាំងអស់មានជាតិពុលខ្លាំង យូ ប្រញាប់ចាប់យកកែវដែលមានស្លាកផ្សេងពីតុ ហើយចាក់ដំណោះស្រាយដោយបង្ខំទៅក្នុងចំពុះរបស់សេក។ សេកត្រូវបានរក្សាទុក។ កែវមួយដែលប្រើដំណោះស្រាយអ្វីដើម្បីសង្គ្រោះសត្វសេក?
ចម្លើយ៖
BaCl 2 + Na 2 SO 4 = BaSO 4 (precipitate) + 2NaCl (បារីយ៉ូមស៊ុលហ្វាតគឺអាចរលាយបានតិចតួចដែលវាមិនអាចមានជាតិពុលដូចជាអំបិលបារីយ៉ូមផ្សេងទៀត) ។
ឧបសម្ព័ន្ធ ១
9 "B" ថ្នាក់ F.I. _______________________ (សម្រាប់សិស្សខ្សោយ)
កិច្ចការ 1. "កង់ទីបី" ។
(ត្រឹមត្រូវចំនួន 4 – “5”, 3-“4”, 2-“3”, 1-“2”)
| មិនមែនលោហធាតុ | អ៊ីដ្រូសែន | អាស៊ីតអាណូស៊ីក |
||||
សិស្សកំណត់ថ្នាក់ដែលពួកគេបានជ្រើសរើស ហើយជ្រើសរើសសារធាតុសមស្របពីឯកសារដែលបានផ្តល់ឲ្យ។
ទង់ដែង ស៊ីលីកុនអុកស៊ីដ អាស៊ីត hydrochloric បារីយ៉ូម អ៊ីដ្រូសែន ធ្យូងថ្ម ម៉ាញេស្យូម ផូស្វ័រ បារីយ៉ូម អ៊ីដ្រូស៊ីត ម៉ាញ៉េស្យូមអុកស៊ីត ជាតិដែក (III) អ៊ីដ្រូសែន ម៉ាញ៉េស្យូមកាបូណាត សូដ្យូមស៊ុលហ្វាត។
(“៤-៥” សរសេរចម្លើយក្នុងរូបមន្ត “៣” ជាពាក្យ)។
12 ចម្លើយ “5”, 11-10- “4”, 9-8- “3”, 7 ឬតិចជាង – “2”
កិច្ចការទី 3 ។
O 2 , + H 2 O , + HCI
ឧទាហរណ៍ K → K 2 O → KOH → KCl (បង្កើតសមីការដោយខ្លួនឯងដែលធ្វើការ "3" កំហុសមួយ "3" កំហុសពីរ "2") ។
កិច្ចការទី 4. អនុវត្តភារកិច្ចតាមគ្រោងការណ៍។ សរសេរសមីការប្រតិកម្មសម្រាប់ការបំប្លែងទាំងនេះ។
O 2 + H 2 O + NaOH
S SO 2 H 2 SO 3 Na 2 SO 3
ឬកំណែស្រាលជាងមុន
H 2 SO 3 + NaOH =
ជម្រើសទី 1 ។
ផ្នែក A (ភារកិច្ចដែលមានចម្លើយត្រឹមត្រូវមួយ)
1. ស៊េរីហ្សែននៃលោហៈមួយគឺ៖ ក) សារធាតុដែលបង្កើតជាស៊េរីដោយផ្អែកលើលោហៈមួយ។
ខ) សារធាតុដែលបង្កើតជាស៊េរីដោយផ្អែកលើមួយមិនមែនលោហធាតុ គ) សារធាតុដែលបង្កើតជាស៊េរីដោយផ្អែកលើលោហៈ ឬមិនមែនលោហធាតុ ឃ) សារធាតុពីថ្នាក់ផ្សេងៗនៃសារធាតុដែលទាក់ទងនឹងការបំប្លែង
2. កំណត់អត្តសញ្ញាណសារធាតុ “X” ពីគ្រោងការណ៍បំប្លែង៖ C → X → CaCO 3
ក) CO 2 ខ) CO គ) CaO ឃ) O 2
3. កំណត់សារធាតុ “Y” ពីគ្រោងការណ៍បំប្លែង៖ Na → Y → NaOH ក) Na 2 O b) Na 2 O 2 គ) H 2 O d) Na
4. នៅក្នុងគ្រោងការណ៍បំប្លែង៖ CuCl 2 → A → B → Cu រូបមន្តនៃផលិតផលកម្រិតមធ្យម A និង B គឺ: ក) CuO និង Cu (OH) 2 ខ) CuSO 4 និង Cu (OH) 2 គ) CuCO 3 និង Cu(OH) 2 ក្រាម) Cu(OH) 2 និង CuO
5. ផលិតផលចុងក្រោយនៅក្នុងខ្សែសង្វាក់នៃការផ្លាស់ប្តូរដោយផ្អែកលើសមាសធាតុកាបូន CO 2 → X 1 → X 2 → NaOH ក) សូដ្យូមកាបូន ខ) សូដ្យូមអ៊ីដ្រូសែនកាបូន c) សូដ្យូម carbide ឃ) សូដ្យូមអាសេតាត
6. ធាតុ "E" ដែលចូលរួមក្នុងខ្សែសង្វាក់នៃការផ្លាស់ប្តូរ: E → E 2 O 5 → H 3 EO 4 → Na 3 EO 4 a)N b) Mn c) P d) Cl
ផ្នែកខ។ (កិច្ចការដែលមានជម្រើសចម្លើយត្រឹមត្រូវ 2 ឬច្រើន)
1. បង្កើតការឆ្លើយឆ្លងគ្នារវាងរូបមន្តនៃសារធាតុចាប់ផ្តើម និងផលិតផលប្រតិកម្ម៖
រូបមន្តនៃសារធាតុចាប់ផ្តើម រូបមន្តនៃផលិតផល
Fe + Cl 2 A) FeCl ២
Fe + HCl B) FeCl ៣
FeO + HCl B) FeCl 2 + H 2
Fe 2 O 3 + HCl D) FeCl 3 + H 2
ឃ) FeCl 2 + H 2 O
ង) FeCl 3 + H 2 O
2. ដំណោះស្រាយនៃទង់ដែង (II) ស៊ុលហ្វាតមានប្រតិកម្ម៖
ក) ប៉ូតាស្យូមអ៊ីដ្រូសែន (ដំណោះស្រាយ) ខ) ជាតិដែក គ) បារីយ៉ូមនីត្រាត (ដំណោះស្រាយ) ឃ) អុកស៊ីដអាលុយមីញ៉ូម
e) កាបូនម៉ូណូអុកស៊ីត (II) f) សូដ្យូមផូស្វាត (ដំណោះស្រាយ)
ផ្នែក C (ជាមួយជម្រើសចម្លើយលម្អិត)
1. អនុវត្តគ្រោងការណ៍សម្រាប់ការបំប្លែងសារធាតុ៖
Fe → FeO → FeCI 2 → Fe (OH) 2 → FeSO 4
ឧបសម្ព័ន្ធ 2
9 "B" ថ្នាក់ F.I. _______________________ (សម្រាប់សិស្សខ្លាំង)
កិច្ចការ 1. "កង់ទីបី" ។កំណត់រូបមន្តដែលលែងត្រូវការតទៅទៀត ហើយពន្យល់ពីមូលហេតុដែលវាលែងត្រូវការតទៅទៀត។
(ត្រឹមត្រូវចំនួន 4 – “5”, 3-“4”, 2-“3”, 1-“2”)
កិច្ចការ 2. “ដាក់ឈ្មោះ និងជ្រើសរើសយើង” (“ដាក់ឈ្មោះយើង”)។ផ្តល់ឈ្មោះសារធាតុដែលបានជ្រើសរើស ហើយបំពេញតារាង។
សិស្សកំណត់ថ្នាក់ដែលពួកគេបានជ្រើសរើស ហើយជ្រើសរើសសារធាតុសមស្របពីឯកសារដែលបានផ្តល់ឲ្យ។
ទង់ដែង ស៊ីលីកុនអុកស៊ីដ អាស៊ីត hydrochloric បារីយ៉ូម អ៊ីដ្រូសែន ធ្យូងថ្ម ម៉ាញេស្យូម ផូស្វ័រ បារីយ៉ូម អ៊ីដ្រូស៊ីត ម៉ាញ៉េស្យូមអុកស៊ីត ជាតិដែក (III) អ៊ីដ្រូសែន ម៉ាញ៉េស្យូមកាបូណាត សូដ្យូមស៊ុលហ្វាត។ (“៤-៥” សរសេរចម្លើយក្នុងរូបមន្ត “៣” ជាពាក្យ)។
12 ចម្លើយ “5”, 11-10- “4”, 9-8- “3”, 7 ឬតិចជាង – “2”
កិច្ចការទី 3 ។
Si → SiO 2 → Na 2 SiO 3 → H 2 SiO 3 → SiO 2 → Si (បង្កើតសមីការដោយខ្លួនឯងដែលធ្វើការ "4-5") ។ តេស្តខ្លួនឯង។ សមីការទាំងអស់គឺត្រឹមត្រូវ "5" កំហុសមួយគឺ "4" កំហុសពីរគឺ "3" ។
កិច្ចការទី 4. នៅក្នុងរូប ចូរភ្ជាប់រូបមន្តនៃសារធាតុជាមួយនឹងបន្ទាត់ស្របតាមទីតាំងរបស់វានៅក្នុងស៊េរីហ្សែននៃអាលុយមីញ៉ូម។ សរសេរសមីការប្រតិកម្ម។ សមីការទាំងអស់គឺត្រឹមត្រូវ "5" កំហុសមួយគឺ "4" កំហុសពីរគឺ "3" ។
កិច្ចការ 5. "វាយគោលដៅ" ។ ជ្រើសរើសរូបមន្តនៃសារធាតុដែលបង្កើតជាស៊េរីហ្សែននៃជាតិកាល់ស្យូម។ សរសេរសមីការប្រតិកម្មសម្រាប់ការបំប្លែងទាំងនេះ។ សមីការទាំងអស់គឺត្រឹមត្រូវ "5" កំហុសមួយគឺ "4" កំហុសពីរគឺ "3" ។

ជម្រើសទី 2 ។
ផ្នែក A (ភារកិច្ចដែលមានចម្លើយត្រឹមត្រូវមួយ)
1. ស៊េរីហ្សែននៃមិនមែនលោហធាតុគឺ៖ ក) សារធាតុដែលបង្កើតជាស៊េរីដោយផ្អែកលើលោហៈមួយ។
ខ) សារធាតុដែលបង្កើតជាស៊េរីដោយផ្អែកលើមួយមិនមែនលោហធាតុ គ) សារធាតុដែលបង្កើតជាស៊េរីដោយផ្អែកលើលោហៈ ឬមិនមែនលោហធាតុ ឃ) សារធាតុពីថ្នាក់ផ្សេងៗនៃសារធាតុដែលទាក់ទងនឹងការបំប្លែង
2. កំណត់អត្តសញ្ញាណសារធាតុ “X” ពីគ្រោងការណ៍បំប្លែង៖ P → X → Ca 3 (PO 4) 2 ក) P 2 O 5 ខ) P 2 O 3 គ) CaO ឃ) O 2
3. កំណត់អត្តសញ្ញាណសារធាតុ “Y” ពីគ្រោងការណ៍បំប្លែង៖ Ca → Y → Ca(OH) 2
a) Ca ខ) CaO គ) CO 2 ឃ) H 2 O
4. នៅក្នុងគ្រោងការណ៍បំប្លែង៖ MgCl 2 → A → B → Mg រូបមន្តនៃផលិតផលកម្រិតមធ្យម A និង B គឺ៖ ក) MgO និង Mg(OH) 2 ខ) MgSO 4 និង Mg(OH) 2 គ) MgCO 3 និង Mg (OH) 2 ក្រាម) Mg (OH) 2 និង MgO
5. ផលិតផលចុងក្រោយនៅក្នុងខ្សែសង្វាក់នៃការផ្លាស់ប្តូរដោយផ្អែកលើសមាសធាតុកាបូន៖
CO 2 → X 1 → X 2 → NaOH ក) សូដ្យូមកាបូន ខ) សូដ្យូមប៊ីកាបូណាត
គ) សូដ្យូម carbide ឃ) សូដ្យូមអាសេតាត
6. ធាតុ "E" ដែលចូលរួមក្នុងខ្សែសង្វាក់នៃការផ្លាស់ប្តូរ៖
E → EO 2 → EO 3 → N 2 EO 4 → Na 2 EO 4 a)N b) S c)P d)Mg
ផ្នែកខ។ (កិច្ចការដែលមានជម្រើសចម្លើយត្រឹមត្រូវ 2 ឬច្រើន)
1. បង្កើតការឆ្លើយឆ្លងគ្នារវាងរូបមន្តនៃសារធាតុចាប់ផ្តើម និងផលិតផលប្រតិកម្ម៖
រូបមន្តនៃសារធាតុចាប់ផ្តើម រូបមន្តនៃផលិតផល
NaOH+ CO 2 A) NaOH + H ២
NaOH + CO 2 B) Na 2 CO 3 + H 2 O
Na + H 2 O B) NaHCO ៣
NaOH + HCl ឃ) NaCl + H 2 O
2. អាស៊ីត Hydrochloric មិនមានប្រតិកម្ម៖
ក) សូដ្យូមអ៊ីដ្រូសែន (ដំណោះស្រាយ) ខ) អុកស៊ីសែន គ) សូដ្យូមក្លរួ (ដំណោះស្រាយ) ឃ) កាល់ស្យូមអុកស៊ីដ
ង) ប៉ូតាស្យូម permanganate (គ្រីស្តាល់) f) អាស៊ីតស៊ុលហ្វួរីក
ផ្នែក C (ជាមួយជម្រើសចម្លើយលម្អិត)
អនុវត្តគ្រោងការណ៍បំប្លែងសារធាតុ៖ S → SO 2 → SO 3 → H 2 SO 4 → CaSO 4 → BaSO 4
ឧបសម្ព័ន្ធទី ៣
តារាងចម្លើយ "៤-៥"៖
កិច្ចការ 1. MgO, Na 2 SO 4, H 2 S
កិច្ចការទី 2 ។
1. ទង់ដែង ម៉ាញេស្យូម;
3. ស៊ីលីកុនអុកស៊ីដ ម៉ាញ៉េស្យូមអុកស៊ីដ;
4. ផូស្វ័រ
5. ម៉ាញ៉េស្យូមកាបូណាតស៊ុលហ្វាត;
6. barium hydroxide, ជាតិដែក (III) hydroxide;
7. សូដ្យូម hydrochloride
កិច្ចការទី 3 ។
SiO 2 + 2NaOH = Na 2 SiO 3 + H 2 O
Na 2 SiO 3 + 2НCI = H 2 SiO 3 + 2NaCI
H 2 SiO 3 = SiO 2 + H 2 O
SiO 2 +2Mg = Si + 2MgO
កិច្ចការទី 4 ។
4AI+ 3O 2 = 2AI 2 O 3
AI 2 O 3 + 6НCI = 2AICI 3 + 3Н 2 О
AICI 3 + 3NaOH = AI(OH) 3 + 3NaCI
AI(OH) 3 = AI 2 O 3 + H 2 O
កិច្ចការទី 5 ។
CaO+H 2 O = Ca(OH) ២
Ca(OH) 2 +2 HCI = CaCI 2 + 2H2O
CaCI 2 +2AgNO 3 = Ca(NO 3) 2 +2AgCI
សន្លឹកវាយតម្លៃខ្លួនឯង។
| ឈ្មោះពេញរបស់សិស្ស | លេខការងារ | |
>> គីមីវិទ្យា៖ ទំនាក់ទំនងហ្សែនរវាងថ្នាក់នៃសារធាតុ
ហ្សែន
គឺជាការផ្សារភ្ជាប់គ្នារវាងសារធាតុនៃថ្នាក់ផ្សេងៗគ្នា ដោយផ្អែកលើការបំប្លែងទៅវិញទៅមករបស់ពួកគេ និងឆ្លុះបញ្ចាំងពីការរួបរួមនៃប្រភពដើមរបស់ពួកគេ ពោលគឺការបង្កើតសារធាតុ។
ដំបូងយើងបង្ហាញព័ត៌មានរបស់យើងអំពីការចាត់ថ្នាក់នៃសារធាតុក្នុងទម្រង់ជាដ្យាក្រាម។
ដោយដឹងពីថ្នាក់នៃសារធាតុសាមញ្ញ វាអាចបង្កើតស៊េរីហ្សែនចំនួនពីរ៖ ស៊េរីហ្សែននៃលោហធាតុ និងមិនមែនលោហធាតុ។
ស៊េរីហ្សែននៃលោហធាតុឆ្លុះបញ្ចាំងពីទំនាក់ទំនងនៃសារធាតុនៃថ្នាក់ផ្សេងៗគ្នាដែលផ្អែកលើលោហៈដូចគ្នា។
បែងចែក ពូជពីរនៃស៊េរីហ្សែននៃលោហធាតុ
1. ស៊េរីហ្សែននៃលោហធាតុដែលអាល់កាឡាំងត្រូវគ្នាជាអ៊ីដ្រូសែន។ ជាទូទៅ ស៊េរីបែបនេះអាចត្រូវបានតំណាងដោយខ្សែសង្វាក់នៃការផ្លាស់ប្តូរដូចខាងក្រោមៈ

2. ស៊េរីហ្សែននៃលោហធាតុដែលត្រូវគ្នានឹងមូលដ្ឋានដែលមិនអាចរលាយបាន។ ស៊េរីនេះគឺសម្បូរបែបនៅក្នុងទំនាក់ទំនងហ្សែនព្រោះវាកាន់តែឆ្លុះបញ្ចាំងយ៉ាងពេញលេញនូវគំនិតនៃការផ្លាស់ប្តូរគ្នាទៅវិញទៅមក (ដោយផ្ទាល់និងបញ្ច្រាស) ។ ជាទូទៅ ស៊េរីបែបនេះអាចត្រូវបានតំណាងដោយខ្សែសង្វាក់នៃការផ្លាស់ប្តូរដូចខាងក្រោមៈ

ស៊េរីហ្សែននៃ nonmetals ឆ្លុះបញ្ចាំងពីទំនាក់ទំនងនៃសារធាតុនៃថ្នាក់ផ្សេងគ្នាដែលផ្អែកលើ nonmetal ដូចគ្នា។
នៅទីនេះផងដែរ ពូជពីរអាចត្រូវបានសម្គាល់។
1. ស៊េរីហ្សែននៃ nonmetals ដែលអាស៊ីតរលាយត្រូវគ្នាជា hydroxide អាចត្រូវបានឆ្លុះបញ្ចាំងក្នុងទម្រង់នៃខ្សែសង្វាក់នៃការផ្លាស់ប្តូរដូចខាងក្រោមៈ
nonmetal -> អុកស៊ីដអាស៊ីត -> អាស៊ីត -> អំបិល
ឧទាហរណ៍ ស៊េរីហ្សែននៃផូស្វ័រ៖
2. ស៊េរីហ្សែននៃ nonmetals ដែលត្រូវនឹងអាស៊ីតមិនរលាយអាចត្រូវបានតំណាងដោយប្រើខ្សែសង្វាក់នៃការបំប្លែងដូចខាងក្រោមៈ
មិនមែនលោហៈ - អុកស៊ីដអាស៊ីត - អំបិល - អាស៊ីត - អុកស៊ីដអាស៊ីត - មិនមែនលោហៈ
ដោយសារអាស៊ីតដែលយើងបានសិក្សា មានតែអាស៊ីតស៊ីលីកប៉ុណ្ណោះដែលមិនរលាយ ជាឧទាហរណ៍នៃស៊េរីហ្សែនចុងក្រោយ សូមពិចារណាពីស៊េរីហ្សែនស៊ីលីកុន៖
1. តំណពូជ។
2. ស៊េរីហ្សែននៃលោហធាតុ និងពូជរបស់វា។
3. ស៊េរីហ្សែននៃមិនមែនលោហធាតុ និងពូជរបស់វា។
សរសេរសមីការប្រតិកម្មដែលអាចត្រូវបានប្រើដើម្បីអនុវត្តការបំប្លែងដែលបញ្ជាក់ពីស៊េរីហ្សែននៃលោហធាតុ និងមិនមែនលោហធាតុ។ ផ្តល់ឈ្មោះសារធាតុ និងសរសេរសមីការសម្រាប់ប្រតិកម្មដែលពាក់ព័ន្ធនឹងអេឡិចត្រូលីតក្នុងទម្រង់អ៊ីយ៉ុង។
សរសេរសមីការប្រតិកម្មដែលអ្នកអាចអនុវត្តការបំប្លែងដូចខាងក្រោម (តើមានព្រួញប៉ុន្មាន សមីការប្រតិកម្មជាច្រើន)៖
ក) Li - Li2O - LiOH - LiNO3
ខ) S - SO2 - H2SO3 - Na2SO3 - SO2 - CaSO3
សរសេរសមីការសម្រាប់ប្រតិកម្មដែលពាក់ព័ន្ធនឹងអេឡិចត្រូលីតក្នុងទម្រង់អ៊ីយ៉ុងផងដែរ។
សារធាតុខាងក្រោមនេះនឹងប្រតិកម្មជាមួយអាស៊ីត hydrochloric៖ ម៉ាញេស្យូម ទង់ដែង (II) អុកស៊ីដ ទង់ដែង (II) អ៊ីដ្រូសែន ទង់ដែង ម៉ាញ៉េស្យូមនីត្រាត ជាតិដែក (III) អ៊ីដ្រូសែន ស៊ីលីកុន (IV) អុកស៊ីដ ប្រាក់នីត្រាត ជាតិដែក (II) ស៊ុលហ្វីត ? សរសេរសមីការសម្រាប់ប្រតិកម្មដែលអាចកើតមានក្នុងទម្រង់ម៉ូលេគុល និងអ៊ីយ៉ុង។
ប្រសិនបើប្រតិកម្មមិនអាចអនុវត្តបាន សូមពន្យល់ពីមូលហេតុ។
សារធាតុខាងក្រោមមួយណានឹងប្រតិកម្មជាមួយសូដ្យូមអ៊ីដ្រូគីមី៖ កាបូន (IV) ម៉ូណូអុកស៊ីត។ កាល់ស្យូមអ៊ីដ្រូសែន ទង់ដែង(II) អុកស៊ីដ ទង់ដែង(II) នីត្រាត អាម៉ូញ៉ូមក្លរួ អាស៊ីតស៊ីលីក ប៉ូតាស្យូមស៊ុលហ្វាត? សរសេរសមីការសម្រាប់ប្រតិកម្មដែលអាចកើតមានក្នុងទម្រង់ម៉ូលេគុល និងអ៊ីយ៉ុង។ ប្រសិនបើប្រតិកម្មមិនកើតឡើង ចូរពន្យល់ពីមូលហេតុ។
ផ្តល់និយមន័យសម្រាប់គ្រប់ថ្នាក់នៃសារធាតុដែលបានផ្តល់ឱ្យក្នុងតារាង។ តើសារធាតុនីមួយៗចែកចេញជាក្រុមអ្វីខ្លះ?
ពិភពសម្ភារៈដែលយើងរស់នៅ និងដែលយើងជាផ្នែកតូចមួយគឺមួយ ហើយក្នុងពេលតែមួយមានភាពចម្រុះគ្មានទីបញ្ចប់។ ការរួបរួមនិងភាពចម្រុះនៃសារធាតុគីមីនៃពិភពលោកនេះត្រូវបានបង្ហាញយ៉ាងច្បាស់បំផុតនៅក្នុងទំនាក់ទំនងហ្សែននៃសារធាតុដែលត្រូវបានឆ្លុះបញ្ចាំងនៅក្នុងអ្វីដែលគេហៅថាស៊េរីហ្សែន។ ចូរយើងរំលេចនូវលក្ខណៈពិសេសបំផុតនៃស៊េរីបែបនេះ។
1. សារធាតុទាំងអស់នៅក្នុងស៊េរីនេះត្រូវតែបង្កើតឡើងដោយធាតុគីមីមួយ។ ឧទាហរណ៍ ស៊េរីដែលសរសេរដោយប្រើរូបមន្តខាងក្រោម៖
2. សារធាតុដែលបង្កើតឡើងដោយធាតុដូចគ្នាត្រូវតែជាកម្មសិទ្ធិរបស់ថ្នាក់ផ្សេងគ្នា ពោលគឺឆ្លុះបញ្ចាំងពីទម្រង់ផ្សេងគ្នានៃអត្ថិភាពរបស់វា។
3. សារធាតុដែលបង្កើតជាស៊េរីហ្សែននៃធាតុមួយត្រូវតែភ្ជាប់ដោយការបំប្លែងទៅវិញទៅមក។ ដោយផ្អែកលើលក្ខណៈពិសេសនេះ វាអាចបែងចែករវាងស៊េរីហ្សែនពេញលេញ និងមិនទាន់ពេញលេញ។
ឧទាហរណ៍ ស៊េរីហ្សែនខាងលើនៃ bromine នឹងមិនពេញលេញ មិនពេញលេញ។ នេះជាជួរបន្ទាប់៖
អាចត្រូវបានចាត់ទុកថាពេញលេញរួចទៅហើយ: វាបានចាប់ផ្តើមជាមួយនឹងសារធាតុសាមញ្ញ bromine និងបញ្ចប់ជាមួយវា។
សរុបសេចក្តីខាងលើ យើងអាចផ្តល់និយមន័យដូចខាងក្រោមនៃស៊េរីហ្សែន។
ស៊េរីហ្សែន- នេះគឺជាសារធាតុមួយចំនួន - តំណាងនៃថ្នាក់ផ្សេងៗគ្នា ដែលជាសមាសធាតុនៃធាតុគីមីមួយ ដែលតភ្ជាប់ដោយការបំប្លែងទៅវិញទៅមក និងឆ្លុះបញ្ចាំងពីប្រភពដើមទូទៅនៃសារធាតុទាំងនេះ ឬហ្សែនរបស់វា។
តំណពូជ- គំនិតទូទៅជាងស៊េរីហ្សែន ដែលទោះបីជាមានភាពរស់រវើកក៏ដោយ ប៉ុន្តែការបង្ហាញជាក់លាក់នៃការតភ្ជាប់នេះ ដែលត្រូវបានដឹងក្នុងអំឡុងពេលនៃការផ្លាស់ប្តូរគ្នាទៅវិញទៅមកនៃសារធាតុ។ បន្ទាប់មក ជាក់ស្តែង ស៊េរីនៃសារធាតុដែលបានផ្តល់ឱ្យដំបូងក៏សមនឹងនិយមន័យនេះដែរ។
ស៊េរីហ្សែនមានបីប្រភេទ៖
ស៊េរីលោហធាតុដែលមានជាងគេបំផុតបង្ហាញពីស្ថានភាពអុកស៊ីតកម្មផ្សេងៗគ្នា។ ជាឧទាហរណ៍ សូមពិចារណាស៊េរីហ្សែននៃជាតិដែកដែលមានស្ថានភាពអុកស៊ីតកម្ម +2 និង +3៖

ចូរយើងចាំថា ដើម្បីកត់សុីជាតិដែកទៅជាជាតិដែក (II) ក្លរ អ្នកត្រូវយកសារធាតុអុកស៊ីតកម្មខ្សោយជាងដើម្បីទទួលបានជាតិដែក (III) ក្លរួ៖

ស្រដៀងគ្នាទៅនឹងស៊េរីដែក ស៊េរីមិនមែនលោហធាតុដែលមានស្ថានភាពអុកស៊ីតកម្មផ្សេងគ្នាគឺសម្បូរទៅដោយចំណង ឧទាហរណ៍ ស៊េរីហ្សែននៃស្ពាន់ធ័រដែលមានស្ថានភាពអុកស៊ីតកម្ម +4 និង +6៖

មានតែការផ្លាស់ប្តូរចុងក្រោយប៉ុណ្ណោះដែលអាចបង្កឱ្យមានការលំបាក។ អនុវត្តតាមច្បាប់៖ ដើម្បីទទួលបានសារធាតុសាមញ្ញពីសមាសធាតុអុកស៊ីតកម្មនៃធាតុមួយ អ្នកត្រូវយកសម្រាប់គោលបំណងនេះ សមាសធាតុដែលកាត់បន្ថយបំផុតរបស់វា ឧទាហរណ៍ សមាសធាតុអ៊ីដ្រូសែនងាយនឹងបង្កជាហេតុនៃមិនមែនលោហៈ។ ក្នុងករណីរបស់យើង៖
ប្រតិកម្មនេះនៅក្នុងធម្មជាតិបង្កើតស្ពាន់ធ័រពីឧស្ម័នភ្នំភ្លើង។
ដូចគ្នាដែរចំពោះក្លរីន៖
3. ស៊េរីហ្សែននៃលោហៈដែលត្រូវគ្នានឹង amphoteric oxide និង hydroxide,សម្បូរទៅដោយមូលបត្របំណុល ព្រោះអាស្រ័យលើលក្ខខណ្ឌ ពួកវាបង្ហាញលក្ខណៈសម្បត្តិអាស៊ីត ឬមូលដ្ឋាន។
ជាឧទាហរណ៍ សូមពិចារណាស៊េរីហ្សែននៃស័ង្កសី៖

ទំនាក់ទំនងហ្សែនរវាងថ្នាក់នៃសារធាតុអសរីរាង្គ
លក្ខណៈគឺជាប្រតិកម្មរវាងអ្នកតំណាងនៃស៊េរីហ្សែនផ្សេងៗគ្នា។ សារធាតុពីស៊េរីហ្សែនដូចគ្នា ជាក្បួនមិនមានអន្តរកម្មទេ។
ឧទាហរណ៍៖
1. លោហៈ + មិនមែនលោហៈ = អំបិល
Hg + S = HgS
2Al + 3I 2 = 2AlI ៣
2. អុកស៊ីដមូលដ្ឋាន + អុកស៊ីដអាស៊ីត = អំបិល
លី 2 O + CO 2 = Li 2 CO 3
CaO + SiO 2 = CaSiO ៣
3. មូលដ្ឋាន + អាស៊ីត = អំបិល
Cu(OH) 2 + 2HCl = CuCl 2 + 2H 2 O
FeCl 3 + 3HNO 3 = Fe(NO 3) 3 + 3HCl
អាស៊ីតអំបិល អាស៊ីតអំបិល
4. លោហៈ - អុកស៊ីដសំខាន់
2Ca + O2 = 2CaO
4Li + O 2 = 2Li 2 O
5. មិនមែនលោហៈ - អុកស៊ីដអាស៊ីត
S + O 2 = SO 2
4As + 5O 2 = 2As 2 O 5
6. អុកស៊ីដមូលដ្ឋាន - មូលដ្ឋាន
BaO + H 2 O = Ba(OH) ២
លី 2 O + H 2 O = 2LiOH
7. អុកស៊ីដអាស៊ីត - អាសុីត
P 2 O 5 + 3H 2 O = 2H 3 PO 4
SO 3 + H 2 O = H 2 SO 4
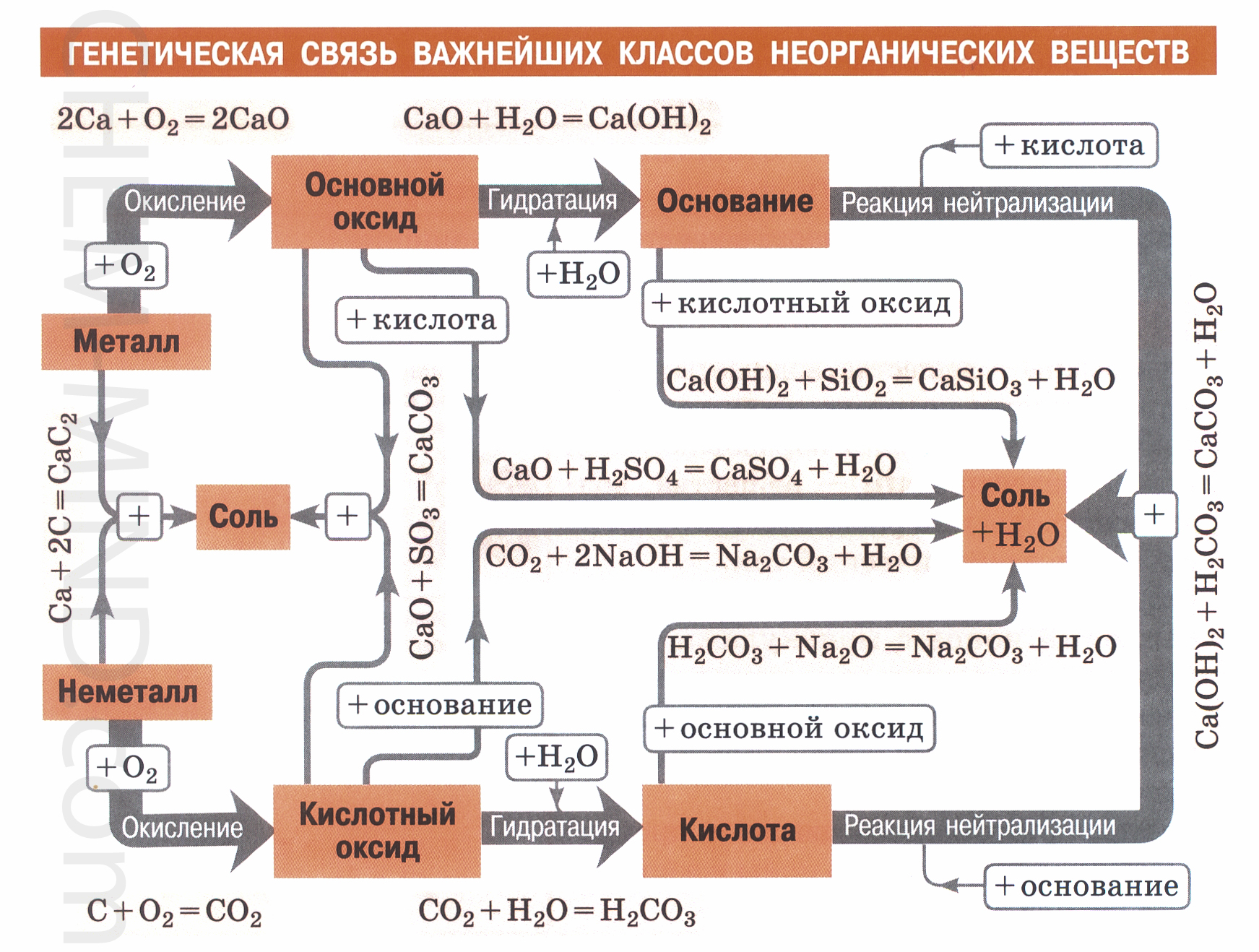
ស៊េរីហ្សែននៃលោហធាតុ និងសមាសធាតុរបស់វា។
ជួរនីមួយៗមានលោហៈ អុកស៊ីដសំខាន់ មូលដ្ឋាន និងអំបិលនៃលោហៈដូចគ្នា៖
ដើម្បីផ្លាស់ទីពីលោហធាតុទៅជាអុកស៊ីដមូលដ្ឋាននៅក្នុងស៊េរីទាំងអស់នេះ ប្រតិកម្មនៃការរួមបញ្ចូលគ្នាជាមួយអុកស៊ីហ្សែនត្រូវបានប្រើឧទាហរណ៍៖
2Ca + O 2 = 2CaO; 2Mg + O 2 = 2MgO;
ការផ្លាស់ប្តូរពីអុកស៊ីដមូលដ្ឋានទៅមូលដ្ឋាននៅក្នុងជួរពីរដំបូងត្រូវបានអនុវត្តតាមរយៈប្រតិកម្មជាតិទឹកដែលអ្នកស្គាល់ ឧទាហរណ៍៖
СaO + H 2 O = Сa(OH) ២.
សម្រាប់ជួរពីរចុងក្រោយ អុកស៊ីដ MgO និង FeO ដែលមាននៅក្នុងពួកវាមិនមានប្រតិកម្មជាមួយទឹកទេ។ ក្នុងករណីបែបនេះ ដើម្បីទទួលបានមូលដ្ឋាន អុកស៊ីដទាំងនេះដំបូងត្រូវបានបំប្លែងទៅជាអំបិល ហើយបន្ទាប់មកពួកវាត្រូវបានបំប្លែងទៅជាមូលដ្ឋាន។ ដូច្នេះ ជាឧទាហរណ៍ ដើម្បីអនុវត្តការផ្លាស់ប្តូរពី MgO oxide ទៅ Mg(OH) 2 hydroxide ប្រតិកម្មជាបន្តបន្ទាប់ត្រូវបានប្រើ៖
MgO + H 2 SO 4 = MgSO 4 + H 2 O; MgSO 4 + 2NaOH = Mg(OH) 2 ↓ + Na 2 SO ៤.
ការផ្លាស់ប្តូរពីមូលដ្ឋានទៅអំបិលត្រូវបានអនុវត្តដោយប្រតិកម្មដែលអ្នកបានដឹងរួចមកហើយ។ ដូច្នេះមូលដ្ឋានរលាយ (អាល់កាឡាំង) ដែលមានទីតាំងនៅជួរពីរដំបូងត្រូវបានបំលែងទៅជាអំបិលក្រោមសកម្មភាពនៃអាស៊ីតអុកស៊ីតអាស៊ីតឬអំបិល។ មូលដ្ឋានមិនរលាយពីជួរពីរចុងក្រោយបង្កើតជាអំបិលក្រោមសកម្មភាពនៃអាស៊ីត។
ស៊េរីហ្សែននៃ nonmetals និងសមាសធាតុរបស់វា។.
ស៊េរីនីមួយៗមានសារធាតុមិនមែនលោហធាតុ អុកស៊ីដអាស៊ីត អាស៊ីតដែលត្រូវគ្នា និងអំបិលដែលមានផ្ទុកអ៊ីយ៉ុងនៃអាស៊ីតនេះ៖
ដើម្បីផ្លាស់ទីពីមិនមែនលោហធាតុទៅជាអុកស៊ីដអាស៊ីតក្នុងស៊េរីទាំងអស់នេះ ប្រតិកម្មនៃការរួមបញ្ចូលគ្នាជាមួយអុកស៊ីហ្សែនត្រូវបានប្រើឧទាហរណ៍៖
4P + 5O 2 = 2 P 2 O 5 ; Si + O 2 = SiO 2;
ការផ្លាស់ប្តូរពីអុកស៊ីដអាស៊ីតទៅជាអាស៊ីតក្នុងជួរបីដំបូងត្រូវបានអនុវត្តតាមរយៈប្រតិកម្មជាតិទឹកដែលអ្នកស្គាល់ ឧទាហរណ៍៖
P 2 O 5 + 3H 2 O = 2 H 3 PO 4 ។
ទោះជាយ៉ាងណាក៏ដោយអ្នកដឹងថាអុកស៊ីដ SiO 2 ដែលមាននៅជួរចុងក្រោយមិនមានប្រតិកម្មជាមួយទឹកទេ។ ក្នុងករណីនេះ វាត្រូវបានបំប្លែងជាលើកដំបូងទៅជាអំបិលដែលត្រូវគ្នា ដែលអាស៊ីតដែលចង់បានត្រូវបានទទួល៖
SiO 2 + 2KOH = K 2 SiO 3 + H 2 O; K 2 SiO 3 + 2HCl = 2KCl + H 2 SiO 3 ↓ ។
ការផ្លាស់ប្តូរពីអាស៊ីតទៅជាអំបិលអាចត្រូវបានអនុវត្តដោយប្រតិកម្មដែលអ្នកស្គាល់ជាមួយនឹងអុកស៊ីដ មូលដ្ឋាន ឬអំបិល។
អ្វីដែលត្រូវចងចាំ៖
· សារធាតុនៃស៊េរីហ្សែនដូចគ្នាមិនមានប្រតិកម្មជាមួយគ្នាទេ។
· សារធាតុនៃប្រភេទផ្សេងគ្នានៃស៊េរីហ្សែនមានប្រតិកម្មជាមួយគ្នា។ ផលិតផលនៃប្រតិកម្មបែបនេះតែងតែជាអំបិល (រូបភាពទី 5)៖
អង្ករ។ 5. ដ្យាក្រាមនៃទំនាក់ទំនងរវាងសារធាតុនៃស៊េរីហ្សែនផ្សេងៗគ្នា។
ដ្យាក្រាមនេះបង្ហាញពីទំនាក់ទំនងរវាងថ្នាក់ផ្សេងគ្នានៃសមាសធាតុអសរីរាង្គ និងពន្យល់ពីភាពខុសគ្នានៃប្រតិកម្មគីមីរវាងពួកវា។
កិច្ចការលើប្រធានបទ៖
សរសេរសមីការប្រតិកម្មដែលអាចប្រើដើម្បីអនុវត្តការបំប្លែងដូចខាងក្រោម៖
1. Na → Na 2 O → NaOH → Na 2 CO 3 → Na 2 SO 4 → NaOH;
2. P → P 2 O 5 → H 3 PO 4 → K 3 PO 4 → Ca 3 (PO 4) 2 → CaSO 4 ;
3. Ca → CaO → Ca(OH) 2 → CaCl 2 → CaCO 3 → CaO;
4. S → SO 2 → H 2 SO 3 → K 2 SO 3 → H 2 SO 3 → BaSO 3 ;
5. Zn → ZnO → ZnCl 2 → Zn(OH) 2 → ZnSO 4 → Zn(OH) 2;
6. C → CO 2 → H 2 CO 3 → K 2 CO 3 → H 2 CO 3 → CaCO 3 ;
7. Al → Al 2 (SO 4) 3 → Al(OH) 3 → Al 2 O 3 → AlCl 3;
8. Fe → FeCl 2 → FeSO 4 → Fe(OH) 2 → FeO → Fe 3 (PO 4) 2;
9. Si → SiO 2 → H 2 SiO 3 → Na 2 SiO 3 → H 2 SiO 3 → SiO 2;
10. Mg → MgCl 2 → Mg(OH) 2 → MgSO 4 → MgCO 3 → MgO;
11. K → KOH → K 2 CO 3 → KCl → K 2 SO 4 → KOH;
12. S → SO 2 → CaSO 3 → H 2 SO 3 → SO 2 → Na 2 SO 3;
13. S → H 2 S → Na 2 S → H 2 S → SO 2 → K 2 SO 3;
14. Cl 2 → HCl → AlCl 3 → KCl → HCl → H 2 CO 3 → CaCO 3 ;
15. FeO → Fe(OH) 2 → FeSO 4 → FeCl 2 → Fe(OH) 2 → FeO;
16. CO 2 → K 2 CO 3 → CaCO 3 → CO 2 → BaCO 3 → H 2 CO 3 ;
17. K 2 O → K 2 SO 4 → KOH → KCl → K 2 SO 4 → KNO 3;
18. P 2 O 5 → H 3 PO 4 → Na 3 PO 4 → Ca 3 (PO 4) 2 → H 3 PO 4 → H 2 SO 3;
19. Al 2 O 3 → AlCl 3 → Al(OH) 3 → Al(NO 3) 3 → Al 2 (SO 4) 3 → AlCl 3;
20. SO 3 → H 2 SO 4 → FeSO 4 → Na 2 SO 4 → NaCl → HCl;
21. KOH → KCl → K 2 SO 4 → KOH → Zn(OH) 2 → ZnO;
22. Fe(OH) 2 → FeCl 2 → Fe(OH) 2 → FeSO 4 → Fe(NO 3) 2 → Fe;
23. Mg(OH) 2 → MgO → Mg(NO 3) 2 → MgSO 4 → Mg(OH) 2 → MgCl 2;
24. Al(OH) 3 → Al 2 O 3 → Al(NO 3) 3 → Al 2 (SO 4) 3 → AlCl 3 → Al(OH) 3;
25. H 2 SO 4 → MgSO 4 → Na 2 SO 4 → NaOH → NaNO 3 → HNO 3;
26. HNO 3 → Ca(NO 3) 2 → CaCO 3 → CaCl 2 → HCl → AlCl 3;
27. CuCO 3 → Cu(NO 3) 2 → Cu(OH) 2 → CuO → CuSO 4 → Cu;
28. MgSO 4 → MgCl 2 → Mg(OH) 2 → MgO → Mg(NO 3) 2 → MgCO 3;
29. K 2 S → H 2 S → Na 2 S → H 2 S → SO 2 → K 2 SO 3;
30. ZnSO 4 → Zn(OH) 2 → ZnCl 2 → HCl → AlCl 3 → Al(OH) 3;
31. Na 2 CO 3 → Na 2 SO 4 → NaOH → Cu(OH) 2 → H 2 O → HNO 3;
