ĐỀ TÀI BÀI HỌC: Phần khối lượng của một nguyên tố hóa học trong hợp chất.
MỤC ĐÍCH CỦA BÀI HỌC: Học cách tính phần khối lượng của các nguyên tố trong hợp chất bằng công thức của hợp chất và thiết lập công thức hóa học của một chất phức tạp bằng cách sử dụng phần khối lượng đã biết của các nguyên tố hóa học.
Các khái niệm cơ bản. Phần khối lượng của một nguyên tố hóa học.
Kết quả học tập dự kiến
Chủ thể. Có thể tính phần khối lượng của một nguyên tố trong hợp chất bằng công thức của nó và thiết lập công thức hóa học của một chất phức tạp bằng cách sử dụng phần khối lượng đã biết của các nguyên tố hóa học.
Siêu chủ đề . Phát triển khả năng thiết lập các phép loại suy và sử dụng các thuật toán để giải quyết các vấn đề giáo dục và nhận thức.
Các loại hoạt động chính của học sinh Tính phần khối lượng của một nguyên tố trong hợp chất bằng công thức của nó. Thiết lập công thức hóa học của một chất phức tạp bằng cách sử dụng các phần khối lượng đã biết của các nguyên tố hóa học.
Cấu trúc bài học
TÔI. Giai đoạn tổ chức
II. Cập nhật kiến thức tham khảo
III. Học tài liệu mới
IV. Hợp nhất. Tóm tắt bài học
V.. Bài tập về nhà
Trong các lớp học
Thời gian tổ chức.
Kiểm tra bài tập về nhà.
Cập nhật kiến thức cơ bản.
Đưa ra định nghĩa: khối lượng nguyên tử tương đối, khối lượng phân tử tương đối.
Khối lượng nguyên tử tương đối có thể được đo bằng đơn vị nào?
Khối lượng phân tử tương đối có thể được đo bằng đơn vị nào?
Học tài liệu mới.
Làm việc với sách giáo khoa. Sách bài tập.
Các bạn ơi, giả sử chúng ta có một chất - axit sulfuricH 2 VÌ THẾ 4,
Chúng ta có thể tìm ra nguyên tử nào là một phần của hợp chất không?
Và số lượng của họ?
Và chúng kết hợp với nhau theo tỷ lệ khối lượng nào?
Tính tỷ lệ khối lượng hóa học
các nguyên tố trong một chất phức tạp. (trang 51)
Làm thế nào bạn có thể biết tỉ lệ khối lượng của các nguyên tố được kết hợp trong một hợp chất có công thức làH 2 VÌ THẾ 4 ?
tôi(H): tôi(S): tôi(Ô)= 2*2 + 32 + 16*4= 2:32:64 = 1:16:32.
1+16+32 = 49, tức là 49 phần khối lượng axit sunfuric, chứa 1 phần khối lượng hydro, 16 phần khối lượng lưu huỳnh, 32 phần khối lượng oxy.
Các bạn ơi, các bạn nghĩ sao, liệu chúng ta có thể tính được tỉ lệ của từng nguyên tố trong hợp chất không?
Hôm nay chúng ta sẽ làm quen với khái niệm mới về phần khối lượng của một nguyên tố trong hợp chất.
W- Phần khối lượng của nguyên tố trong hợp chất.
N- số nguyên tử của nguyên tố đó.
Ông- trọng lượng phân tử tương đối.
Tính phần khối lượng của các nguyên tố hóa học
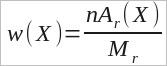
trong một chất phức tạp. (RT)
1. Nghiên cứu thuật toán tính phần khối lượng của một nguyên tố trong hợp chất.
Nhiệm vụ số 1 (RT)
Suy ra công thức hóa học nếu biết phần khối lượng của các nguyên tố hóa học,
có trong chất này. (RT)
2. Nghiên cứu thuật toán tính phần khối lượng của một nguyên tố trong hợp chất.
Vấn đề số 5 (RT)
Tổng hợp tài liệu đã học.
RT trang 25 số 2.
RT trang 27 số 6.
Tóm tắt bài học.
Những khái niệm mới nào bạn đã học được trong lớp hôm nay?
Làm việc độc lập.
Bài tập về nhà:
nghiên cứu §15 trang 51 - 53;
trả lời các câu hỏi số 3,4,7 tr. 53-54 (bằng văn bản).
P Danh sách tài liệu được sử dụng
Sách giáo khoa. Hoá học lớp 8. tự động G.E. Viêm Rudz, F.G. Feldman. Nhà xuất bản "Prosveshcheniye", 2014.
Sách bài tập hóa học. tự động Borovskikh T.A.



Bài học17
Chủ thể. Tính phần khối lượng của một nguyên tố trong thành phần của chất.
Giải bài toán xác định công thức hóa học dựa vào thành phần khối lượng của các nguyên tố cấu tạo nên chất
Mục tiêu: khắc sâu kiến thức của học sinh về phần khối lượng của một nguyên tố trong thành phần của chất; nâng cao kỹ năng thực hành tính thành phần khối lượng của một chất, giải các bài toán xác định công thức của một chất dựa vào thành phần khối lượng của các nguyên tố cấu tạo nên phân tử của chất đó.
Loại bài: đào sâu và điều chỉnh kiến thức, củng cố kĩ năng thực hành.
Hình thức làm việc: làm việc trực tiếp, làm việc độc lập bằng văn bản.
Thiết bị: hệ thống tuần hoàn các nguyên tố hóa học, thẻ nhiệm vụ cho công việc trực tiếp, thuật toán.
II. Cập nhật kiến thức
1. Học sinh viết lên bảng và giải thích công thức tính phần khối lượng của một nguyên tố trong thành phần chất đó.
2. Chúng tôi kiểm tra bài tập về nhà (câu hỏi trực tiếp và sửa lỗi).

3. Tính thành phần khối lượng các nguyên tố trong phân tử H 2 SO 4.
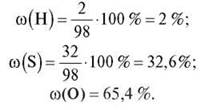
III. Tổng hợp các kỹ năng và khả năng
Bài tập huấn luyện
Bài tập 1. Sắp xếp các chất theo thứ tự tăng dần về khối lượng của Oxy trong phân tử. (Điền vào bảng trên bảng.)
Cu2O |
Al2O3 |
Fe2O3 |
|||
20,7 |
|||||
Bài tập 2. (Giáo viên giải thích.) Một số hợp chất của Nitơ với Oxi chứa 63,2% Nitơ. Xác định công thức của chất này nếu khối lượng phân tử của nó là 76 giờ sáng.

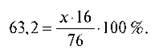
![]()
Do đó, số lượng nguyên tử oxy là ba.
2. m(N) = 76 – 3 18 = 28.
Biết rằng Ar(N) = 14,
trong = 28/14 = 2.
Do đó, số nguyên tử Nitơ là hai và công thức của chất là N 2 O 3.
Nhiệm vụ 3. Phần khối lượng của Carbon khi kết hợp với Oxy là 27,3%. Xác định công thức của hợp chất này khi biết khối lượng phân tử tương đối của nó là 44.
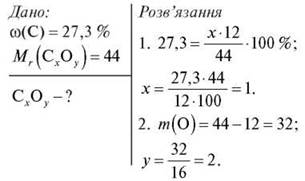
Đáp án: CO2.
Nhiệm vụ 4. Phần khối lượng của Cuprum kết hợp với Oxy là 88,9%. Khối lượng phân tử tương đối của hợp chất này là 144. Xác định công thức của hợp chất CuxOy.
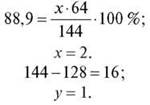
Đáp án: Cu2O.
IV. Công việc độc lập bằng văn bản về các lựa chọn
Nhiệm vụ 1. Theo công thức hóa học của chất:
Mô tả thành phần định tính của phân tử;
Mô tả thành phần định lượng của phân tử;
Tính thành phần khối lượng của các nguyên tố có trong phân tử chất này.
Lựa chọn tôi |
Phương án II |
Phương án III |
FeCl3 |
P2O5 |
C3H8 |
Cu(OH)2 |
Fe(OH)3 |
Al(OH)3 |
Na2SO4 |
K2CO3 |
Na3PO4 |
Bài 2. Dựa vào thành phần khối lượng đã biết của Clo trong thành phần chất và khối lượng nguyên tử phân tử, hãy suy ra công thức của chất này.
Ông (MgxCl trong) = 95 |
Ông (AlxCl trong) = 133,5 |
Ông (FexCl trong) = 162,5 |
ω(Cl) = 74,7% |
ω(Сl) = 79% |
ω(Сl) = 65% |
V. Bài tập về nhà
Nhắc lại phần “Khối lượng của một nguyên tố trong thành phần chất”.
Nhiệm vụ sáng tạo. Phân tử baking soda chứa các nguyên tử Natri, Hydro, Carbon và Oxy. Phần khối lượng của các nguyên tố lần lượt bằng nhau: ω(Na) = 27,4%; ω(H) = 1,2%; ω(C) = 14,3%; ω(O) = 57,1%. Xác định công thức của baking soda và tính trọng lượng phân tử tương đối của nó.
