موضوع الدرس: الكسر الكتلي للعنصر الكيميائي في المركب.
الغرض من الدرس: تعلم كيفية حساب الجزء الكتلي للعناصر في المركب باستخدام صيغة المركب وإنشاء الصيغة الكيميائية لمادة معقدة باستخدام الكسور الكتلية المعروفة للعناصر الكيميائية.
مفاهيم أساسية. الجزء الكتلي من العنصر الكيميائي.
نتائج التعلم المخطط لها
موضوع. تكون قادرًا على حساب الجزء الكتلي لعنصر ما في المركب باستخدام صيغته وإنشاء الصيغة الكيميائية لمادة معقدة باستخدام أجزاء الكتلة المعروفة للعناصر الكيميائية.
موضوع ميتا . تنمية القدرة على إقامة المقارنات واستخدام الخوارزميات لحل المشكلات التعليمية والمعرفية.
الأنواع الرئيسية للأنشطة الطلابية. احسب الكسر الكتلي لعنصر ما في المركب باستخدام صيغته. إنشاء الصيغة الكيميائية لمادة معقدة باستخدام أجزاء الكتلة المعروفة من العناصر الكيميائية.
هيكل الدرس
أنا. المرحلة التنظيمية
ثانيا. تحديث المعرفة المرجعية
ثالثا. تعلم مواد جديدة
رابعا. الدمج. تلخيص الدرس
الخامس. العمل في المنزل
خلال الفصول الدراسية
تنظيم الوقت.
التحقق من الواجبات المنزلية.
تحديث المعرفة الأساسية.
إعطاء تعريفات: الكتلة الذرية النسبية، الكتلة الجزيئية النسبية.
ما هي الوحدات التي يمكن قياس الكتلة الذرية النسبية؟
في أي وحدات يمكن قياس الكتلة الجزيئية النسبية؟
تعلم مواد جديدة.
العمل مع الكتاب المدرسي. دفتر العمل.
يا رفاق، لنفترض أن لدينا مادة - حمض الكبريتيكح 2 لذا 4,
هل يمكننا معرفة الذرات التي تشكل جزءًا من المركب؟
وعددهم ؟
وما هي نسبة الكتلة التي يتم دمجها؟
حساب نسب الكتلة الكيميائية
العناصر في مادة معقدة. (صفحة 51)
كيف يمكنك معرفة نسب الكتلة التي يتم دمج العناصر فيها في مركب تكون صيغتهح 2 لذا 4 ?
م(ح): م(س): م(يا)= 2*2 + 32 + 16*4= 2:32:64 = 1:16:32.
1+16+32 = 49، أي 49 جزءًا من كتلة حمض الكبريتيك، يحتوي على جزء واحد من كتلة الهيدروجين، و16 جزءًا من كتلة الكبريت، و32 جزءًا من كتلة الأكسجين.
يا جماعة رأيكم نقدر نحسب نسبة كل عنصر في المركب؟
اليوم سوف نتعرف على المفهوم الجديد للكسر الكتلي للعنصر في المركب.
دبليو- الكسر الكتلي للعنصر الموجود في المركب .
ن- عدد ذرات العنصر .
السيد- الوزن الجزيئي النسبي.
حساب الكسور الجماعية للعناصر الكيميائية
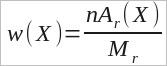
في مادة معقدة. (ر ت)
1. دراسة خوارزمية حساب الجزء الكتلي للعنصر في المركب.
المهمة رقم 1 (RT)
استخلاص الصيغ الكيميائية إذا كانت الأجزاء الكتلية للعناصر الكيميائية معروفة،
المدرجة في هذه المادة. (ر ت)
2. دراسة خوارزمية حساب الكسر الكتلي للعنصر في المركب.
المشكلة رقم 5 (رت)
توحيد المواد المدروسة.
صفحة RT 25 رقم 2.
صفحة RT 27 رقم 6.
تلخيص الدرس.
ما هي المفاهيم الجديدة التي تعلمتها في الفصل اليوم؟
عمل مستقل.
العمل في المنزل:
دراسة §15 ص 51 - 53؛
الإجابة على الأسئلة رقم 3،4،7 ص53-54 (كتابيا).
ص قائمة الأدب المستخدم.
كتاب مدرسي. الكيمياء الصف الثامن. آلي ج. رودزيتيس ، ف. فيلدمان. دار النشر "Prosveshcheniye"، 2014.
مصنف الكيمياء. آلي بوروفسكيخ ت.



درس17
موضوع. حساب الكسر الكتلي للعنصر في تكوين المادة.
حلول مسائل تحديد الصيغ الكيميائية على أساس الكسور الكتلية للعناصر التي تتكون منها المادة
الأهداف: تعميق معرفة الطلاب حول الجزء الكتلي للعنصر في تركيب المادة. تحسين المهارات العملية في حساب الجزء الكتلي للمادة، وحل المشكلات لتحديد صيغة المادة بناءً على الكسور الكتلية للعناصر التي يتكون منها جزيء المادة.
نوع الدرس: تعميق المعرفة وتعديلها وتعزيز المهارات العملية.
أشكال العمل: العمل الأمامي، العمل المستقل الكتابي.
المعدات: النظام الدوري للعناصر الكيميائية، بطاقات بمهام العمل الأمامي، الخوارزمية.
ثانيا. تحديث المعرفة
1. يكتب الطالب على السبورة ويشرح صيغة الكسر الكتلي للعنصر في تركيب المادة.
2. نتحقق من الواجبات المنزلية (الاستجواب والتصحيحات الشفهية).

3. احسب الكسور الكتلية للعناصر الموجودة في جزيء H 2 SO 4.
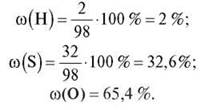
ثالثا. توحيد المهارات والقدرات
تمارين تدريبية
المهمة 1. رتب المواد بترتيب تصاعدي لنسبة كتلة الأكسجين في الجزيء. (املأ الجدول الموجود على السبورة).
Cu2O |
Al2O3 |
Fe2O3 |
|||
20,7 |
|||||
المهمة 2. (الشرح من المعلم.) تحتوي بعض مركبات النيتروجين مع الأكسجين على 63.2% نيتروجين. حدد صيغة هذه المادة إذا كان وزنها الجزيئي 76 م.

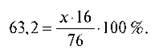
![]()
وبالتالي فإن عدد ذرات الأكسجين هو ثلاث.
2. م(ن) = 76 – 3 18 = 28.
مع العلم أن Ar(N) = 14،
في = 28/14 = 2.
ولذلك فإن عدد ذرات النيتروجين هو ذرتان، وصيغة المادة هي N 2 O 3.
المهمة 3. الجزء الكتلي للكربون في اتحاده مع الأكسجين هو 27.3%. حدد صيغة هذا المركب، مع العلم أن وزنه الجزيئي النسبي هو 44.
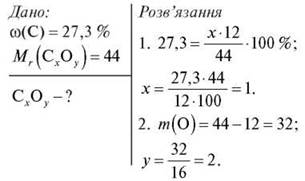
الجواب: ثاني أكسيد الكربون 2.
المهمة 4. الجزء الكتلي من كوبروم مع الأكسجين هو 88.9٪. الوزن الجزيئي النسبي لهذا المركب هو 144. حدد صيغة المركب CuxOy.
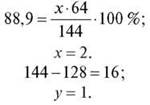
الجواب: النحاس 2O.
رابعا. عمل مستقل مكتوب على الخيارات
المهمة 1. حسب الصيغة الكيميائية للمادة:
وصف التركيب النوعي للجزيء؛
وصف التركيب الكمي للجزيء؛
احسب الكسور الكتلية للعناصر الموجودة في جزيء هذه المادة.
الخيار الأول |
الخيار الثاني |
الخيار الثالث |
FeCl3 |
P2O5 |
C3H8 |
النحاس (أوه)2 |
الحديد (أوه)3 |
آل(يا)3 |
Na2SO4 |
K2CO3 |
Na3PO4 |
المهمة 2. بناءً على نسبة كتلة الكلور المعروفة في تركيبة المادة والوزن الجزيئي الذري، اشتق صيغة هذه المادة.
السيد (MgxCl in) = 95 |
السيد (AlxCl in) = 133.5 |
السيد (FexCl in) = 162.5 |
ω(الكلور) = 74.7% |
ω(Сl) = 79% |
ω(Сl) = 65% |
خامسا الواجبات المنزلية
كرر القسم "الجزء الكتلي من العنصر في تركيب المادة."
مهمة إبداعية. يحتوي جزيء صودا الخبز على ذرات الصوديوم والهيدروجين والكربون والأكسجين. الكسور الكتلية للعناصر متساوية على التوالي: ω(Na) = 27.4%؛ ω(ح) = 1.2%؛ ω(ج) = 14.3%؛ ω(O) = 57.1%. تحديد صيغة صودا الخبز وحساب وزنها الجزيئي النسبي.
