1. إن التغير في الطاقة الداخلية نتيجة بذل الشغل يتميز بكمية الشغل، أي: الشغل هو مقياس للتغير في الطاقة الداخلية في عملية معينة. يتميز التغير في الطاقة الداخلية للجسم أثناء انتقال الحرارة بكمية تسمى كمية من الحرارة.
كمية الحرارة هي التغير في الطاقة الداخلية للجسم أثناء عملية انتقال الحرارة دون بذل شغل.
يُشار إلى كمية الحرارة بالحرف \(Q\) . وبما أن كمية الحرارة هي مقياس للتغير في الطاقة الداخلية، فإن وحدتها هي الجول (1 J).
عندما ينقل الجسم كمية معينة من الحرارة دون بذل شغل، فإن طاقته الداخلية تزداد؛ وإذا أطلق الجسم كمية معينة من الحرارة، فإن طاقته الداخلية تنخفض.
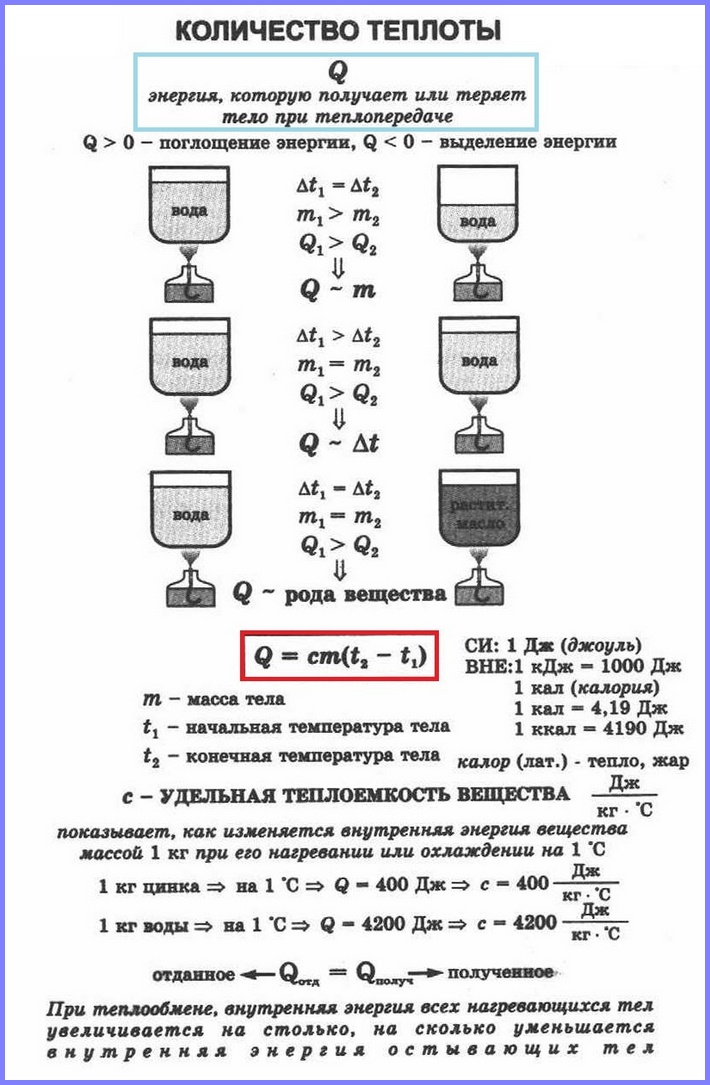
2. إذا صببت 100 جرام من الماء في وعاءين متطابقين، أحدهما و400 جرام في الآخر بنفس درجة الحرارة ووضعتهما على شعلات متماثلة، فإن الماء الموجود في الوعاء الأول سوف يغلي مبكرًا. وبالتالي، كلما زادت كتلة الجسم، زادت كمية الحرارة التي يحتاجها للتسخين. وينطبق الشيء نفسه على التبريد: عندما يتم تبريد جسم ذي كتلة أكبر، فإنه يطلق كمية أكبر من الحرارة. هذه الأجسام مصنوعة من نفس المادة وتسخن أو تبرد بنفس عدد الدرجات.
3. إذا قمنا الآن بتسخين 100 جرام من الماء من 30 إلى 60 درجة مئوية، أي. عند 30 درجة مئوية، ثم حتى 100 درجة مئوية، أي. بمقدار 70 درجة مئوية، ففي الحالة الأولى سيستغرق التسخين وقتًا أقل مما هو عليه في الحالة الثانية، وبالتالي فإن تسخين الماء بمقدار 30 درجة مئوية سيتطلب حرارة أقل من تسخين الماء بمقدار 70 درجة مئوية. وبالتالي، فإن كمية الحرارة تتناسب طرديًا مع الفرق بين درجات الحرارة النهائية \((t_2\,^\circ C) \) ودرجات الحرارة الأولية \((t_1\,^\circ C) \) : \( س\سيم(t_2- t_1) \) .
4. إذا صببت الآن 100 جرام من الماء في وعاء واحد، وسكبت القليل من الماء في وعاء آخر مماثل ووضعت فيه جسمًا معدنيًا بحيث تكون كتلته وكتلة الماء 100 جرام، وقمت بتسخين الأوعية على بلاطات متماثلة، إذن ستلاحظ أنه في الوعاء الذي يحتوي على الماء فقط ستكون درجة حرارته أقل من الوعاء الذي يحتوي على الماء وجسم معدني. لذلك، لكي تكون درجة حرارة المحتويات في كلا الوعاءين هي نفسها، من الضروري نقل حرارة إلى الماء أكثر من الماء والجسم المعدني. وبالتالي، فإن كمية الحرارة اللازمة لتسخين الجسم تعتمد على نوع المادة التي يتكون منها الجسم.
5. يتميز اعتماد كمية الحرارة اللازمة لتسخين الجسم على نوع المادة بكمية فيزيائية تسمى السعة الحرارية النوعية للمادة.
تسمى الكمية الفيزيائية التي تساوي كمية الحرارة التي يجب نقلها إلى 1 كجم من المادة لتسخينها بمقدار 1 درجة مئوية (أو 1 كلفن) بالسعة الحرارية النوعية للمادة.
يطلق 1 كجم من المادة نفس كمية الحرارة عند تبريدها بمقدار 1 درجة مئوية.
يُشار إلى السعة الحرارية النوعية بالحرف \(c\) . وحدة السعة الحرارية النوعية هي 1 جول/كجم درجة مئوية أو 1 جول/كجم كلفن.
يتم تحديد السعة الحرارية المحددة للمواد تجريبيا. تتمتع السوائل بسعة حرارية نوعية أعلى من المعادن؛ الماء لديه أعلى حرارة نوعية، والذهب لديه حرارة نوعية صغيرة جدا.
الحرارة النوعية للرصاص هي 140 جول/كجم درجة مئوية. هذا يعني أنه لتسخين 1 كجم من الرصاص بمقدار 1 درجة مئوية، من الضروري إنفاق كمية حرارة قدرها 140 جول. وسيتم إطلاق نفس الكمية من الحرارة عندما يبرد 1 كجم من الماء بمقدار 1 درجة مئوية.
وبما أن كمية الحرارة تساوي التغير في الطاقة الداخلية للجسم، فيمكننا القول إن السعة الحرارية النوعية توضح مقدار تغير الطاقة الداخلية لـ 1 كجم من المادة عندما تتغير درجة حرارتها بمقدار 1 درجة مئوية. على وجه الخصوص، تزيد الطاقة الداخلية لـ 1 كجم من الرصاص بمقدار 140 جول عند تسخينه بمقدار 1 درجة مئوية، وتنخفض بمقدار 140 جول عند تبريده.
كمية الحرارة \(Q \) اللازمة لتسخين جسم كتلته \(m \) من درجة الحرارة \((t_1\,^\circ C) \) إلى درجة الحرارة \((t_2\,^\ circ C) \) يساوي حاصل ضرب السعة الحرارية النوعية للمادة وكتلة الجسم والفرق بين درجتي الحرارة النهائية والابتدائية، أي.
\[ Q=cm(t_2()^\circ-t_1()^\circ) \]
وتستخدم نفس الصيغة لحساب كمية الحرارة التي يطلقها الجسم عند تبريده. فقط في هذه الحالة يجب طرح درجة الحرارة النهائية من درجة الحرارة الأولية، أي. اطرح درجة الحرارة الأصغر من درجة الحرارة الأكبر.
6. مثال على حل المشكلة. تم صب 100 جرام من الماء عند درجة حرارة 20 درجة مئوية في كوب يحتوي على 200 جرام من الماء عند درجة حرارة 80 درجة مئوية. وبعد ذلك وصلت درجة الحرارة في الوعاء إلى 60 درجة مئوية. ما مقدار الحرارة التي استقبلها الماء البارد وما مقدار الحرارة التي أطلقها الماء الساخن؟
عند حل مشكلة ما، يجب عليك تنفيذ التسلسل التالي من الإجراءات:
- اكتب بإيجاز شروط المشكلة؛
- تحويل قيم الكميات إلى SI؛
- تحليل المشكلة، وتحديد الهيئات التي تشارك في التبادل الحراري، والتي تعطي الطاقة والتي تستقبلها؛
- حل المشكلة بشكل عام.
- إجراء العمليات الحسابية.
- تحليل الإجابة المستلمة.
1. المهمة.
منح:
\(م_1 \) = 200 غرام
\(م_2\) = 100 جرام
\(t_1 \) = 80 درجة مئوية
\(t_2 \) = 20 درجة مئوية
\(ر\) = 60 درجة مئوية
______________
\(س_1 \) — ؟ \(س_2 \) — ؟
\(c_1 \) = 4200 جول/كجم درجة مئوية
2. سي:\(m_1\) = 0.2 كجم؛ \(م_2\) = 0.1 كجم.
3. تحليل المهمة. تصف المشكلة عملية التبادل الحراري بين الماء الساخن والبارد. يعطي الماء الساخن كمية من الحرارة \(Q_1 \) ويبرد من درجة الحرارة \(t_1 \) إلى درجة الحرارة \(t \) . يستقبل الماء البارد كمية الحرارة \(Q_2 \) ويتم تسخينه من درجة الحرارة \(t_2 \) إلى درجة الحرارة \(t \) .
4. حل المشكلة بشكل عام. يتم حساب كمية الحرارة المنبعثة من الماء الساخن بالصيغة: \(Q_1=c_1m_1(t_1-t) \) .
يتم حساب كمية الحرارة التي يتلقاها الماء البارد بالصيغة: \(Q_2=c_2m_2(t-t_2) \) .
5.
الحسابات.
\(Q_1 \) = 4200 جول/كجم · درجة مئوية · 0.2 كجم · 20 درجة مئوية = 16800 جول
\(Q_2\) = 4200 جول/كجم درجة مئوية 0.1 كجم 40 درجة مئوية = 16800 جول
6. الجواب هو أن كمية الحرارة المنبعثة من الماء الساخن تساوي كمية الحرارة التي يستقبلها الماء البارد. في هذه الحالة، تم النظر في الوضع المثالي ولم يؤخذ في الاعتبار استخدام كمية معينة من الحرارة لتسخين الزجاج الذي يوجد فيه الماء والهواء المحيط. في الواقع، كمية الحرارة المنبعثة من الماء الساخن أكبر من كمية الحرارة التي يستقبلها الماء البارد.
الجزء 1
1. السعة الحرارية النوعية للفضة هي 250 جول/(كجم درجة مئوية). ماذا يعني هذا؟
1) عندما يبرد 1 كجم من الفضة عند 250 درجة مئوية، تنطلق كمية من الحرارة قدرها 1 جول
2) عندما يبرد 250 كجم من الفضة بمقدار 1 درجة مئوية، تنطلق كمية من الحرارة مقدارها 1 جول
3) عندما يبرد 250 كجم من الفضة بمقدار 1 درجة مئوية، يتم امتصاص كمية من الحرارة مقدارها 1 J
4) عندما يبرد 1 كجم من الفضة بمقدار 1 درجة مئوية، تنطلق كمية من الحرارة قدرها 250 جول
2. تبلغ السعة الحرارية النوعية للزنك 400 جول/(كجم درجة مئوية). هذا يعني انه
1) عند تسخين 1 كجم من الزنك بمقدار 400 درجة مئوية، تزداد طاقته الداخلية بمقدار 1 J
2) عند تسخين 400 كجم من الزنك بمقدار 1 درجة مئوية، تزداد طاقته الداخلية بمقدار 1 J
3) لتسخين 400 كجم من الزنك بمقدار 1 درجة مئوية، من الضروري إنفاق 1 J من الطاقة
4) عند تسخين 1 كجم من الزنك بمقدار 1 درجة مئوية، تزداد طاقته الداخلية بمقدار 400 J
3. عند نقل كمية الحرارة \(Q \) إلى جسم صلب له كتلة \(m \) ، تزيد درجة حرارة الجسم بمقدار \(\Delta t^\circ \) . أي من العبارات التالية تحدد السعة الحرارية النوعية لمادة هذا الجسم؟
1) \(\frac(m\Delta t^\circ)(Q) \)
2) \(\frac(Q)(m\Delta t^\circ) \)
3) \(\frac(Q)(\Delta t^\circ) \)
4) \(Qm\Delta t^\circ \)
4. يوضح الشكل رسمًا بيانيًا لاعتماد كمية الحرارة اللازمة لتسخين جسمين (1 و 2) لهما نفس الكتلة على درجة الحرارة. قارن بين قيم السعة الحرارية النوعية (\(c_1 \) و \(c_2 \) ) للمواد التي تتكون منها هذه الأجسام.

1) \(c_1=c_2 \)
2) \(c_1>c_2 \)
3)\(ج_1
5. يوضّح الشكل كمية الحرارة المنتقلة إلى جسمين متساويين في الكتلة عندما تتغير درجة حرارتهما بنفس عدد الدرجات. ما العلاقة الصحيحة بين السعات الحرارية النوعية للمواد التي تتكون منها الأجسام؟

1) \(c_1=c_2\)
2) \(c_1=3c_2\)
3) \(c_2=3c_1\)
4) \(c_2=2c_1\)
6. يوضح الشكل رسمًا بيانيًا لدرجة حرارة الجسم الصلب اعتمادًا على كمية الحرارة المنبعثة منه. وزن الجسم 4 كجم. ما هي السعة الحرارية النوعية لمادة هذا الجسم؟

1) 500 جول/(كجم درجة مئوية)
2) 250 جول/(كجم درجة مئوية)
3) 125 جول/(كجم درجة مئوية)
4) 100 جول/(كجم درجة مئوية)
7. عند تسخين مادة بلورية وزنها 100 جرام، تم قياس درجة حرارة المادة وكمية الحرارة المنقولة للمادة. تم تقديم بيانات القياس في شكل جدول. بافتراض إمكانية إهمال فقدان الطاقة، حدد السعة الحرارية النوعية للمادة في الحالة الصلبة.
1) 192 جول/(كجم درجة مئوية)
2) 240 جول/(كجم درجة مئوية)
3) 576 جول/(كجم درجة مئوية)
4) 480 جول/(كجم درجة مئوية)
8. لتسخين 192 جم من الموليبدينوم بمقدار 1 K، يلزمك نقل كمية من الحرارة قدرها 48 J إليها. ما هي الحرارة النوعية لهذه المادة؟
1) 250 جول/(كجم ك)
2) 24 جول/(كجم ك)
3) 4·10 -3 ي/(كجم ك)
4) 0.92 جول/(كجم ك)
9. ما كمية الحرارة اللازمة لتسخين 100 جم من الرصاص من 27 إلى 47 درجة مئوية؟
1) 390 ج
2) 26 كيلوجول
3) 260 ج
4) 390 كيلوجول
10. يتطلب تسخين الطوب من 20 إلى 85 درجة مئوية نفس كمية الحرارة التي يتطلبها تسخين الماء بنفس الكتلة بمقدار 13 درجة مئوية. السعة الحرارية النوعية للطوب هي
1) 840 جول/(كجم ك)
2) 21000 جول/(كجم ك)
3) 2100 جول/(كجم ك)
4) 1680 جول/(كجم ك)
11. من قائمة العبارات أدناه، اختر جملتين صحيحتين واكتب أرقامهما في الجدول.
1) كمية الحرارة التي يتلقاها الجسم عندما ترتفع درجة حرارته بعدد معين من الدرجات تساوي كمية الحرارة التي يطلقها هذا الجسم عندما تنخفض درجة حرارته بنفس العدد من الدرجات.
2) عندما تبرد المادة تزداد طاقتها الداخلية .
3) تستخدم كمية الحرارة التي تتلقاها المادة عند تسخينها بشكل أساسي لزيادة الطاقة الحركية لجزيئاتها.
4) تستخدم كمية الحرارة التي تتلقاها المادة عند تسخينها بشكل أساسي لزيادة الطاقة الكامنة للتفاعل بين جزيئاتها
5) لا يمكن تغيير الطاقة الداخلية للجسم إلا عن طريق إمداده بقدر معين من الحرارة
12. يعرض الجدول نتائج قياسات الكتلة \(\m\) والتغيرات في درجات الحرارة \(\Delta t\) وكمية الحرارة \(Q\) المنبعثة أثناء تبريد الأسطوانات المصنوعة من النحاس أو الألومنيوم .

ما هي العبارات التي تتوافق مع نتائج التجربة؟ حدد اثنين الصحيحين من القائمة المقدمة. اذكر أرقامهم. وبناء على القياسات التي تم إجراؤها، يمكن القول أن كمية الحرارة المنبعثة أثناء التبريد
1) يعتمد على المادة التي تصنع منها الاسطوانة.
2) لا يعتمد على المادة التي تصنع منها الاسطوانة.
3) يزداد مع زيادة كتلة الاسطوانة.
4) يزداد مع زيادة اختلاف درجات الحرارة.
5) السعة الحرارية النوعية للألمنيوم أكبر بأربع مرات من السعة الحرارية النوعية للقصدير.
الجزء 2
ج1.وُضِع جسم صلب كتلته ٢ كجم في فرن قدرته ٢ كيلو وات وبدأ في التسخين. يوضح الشكل اعتماد درجة الحرارة \(t\) لهذا الجسم على وقت التسخين \(\tau \) . ما هي السعة الحرارية النوعية للمادة؟

1) 400 جول/(كجم درجة مئوية)
2) 200 جول/(كجم درجة مئوية)
3) 40 جول/(كجم درجة مئوية)
4) 20 جول/(كجم درجة مئوية)
الإجابات


إن التغير في الطاقة الداخلية نتيجة بذل الشغل يتميز بكمية الشغل، أي: الشغل هو مقياس للتغير في الطاقة الداخلية في عملية معينة. يتميز التغير في الطاقة الداخلية للجسم أثناء انتقال الحرارة بكمية تسمى كمية الحرارة.
هو التغير في الطاقة الداخلية للجسم أثناء عملية انتقال الحرارة دون أداء شغل. يشار إلى كمية الحرارة بالحرف س .
يتم قياس الشغل والطاقة الداخلية والحرارة بنفس الوحدات - الجول ( ج)، مثل أي نوع من الطاقة.
في القياسات الحرارية، تم استخدام وحدة خاصة للطاقة سابقًا كوحدة لكمية الحرارة - السعرات الحرارية ( البراز)، يساوي كمية الحرارة اللازمة لتسخين 1 جرام من الماء بمقدار 1 درجة مئوية (بتعبير أدق، من 19.5 إلى 20.5 درجة مئوية). تُستخدم هذه الوحدة، على وجه الخصوص، حاليًا عند حساب استهلاك الحرارة (الطاقة الحرارية) في المباني السكنية. تم تحديد المعادل الميكانيكي للحرارة تجريبيًا - العلاقة بين السعرات الحرارية والجول: 1 كال = 4.2 ج.
عندما ينقل الجسم كمية معينة من الحرارة دون بذل شغل، فإن طاقته الداخلية تزداد؛ وإذا أطلق الجسم كمية معينة من الحرارة، فإن طاقته الداخلية تنخفض.
إذا صببت 100 جرام من الماء في وعاءين متطابقين، أحدهما و400 جرام في الآخر بنفس درجة الحرارة ووضعتهما على شعلات متماثلة، فإن الماء الموجود في الوعاء الأول سوف يغلي مبكرًا. وبالتالي، كلما زادت كتلة الجسم، زادت كمية الحرارة التي يحتاجها للإحماء. إنه نفس الشيء مع التبريد.

تعتمد كمية الحرارة اللازمة لتسخين الجسم أيضًا على نوع المادة التي يتكون منها الجسم. يتميز هذا الاعتماد لكمية الحرارة اللازمة لتسخين الجسم على نوع المادة بكمية فيزيائية تسمى السعة الحرارية محددة مواد.
هي كمية فيزيائية تساوي كمية الحرارة التي يجب نقلها إلى 1 كجم من المادة لتسخينها بمقدار 1 درجة مئوية (أو 1 كلفن). يطلق 1 كجم من المادة نفس كمية الحرارة عند تبريدها بمقدار 1 درجة مئوية.
يتم تحديد السعة الحرارية المحددة بالحرف مع. وحدة السعة الحرارية النوعية هي 1 ي/كجم درجة مئويةأو 1 جول/كجم درجة كلفن.
يتم تحديد السعة الحرارية المحددة للمواد تجريبيا. تتمتع السوائل بسعة حرارية نوعية أعلى من المعادن؛ الماء لديه أعلى حرارة نوعية، والذهب لديه حرارة نوعية صغيرة جدا.
وبما أن كمية الحرارة تساوي التغير في الطاقة الداخلية للجسم، فيمكننا القول إن السعة الحرارية النوعية توضح مدى تغير الطاقة الداخلية 1 كجمالمادة عندما تتغير درجة حرارتها 1 درجة مئوية. على وجه الخصوص، تزيد الطاقة الداخلية لـ 1 كجم من الرصاص بمقدار 140 جول عند تسخينه بمقدار 1 درجة مئوية، وتنخفض بمقدار 140 جول عند تبريده.
ساللازمة لتسخين جسم كتلته معلى درجة الحرارة ر 1 درجة مئويةتصل إلى درجة الحرارة ر 2 درجة مئوية، يساوي حاصل ضرب السعة الحرارية النوعية للمادة وكتلة الجسم والفرق بين درجتي الحرارة النهائية والابتدائية، أي.س = ج ∙ م (ر 2 - ر 1)
يتم استخدام نفس الصيغة لحساب كمية الحرارة التي يطلقها الجسم عند التبريد. فقط في هذه الحالة يجب طرح درجة الحرارة النهائية من درجة الحرارة الأولية، أي. اطرح درجة الحرارة الأصغر من درجة الحرارة الأكبر.

هذا ملخص للموضوع "كمية الحرارة. حرارة نوعية". حدد الخطوات التالية:
- انتقل إلى الملخص التالي:
سوف نتعلم في هذا الدرس كيفية حساب كمية الحرارة اللازمة لتسخين الجسم أو التي يطلقها عند تبريده. للقيام بذلك، سنقوم بتلخيص المعرفة التي تم الحصول عليها في الدروس السابقة.
بالإضافة إلى ذلك سنتعلم باستخدام صيغة كمية الحرارة التعبير عن الكميات المتبقية من هذه الصيغة وحسابها مع معرفة الكميات الأخرى. سيتم أيضًا النظر في مثال لمشكلة مع حل لحساب كمية الحرارة.
هذا الدرس مخصص لحساب كمية الحرارة عند تسخين الجسم أو إطلاقها عند تبريده.
القدرة على حساب الكمية المطلوبة من الحرارة مهمة جدًا. قد يكون ذلك ضروريًا، على سبيل المثال، عند حساب كمية الحرارة التي يجب نقلها إلى الماء لتدفئة الغرفة.
أرز. 1. كمية الحرارة التي يجب إيصالها إلى الماء لتدفئة الغرفة
أو لحساب كمية الحرارة المنبعثة عند احتراق الوقود في المحركات المختلفة:

أرز. 2. كمية الحرارة المنبعثة عند احتراق الوقود في المحرك
وهذه المعرفة مطلوبة أيضًا، على سبيل المثال، لتحديد كمية الحرارة التي تطلقها الشمس وتهطل على الأرض:

أرز. 3. كمية الحرارة التي تطلقها الشمس وتسقط على الأرض
لحساب كمية الحرارة، عليك أن تعرف ثلاثة أشياء (الشكل 4):
- وزن الجسم (والذي يمكن قياسه عادة باستخدام مقياس)؛
- الفرق في درجة الحرارة الذي يجب أن يتم من خلاله تسخين الجسم أو تبريده (يتم قياسه عادةً باستخدام مقياس الحرارة)؛
- السعة الحرارية المحددة للجسم (والتي يمكن تحديدها من الجدول).

أرز. 4. ما تحتاج إلى معرفته لتحديد
تبدو الصيغة التي يتم من خلالها حساب كمية الحرارة كما يلي:
تظهر الكميات التالية في هذه الصيغة:
كمية الحرارة المقاسة بالجول (J)؛
يتم قياس السعة الحرارية النوعية للمادة بـ :
- الفرق في درجات الحرارة، ويقاس بالدرجة المئوية ().
دعونا ننظر في مشكلة حساب كمية الحرارة.
مهمة
يحتوي كوب من النحاس كتلته بالجرام على ماء حجمه لتر عند درجة حرارة. ما مقدار الحرارة التي يجب نقلها إلى كوب من الماء حتى تصبح درجة حرارته مساوية؟

أرز. 5. توضيح لظروف المشكلة
أولا نكتب شرطا قصيرا ( منح) وتحويل جميع الكميات إلى النظام الدولي (SI).
|
منح: |
سي |
|
|
يجد: |
حل:
أولًا، حدد الكميات الأخرى التي نحتاجها لحل هذه المشكلة. باستخدام جدول السعة الحرارية النوعية (جدول 1) نجد (السعة الحرارية النوعية للنحاس، حيث أن الزجاج حسب الحالة نحاس)، (السعة الحرارية النوعية للماء، لأنه حسب الحالة يوجد ماء في الزجاج). بالإضافة إلى ذلك، نحن نعلم أنه لحساب كمية الحرارة نحتاج إلى كتلة من الماء. وفقًا للشرط، يُعطى لنا الحجم فقط. لذلك نأخذ من الجدول كثافة الماء: (الجدول 2).
طاولة 1. السعة الحرارية النوعية لبعض المواد،
طاولة 2. كثافات بعض السوائل
الآن لدينا كل ما نحتاجه لحل هذه المشكلة.
لاحظ أن الكمية النهائية للحرارة ستتكون من مجموع كمية الحرارة المطلوبة لتسخين الزجاج النحاسي وكمية الحرارة المطلوبة لتسخين الماء الموجود فيه:
دعونا أولاً نحسب كمية الحرارة اللازمة لتسخين كوب من النحاس:
قبل حساب كمية الحرارة اللازمة لتسخين الماء، دعونا نحسب كتلة الماء باستخدام صيغة مألوفة لنا من الصف السابع:
الآن يمكننا حساب:
ثم يمكننا حساب:
دعونا نتذكر ما يعنيه كيلوجول. البادئة "كيلو" تعني ![]() .
.
إجابة:.
ولتسهيل حل مسائل العثور على كمية الحرارة (ما يسمى بالمسائل المباشرة) والكميات المرتبطة بهذا المفهوم، يمكنك استخدام الجدول التالي.
|
الكمية المطلوبة |
تعيين |
الوحدات |
الصيغة الأساسية |
صيغة للكمية |
|
كمية الحرارة |
(أو نقل الحرارة).
السعة الحرارية النوعية للمادة.
السعة الحرارية- هي كمية الحرارة التي يمتصها الجسم عند تسخينه بمقدار درجة واحدة.
يُشار إلى السعة الحرارية لجسم ما بحرف لاتيني كبير مع.
على ماذا تعتمد السعة الحرارية للجسم؟ بادئ ذي بدء، من كتلته. ومن الواضح أن تسخين كيلوغرام واحد من الماء، على سبيل المثال، سيتطلب حرارة أكثر من تسخين 200 جرام.
وماذا عن نوع المادة؟ دعونا نقوم بالتجربة. لنأخذ وعاءين متطابقين، وبعد سكب الماء الذي يزن 400 جرام في أحدهما، وفي الآخر زيت نباتي يزن 400 جرام، سنبدأ في تسخينهما باستخدام شعلات متطابقة. ومن خلال مراقبة قراءات مقياس الحرارة سنرى أن الزيت يسخن بسرعة. لتسخين الماء والزيت إلى نفس درجة الحرارة، يجب تسخين الماء لفترة أطول. ولكن كلما قمنا بتسخين الماء لفترة أطول، كلما زادت الحرارة التي يتلقاها من الموقد.
وبالتالي، فإن تسخين نفس الكتلة من مواد مختلفة إلى نفس درجة الحرارة يتطلب كميات مختلفة من الحرارة. تعتمد كمية الحرارة اللازمة لتسخين الجسم، وبالتالي سعته الحرارية، على نوع المادة التي يتكون منها الجسم.
لذلك، على سبيل المثال، لزيادة درجة حرارة الماء وزنه 1 كجم بمقدار 1 درجة مئوية، يلزم وجود كمية حرارة تساوي 4200 جول، ولتسخين نفس الكتلة من زيت عباد الشمس بمقدار 1 درجة مئوية، يلزم وجود كمية من الحرارة تساوي مطلوب 1700ج.
تسمى الكمية الفيزيائية التي توضح مقدار الحرارة اللازمة لتسخين 1 كجم من المادة بمقدار 1 درجة مئوية السعة الحرارية محددةمن هذه المادة.
كل مادة لها قدرتها الحرارية الخاصة، والتي يُشار إليها بالحرف اللاتيني c وتُقاس بالجول لكل كيلوغرام درجة (J/(kg °C)).
تختلف السعة الحرارية النوعية لنفس المادة في حالات التجميع المختلفة (الصلبة والسائلة والغازية). على سبيل المثال، السعة الحرارية النوعية للماء هي 4200 جول/(كجم درجة مئوية)، والسعة الحرارية النوعية للثلج هي 2100 جول/(كجم درجة مئوية)؛ الألومنيوم في الحالة الصلبة لديه قدرة حرارية محددة تبلغ 920 جول/(كجم - درجة مئوية)، وفي الحالة السائلة - 1080 جول/(كجم - درجة مئوية).
لاحظ أن الماء لديه قدرة حرارية نوعية عالية جدًا. لذلك فإن الماء في البحار والمحيطات الذي يسخن في الصيف يمتص كمية كبيرة من الحرارة من الهواء. وبفضل هذا، في تلك الأماكن التي تقع بالقرب من المسطحات المائية الكبيرة، الصيف ليس حارا كما هو الحال في الأماكن البعيدة عن الماء.
حساب كمية الحرارة اللازمة لتسخين الجسم أو التي يطلقها أثناء التبريد.
ومما سبق يتبين أن كمية الحرارة اللازمة لتسخين الجسم تعتمد على نوع المادة التي يتكون منها الجسم (أي سعتها الحرارية النوعية) وعلى كتلة الجسم. ومن الواضح أيضًا أن كمية الحرارة تعتمد على عدد الدرجات التي سنزيد بها درجة حرارة الجسم.
لذا، لتحديد كمية الحرارة اللازمة لتسخين الجسم أو التي يطلقها أثناء التبريد، عليك ضرب السعة الحرارية النوعية للجسم بكتلته وبالفرق بين درجتي حرارته النهائية والابتدائية:
س = سم (ر 2 - ر 1 ) ,
أين س- كمية الحرارة، ج- السعة الحرارية محددة، م- كتلة الجسم ، ر 1 - درجة الحرارة الأولية، ر 2 - درجة الحرارة النهائية .
عندما يسخن الجسم ر2> ر 1 وبالتالي س > 0 . عندما يبرد الجسم ر 2ط< ر 1 وبالتالي س< 0 .
إذا عرفت السعة الحرارية للجسم كله مع, ستحددها الصيغة:
س = ج (ر 2 - ر 1 ) .
يمكن أن تتغير الطاقة الداخلية للجسم بسبب عمل القوى الخارجية. لتوصيف التغير في الطاقة الداخلية أثناء نقل الحرارة، تم إدخال كمية تسمى كمية الحرارة ويشار إليها بـ Q.
في النظام الدولي، وحدة الحرارة، وكذلك الشغل والطاقة، هي الجول: = = = 1 J.
ومن الناحية العملية، يتم أحيانًا استخدام وحدة غير نظامية لكمية الحرارة - السعرات الحرارية. 1 كالوري. = 4.2 ج.
وتجدر الإشارة إلى أن مصطلح "كمية الحرارة" أمر مؤسف. تم تقديمه في وقت كان يُعتقد فيه أن الأجسام تحتوي على سائل معين عديم الوزن وبعيد المنال - السعرات الحرارية. من المفترض أن عملية التبادل الحراري تتكون من حقيقة أن السعرات الحرارية المتدفقة من جسم إلى آخر تحمل معها كمية معينة من الحرارة. الآن، بمعرفة أساسيات النظرية الحركية الجزيئية لبنية المادة، نفهم أنه لا يوجد سعر حراري في الأجسام، وأن آلية تغيير الطاقة الداخلية للجسم مختلفة. ومع ذلك، فإن قوة التقليد عظيمة ونحن مستمرون في استخدام مصطلح تم تقديمه على أساس أفكار غير صحيحة حول طبيعة الحرارة. في الوقت نفسه، لفهم طبيعة انتقال الحرارة، لا ينبغي للمرء أن يتجاهل تماما المفاهيم الخاطئة حول هذا الموضوع. على العكس من ذلك، من خلال إجراء تشبيه بين تدفق الحرارة وتدفق سائل افتراضي من السعرات الحرارية، وكمية الحرارة وكمية السعرات الحرارية، عند حل فئات معينة من المشاكل، فمن الممكن تصور العمليات الجارية وبشكل صحيح حل المشاكل. في النهاية، تم الحصول على المعادلات الصحيحة التي تصف عمليات نقل الحرارة على أساس أفكار غير صحيحة حول السعرات الحرارية كحامل للحرارة.
دعونا نفكر بمزيد من التفصيل في العمليات التي يمكن أن تحدث نتيجة للتبادل الحراري.
صب بعض الماء في أنبوب الاختبار وأغلقه بسدادة. نعلق أنبوب الاختبار من قضيب مثبت في حامل ونضع لهبًا مفتوحًا تحته. يتلقى أنبوب الاختبار كمية معينة من الحرارة من اللهب، فترتفع درجة حرارة السائل الموجود فيه. مع ارتفاع درجة الحرارة، تزداد الطاقة الداخلية للسائل. تحدث عملية تبخر مكثفة. يؤدي تمدد الأبخرة السائلة إلى إجراء عمل ميكانيكي لدفع السدادة خارج أنبوب الاختبار.
دعونا نجري تجربة أخرى مع نموذج لمدفع مصنوع من قطعة أنبوب نحاسي مثبت على عربة. على جانب واحد، يتم إغلاق الأنبوب بإحكام بسدادة من الإيبونيت يتم من خلالها تمرير الدبوس. يتم لحام الأسلاك بالمسمار والأنبوب، وتنتهي بأطراف يمكن توصيل الجهد الكهربائي من شبكة الإضاءة إليها. وبالتالي فإن نموذج المدفع هو نوع من الغلايات الكهربائية.
 |
صب بعض الماء في ماسورة المدفع وأغلق الأنبوب بسدادة مطاطية. دعونا نربط البندقية بمصدر الطاقة. التيار الكهربائي الذي يمر عبر الماء يسخنه. يغلي الماء، مما يؤدي إلى تكوين بخار كثيف. يزداد ضغط بخار الماء، وفي النهاية يقومون بدفع السدادة خارج ماسورة البندقية.
تتدحرج البندقية بسبب الارتداد في الاتجاه المعاكس لإخراج القابس.
كلتا التجربتين متحدتان بالظروف التالية. في عملية تسخين السائل بطرق مختلفة، زادت درجة حرارة السائل، وبالتالي زادت طاقته الداخلية. لكي يغلي السائل ويتبخر بشكل مكثف، كان من الضروري الاستمرار في تسخينه.
تقوم الأبخرة السائلة بسبب طاقتها الداخلية بعمل ميكانيكي.
 |
نحن نتحقق من اعتماد كمية الحرارة اللازمة لتسخين الجسم على كتلته وتغيرات درجة الحرارة ونوع المادة. لدراسة هذه التبعيات سوف نستخدم الماء والنفط. (لقياس درجة الحرارة في التجربة يتم استخدام ميزان حرارة كهربائي مصنوع من مزدوجة حرارية متصلة بجلفانومتر مرآة. ويتم إنزال إحدى الوصلات المزدوجة الحرارية في وعاء به ماء بارد لضمان ثبات درجة حرارته. والوصلة الحرارية الأخرى تقيس درجة حرارة السائل. قيد الدراسة).
تتكون التجربة من ثلاث سلاسل. في السلسلة الأولى، بالنسبة لكتلة ثابتة من سائل معين (في حالتنا، الماء)، تتم دراسة اعتماد كمية الحرارة اللازمة لتسخينه على التغيرات في درجات الحرارة. سوف نحكم على كمية الحرارة التي يتلقاها السائل من المدفأة (الموقد الكهربائي) من خلال زمن التسخين، على افتراض أن هناك علاقة طردية بينهما. لكي تتوافق نتيجة التجربة مع هذا الافتراض، من الضروري ضمان تدفق حرارة ثابت من الموقد الكهربائي إلى الجسم الساخن. للقيام بذلك، تم توصيل الموقد الكهربائي بالشبكة مسبقًا، بحيث تتوقف درجة حرارة سطحه عن التغير مع بداية التجربة. لتسخين السائل بشكل متساوٍ أثناء التجربة، سنقوم بتقليبه باستخدام المزدوج الحراري نفسه. سوف نسجل قراءات الترمومتر على فترات منتظمة حتى تصل نقطة الضوء إلى حافة المقياس.
لنستنتج: أن هناك علاقة طردية طردية بين كمية الحرارة اللازمة لتسخين الجسم والتغير في درجة حرارته.
في السلسلة الثانية من التجارب سوف نقوم بمقارنة كميات الحرارة اللازمة لتسخين سوائل متطابقة ذات كتل مختلفة عندما تتغير درجة حرارتها بنفس المقدار.
ولتسهيل مقارنة القيم التي تم الحصول عليها، سيتم اعتبار كتلة الماء في التجربة الثانية أقل بمرتين مما كانت عليه في التجربة الأولى.
سنقوم مرة أخرى بتسجيل قراءات مقياس الحرارة على فترات منتظمة.
وبمقارنة نتائج التجربتين الأولى والثانية يمكن استخلاص الاستنتاجات التالية.
في السلسلة الثالثة من التجارب سوف نقوم بمقارنة كميات الحرارة اللازمة لتسخين كتل متساوية من السوائل المختلفة عندما تتغير درجة حرارتها بنفس المقدار.
سنقوم بتسخين الزيت على موقد كهربائي، كتلته تساوي كتلة الماء في التجربة الأولى. سوف نقوم بتسجيل قراءات مقياس الحرارة على فترات منتظمة.
تؤكد نتيجة التجربة الاستنتاج القائل بأن كمية الحرارة اللازمة لتسخين الجسم تتناسب طرديًا مع التغير في درجة حرارته، بالإضافة إلى أنها تشير إلى اعتماد هذه الكمية من الحرارة على نوع المادة.
بما أن التجربة استخدمت زيتًا كثافته أقل من كثافة الماء، وتسخين الزيت إلى درجة حرارة معينة يتطلب حرارة أقل من تسخين الماء، فيمكن افتراض أن كمية الحرارة اللازمة لتسخين جسم ما تعتمد على طاقته. كثافة.
لاختبار هذا الافتراض، سنقوم في نفس الوقت بتسخين كتل متساوية من الماء والبارافين والنحاس على سخان طاقة ثابت.
بعد نفس الوقت، تكون درجة حرارة النحاس حوالي 10 مرات، والبارافين حوالي 2 مرات أعلى من درجة حرارة الماء.
لكن كثافة النحاس أعلى وكثافة البارافين أقل من كثافة الماء.
تظهر التجربة أن الكمية التي تميز معدل التغير في درجة حرارة المواد التي تتكون منها الأجسام المشاركة في التبادل الحراري ليست الكثافة. تسمى هذه الكمية بالسعة الحرارية النوعية للمادة ويشار إليها بالحرف c.
 |
يتم استخدام جهاز خاص لمقارنة السعات الحرارية المحددة للمواد المختلفة. يتكون الجهاز من رفوف يتم فيها ربط لوحة بارافين رفيعة وشريط بقضبان تمر عبره. يتم تثبيت أسطوانات الألمنيوم والفولاذ والنحاس ذات الكتلة المتساوية في نهايات القضبان.
دعونا نقوم بتسخين الأسطوانات إلى نفس درجة الحرارة عن طريق غمرها في وعاء به ماء على موقد ساخن. دعونا نثبت الأسطوانات الساخنة على الرفوف ونحررها من أداة التثبيت. تلمس الأسطوانات صفيحة البارافين في نفس الوقت وتبدأ في ذوبان البارافين في الغرق فيها. تبين أن عمق غمر الأسطوانات من نفس الكتلة في صفيحة البارافين، عندما تتغير درجة حرارتها بنفس المقدار، يكون مختلفًا.
تظهر التجربة أن السعات الحرارية المحددة للألمنيوم والصلب والنحاس مختلفة.
بعد إجراء التجارب المناسبة مع ذوبان المواد الصلبة، وتبخير السوائل، واحتراق الوقود، حصلنا على التبعيات الكمية التالية.
للحصول على وحدات ذات كميات محددة، يجب التعبير عنها من الصيغ المقابلة وفي التعبيرات الناتجة وحدات بديلة للحرارة - 1 جول، الكتلة - 1 كجم، وللسعة الحرارية المحددة - 1 ك.
نحصل على الوحدات التالية: السعة الحرارية النوعية – 1 جول/كجم·ك، درجات الحرارة النوعية الأخرى: 1 جول/كجم.
